QIEP
Relacions estructura-funció: Sucrosa isomerasa
PRÀCTICA 1
Relacions estructura-funció de proteïnes
Queralt Datzira, Elsa Gutiérrez i Ariadna Parisi
- PRÀCTICA 1
- Informació sobre la proteïna
- Estructura de la proteïna
- Funció de la proteïna
Informació sobre la proteïna
La proteïna estudiada és l’enzim isomerasa de sacarosa, més concretament el gen mutB d’aquest enzim. El codi Uniprot d’aquest enzim: M1E1F7 i al tractar-se d’un enzim torbem també codi Brenda: EC.5.4.99.11. El codi PDB: 4H2C, ens determina que només hi ha una estructura a 1,70Å vàlida.
La seqüència de la proteïna és:
>4H2C_1|Chain A|Sucrose isomerase|Rhizobium (1071045)
KPGAPWWKSAVFYQVYPRSFKDTNGDGIGDFKGLTEKLDYLKGLGIDAIWINPHYASPNTDNGYDISDYREVMKEYGTMEDFDRLMAELKKRGMRLMVDVVINHSSDQHEWFKSSRASKDNPYRDYYFWRDGKDGHEPNNYPSFFGGSAWEKDPVTGQYYLHYFGRQQPDLNWDTPKLREELYAMLRFWLDKGVSGMRFDTVATYSKTPGFPDLTPEQMKNFAEAYTQGPNLHRYLQEMHEKVFDHYDAVTAGEIFGAPLNQVPLFIDSRRKELDMAFTFDLICYDRALDRWHTIPRTLADFRQTIDKVDAIAGEYGWNTFFLGNHDNPRAVSHFGDDRPQWREASAKALATVTLTQRGTPFIFQGDELGMTNYPFKTLQDFDDIEVKGFFQDYVETGKATAEELLTNVALTSRDNARTPFQWDDSANAGFTTGKPWLKVNPNYTEINAAREIGDPKSVYSFYRNLISIRHETPALSTGSYRDIDPSNADVYAYTRSQDGETYLVVVNFKAEPRSFTLPDGMHIAETLIESSSPAAPAAGAASLELQPWQSGIYKVK
Estructura de la proteïna
Treball amb ChimeraX
Tipus d’estructures secundàries detectades
Hem diferenciat les següents estructures secundàries en la proteïna:
- Hèlix alfa:
- Hèlix 3₁₀: Més compacta, amb 3 residus per volta i ponts d’hidrogen entre residus separats per 3 posicions.
- Hèlix α: La més comuna, amb 3.6 residus per volta estabilitzada per ponts d’hidrogen entre el C=O d’un residu i el N-H del residu situat 4 posicions més endavant.
- Fulles beta:
- Tipus 0: Cadenes perfectament alineades sense desplaçament.
- Tipus 1: Desplaçament d’un residu entre les cadenes.
- Tipus -1: Desplaçament en direcció oposada.
- Llaços: 7 llaços connectant estructures secundàries i permeten canvis de direcció.

Figura 1: Estructura de la proteïna amb els ponts d’hidrogen marcats.
Identifiquem 3158 Ponts d’hidrogen interns en total.
- Que formen part d’Hèlix alfa: 838
- Que formen part de Fulles beta: 273
- I la resta, formen part d’ Altres interaccions: 2047 (llaços, aigua, subunitats, etc.)
Per una millor visualització, hem assignat colors: vermell per a les hèlixs, blau per a les fulles i verd per als llaços.
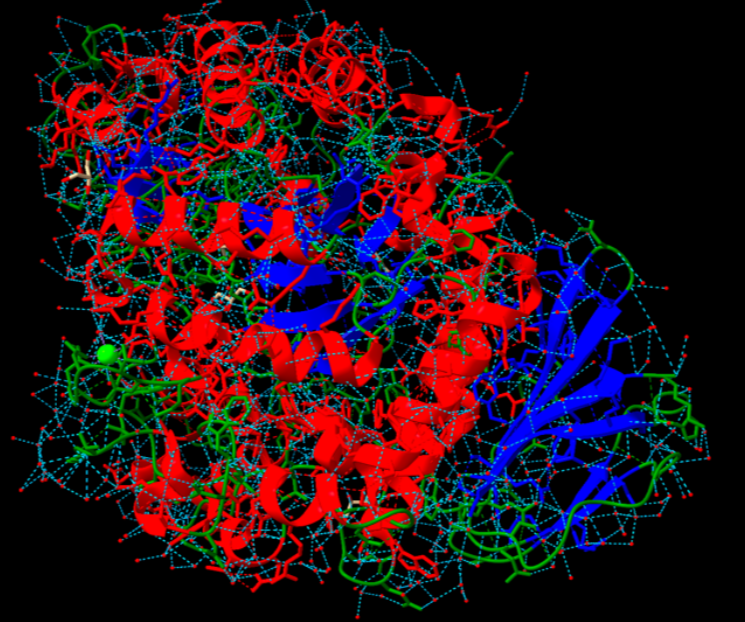
Figura 2: Estructura de la porteïna amb diferenciació de colors segons les estructures.
Motius de l’estructura supersecundària
El motiu detectat és helix-turn-helix, freqüent en factors de transcripció.
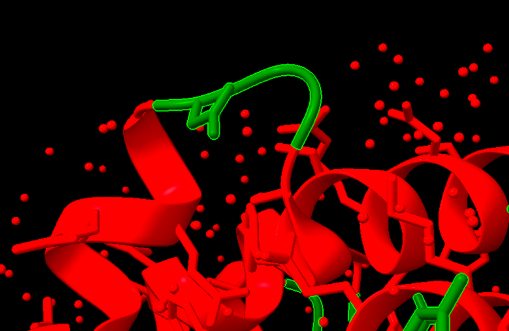
Figura 3: Visualització d’un motiu helix-turn-helix a l’estructura de la proteïna.
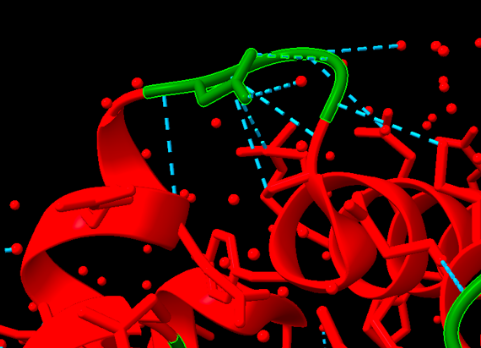
Figura 4: Motiu helix-turn-helix amb les interaccions ponts d’hidrogen marcats.
Aquest motiu beta-loop és comú en estructures beta i permet la connexió entre dues làmines beta antiparal·leles mitjançant un gir.
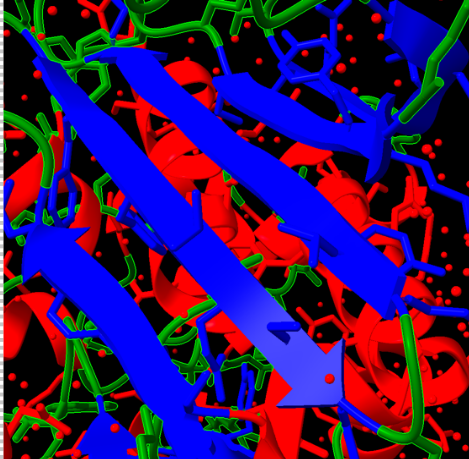
Figura 5: Visualització d’un motiu beta-loop a l’estructura de la proteïna.
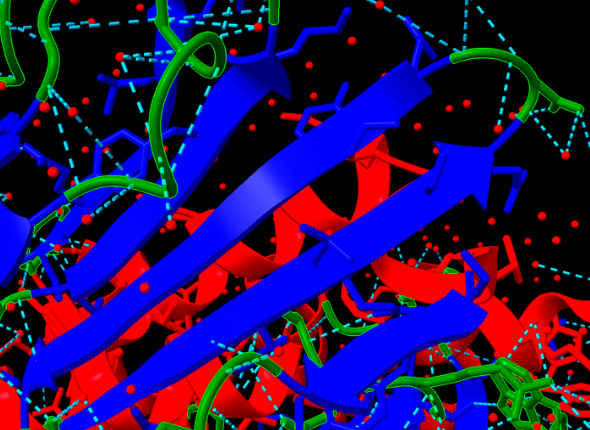
Figura 6: Motiu beta-loop amb les interaccions ponts d’hidrogen marcats.
Trobem Interaccions estabilitzadores com:
- Ponts d’hidrogen , els observem a través de les línies blaves discontínues i estabilitzen aquestes estructures.
- Interaccions van der Waals entre diferents elements estructurals.
Estructura terciària i classificació SCOP
L’estructura terciària es caracteritza per un plegament globular amb una disposició de barrel α/β, típic de les isomerases de sucrosa.
- Codi SCOP:
a.118.1.2 - Jerarquia SCOP:
- Classe: Proteïnes α/β
- Plegament: Barrel α/β tancat
- Superfamília: Barrel tipus isomerasa
- Família: Barrel tipus isomerasa
- Proteïna: Sucrose isomerase
Aquesta proteïna no té una estructura quaternària, ja que es presenta com una proteïna monomèrica i no forma complexos amb altres cadenes polipeptídiques.
Funció de la proteïna
Localització del centre actiu
El centre actiu de la proteïna es localitza al domini A i té forma de butxaca.

Figura 7: Centre actiu de l’enzim localitzat al domini A.
Residus rellevants
- Un residu nucleòfil
- El residu que actua com a àcid/base general: Glu254
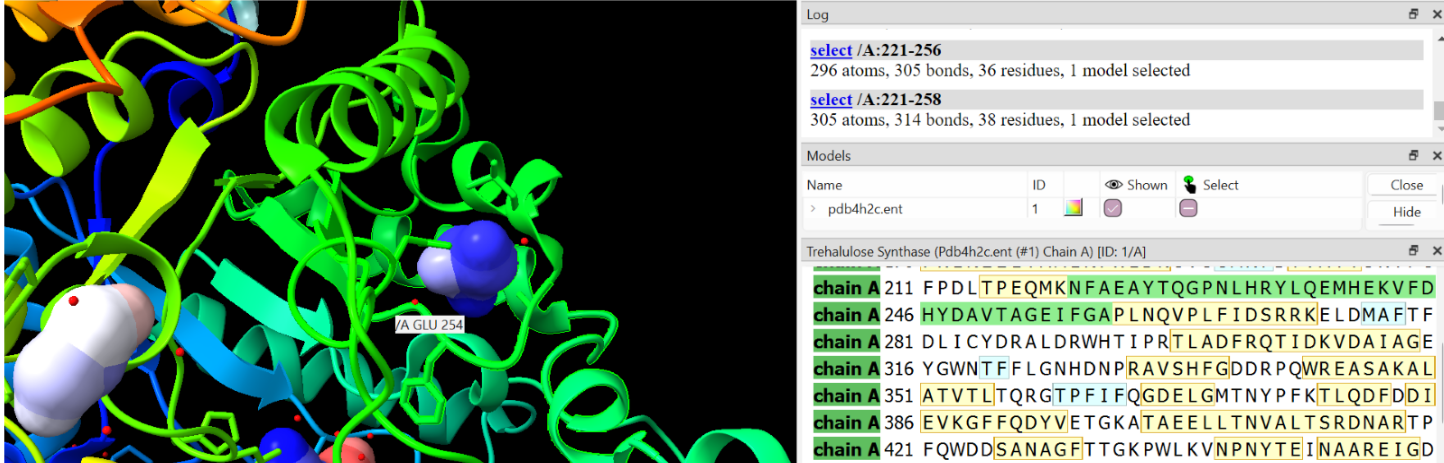
Figura 8: Residu àcid/base de la cadena A de l’enzim isomerasa de sacarosa identificat com Glu254.
- El residu que estabilitza l’estat de transició: Asp327 (No localitzable per la cristal·lografia de raigs X)
Substrats i inhibidors
- Substrat: La sacarosa, que es transforma per una reacció d’isomerització a isomaltulosa i trehalulosa.
- Inhibidors:
- Glucosa: Quan està unida al centre actiu, impedeix la unió del substrat i bloqueja la reacció.
- Deoxynojirimycin: Mencionat com a possible inhibidor, però sense activitat inhibidora demostrada.
Interaccions entre residus del centre actiu i substrat/inhibidor
Ponts salins
- Arg414 - Asp61
- Arg414 - Asp384
- Aquestes interaccions ajuden a mantenir la forma de butxaca funcional.
Ponts d’hidrogen
- Wat4101 (molècula d’aigua catalítica) forma enllaços d’hidrogen amb:
- Asn325
- Asp327
- Glu254
Interaccions aromàtiques
- Phe164 i Phe280 estableixen interaccions aromàtiques amb la glucosa.
Funció de la proteïna i mecanisme de reacció
L’isomerasa de sacarosa catalitza la conversió de sacarosa en isomaltulosa i trehalulosa per mitjà d’una isomerització, sense trencar la molècula. També pot hidrolitzar la sacarosa en monosacàrids com poden ser la glucosa i la fructosa.
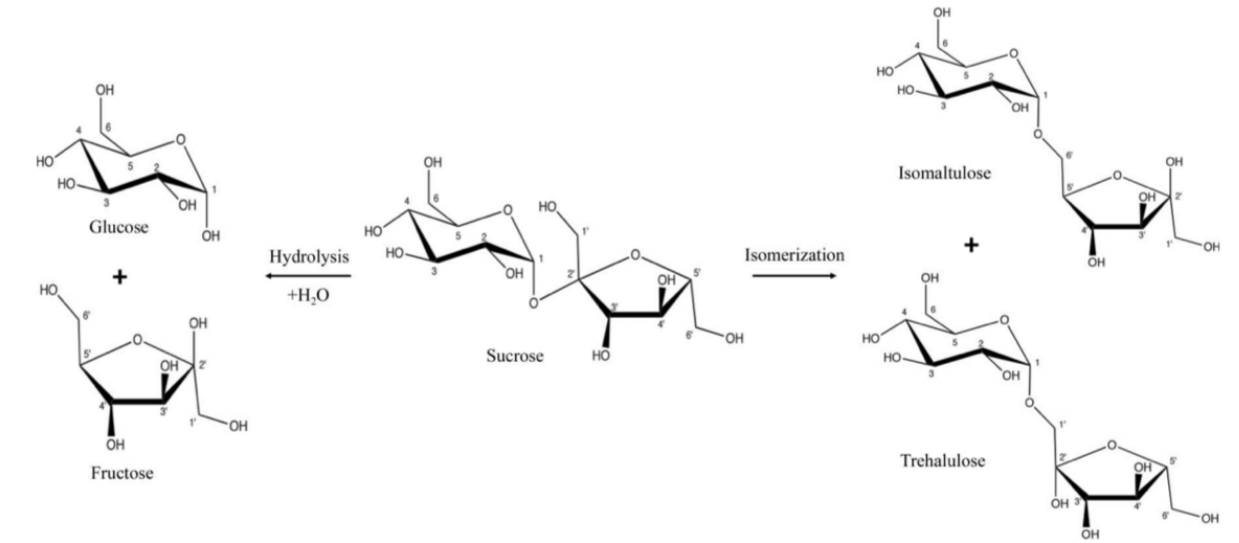
Figura 9: Mecanisme de reacció de l’enzim. Extret Acta Crystallographica.
Relació seqüència-estructura-funció
- Centre actiu en forma de butxaca: Impedeix l’entrada d’aigua i afavoreix la reacció d’isomerització.
- Interaccions estabilitzadores:
- Ponts salins (Arg414 - Asp61 - Asp384) mantenen la forma de la butxaca.
- Residus aromàtics (Phe164, Phe280) controlen la interacció amb el substrat.
- Asp327 i Glu254 són essencials per a la funció catalítica.
- Residus conservats (Asp61, Phe145, Phe164, Gln168, Arg414) contribueixen al reconeixement del substrat i estabilització del complex.
Residus clau per a la funció
- Asp327 i Glu254: Participen en la catàlisi mitjançant ponts d’hidrogen.
- Phe164 i Phe280: Regulen l’accés del substrat.
- Arg414, Asp61 i Asp384: Formen ponts salins per estabilitzar la conformació.
Variants de la proteïna i efectes funcionals
S’han identificat mutacions en:
- R284C i F164L: Afecten el centre actiu, obrint la butxaca i permetent l’entrada d’aigua.
- Això redueix la capacitat d’isomerització i afavoreix la hidròlisi de la sacarosa en glucosa i fructosa.
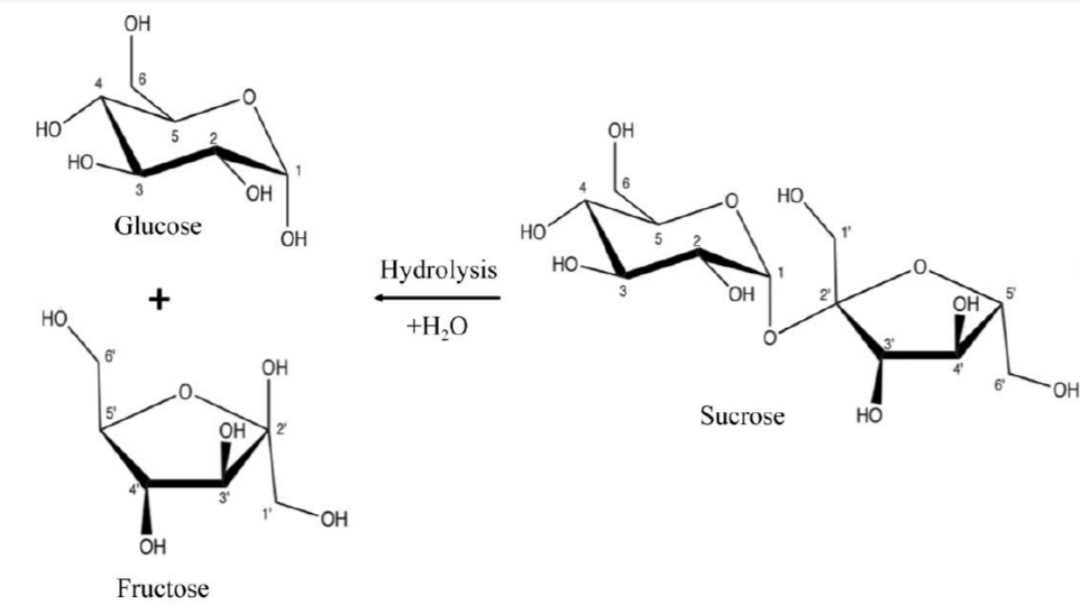
Figura 10: Funcionalitat de les variants de l’enzim. Extret Acta Crystallographica.