QIEP
Relacions estructura-funció: DNA ligasa
Pràctica 1
Grup F - Marc Conde, Marc Sánchez, Adrià Segura
Relacions estructura-funció de proteïnes
DNA ligase 1
Sobre la proteïna: Proteïna amb seqüència: MQRSIMSFFHPKKEGKAKKPEKEASNSSRETEPPPKAALKEWNGVVSESDSPVKRPGRKAARVLGSEGEEEDEALSPAKGQKPALDCSQVSPPRPATSPENNASLSDTSPMDSSPSGIPKRRTARKQLPKRTIQEVLEEQSEDEDREAKRKKEEEEEETPKESLTEAEVATEKEGEDGDQPTTPPKPLKTSKAETPTESVSEPEVATKQELQEEEEQTKPPRRAPKTLSSFFTPRKPAVKKEVKEEEPGAPGKEGAAEGPLDPSGYNPAKNNYHPVEDACWKPGQKVPYLAVARTFEKIEEVSARLRMVETLSNLLRSVVALSPPDLLPVLYLSLNHLGPPQQGLELGVGDGVLLKAVAQATGRQLESVRAEAAEKGDVGLVAENSRSTQRLMLPPPPLTASGVFSKFRDIARLTGSASTAKKIDIIKGLFVACRHSEARFIARSLSGRLRLGLAEQSVLAALSQAVSLTPPGQEFPPAMVDAGKGKTAEARKTWLEEQGMILKQTFCEVPDLDRIIPVLLEHGLERLPEHCKLSPGIPLKPMLAHPTRGISEVLKRFEEAAFTCEYKYDGQRAQIHALEGGEVKIFSRNQEDNTGKYPDIISRIPKIKLPSVTSFILDTEAVAWDREKKQIQPFQVLTTRKRKEVDASEIQVQVCLYAFDLIYLNGESLVREPLSRRRQLLRENFVETEGEFVFATSLDTKDIEQIAEFLEQSVKDSCEGLMVKTLDVDATYEIAKRSHNWLKLKKDYLDGVGDTLDLVVIGAYLGRGKRAGRYGGFLLASYDEDSEELQAICKLGTGFSDEELEEHHQSLKALVLPSPRPYVRIDGAVIPDHWLDPSAVWEVKCADLSLSPIYPAARGLVDSDKGISLRFPRFIRVREDKQPEQATTSAQVACLYRKQSQIQNQQGEDSGSDPEDTY Proteïna trobada: P18858 Nom del gen: DNLI1_HUMAN DNA ligase 1 Organisme: Homo Sapiens EC: 6.5.1.1 PBD: 7QNZ (1-919) 4.58 Å Funció: lligasa de l’ADN que segella els nicks en doble cadena durant la reparació de l’ADN. També participen en la replicació de l’ADN i la recombinació de l’ADN. Té activitat catalítica i un cofactor (Mg2+).
2. Treball amb ChimeraX Tipus d’estructures secundàries: El tipus d’estructures secundàries que conté la nostra proteïna són:
- Hèlix-α: Format per un total de 3448 àtoms, 3463 bonds (enllaços) i 443 residus repartits en 2 estructures (Humann LIG1 i Human PCNA), també, aquesta estructura està constituïda per 386 pseudoenllaços que tots aquests representen ponts d’hidrogen.
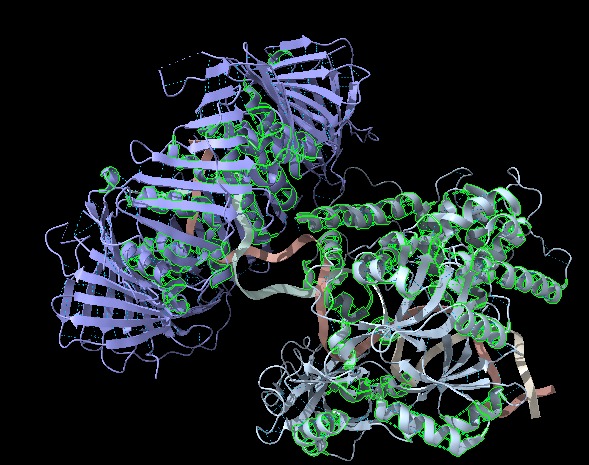
Figura 1: Imatge pròpia que mostra les hèlixs (ChimeraX).
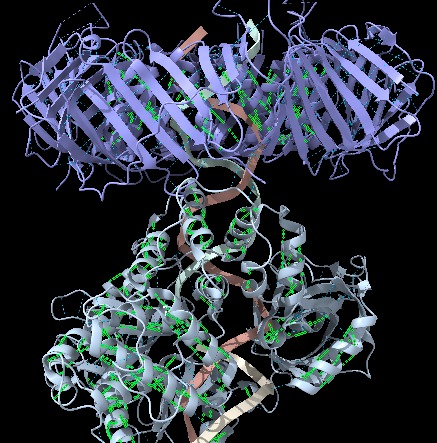
Figura 2: Imatge pròpia que mostra els ponts d’hidrogen interns de les hèlixs (ChimeraX).
- β-sheet (strand): Format per un total de 3678 àtoms, 3671 bonds (enllaços) i 470 residus repartits en 2 estructures (Human LIG1 i Human PCNA), també, aquesta estructura està constituïda per 390 pseudoenllaços que tots aquests representen ponts d’hidrogen.
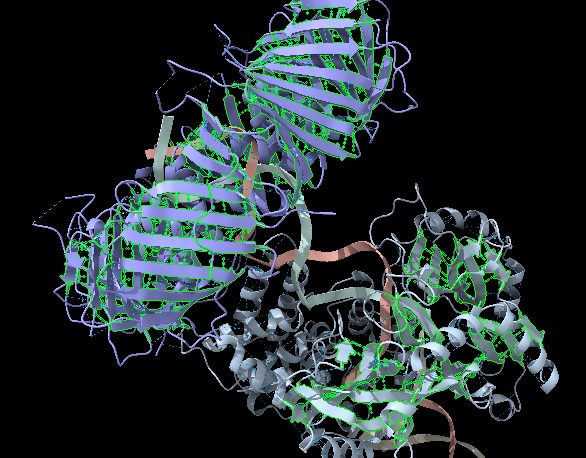
Figura 3: Imatge pròpia que mostra les fulles (ChimeraX).
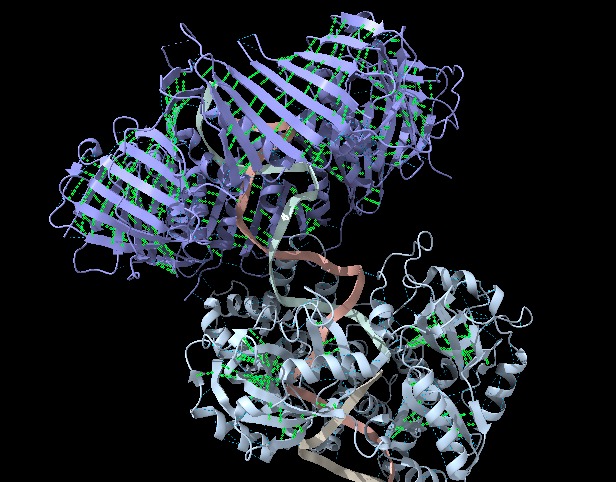
Figura 4: Imatge pròpia que mostra els ponts d’hidrogen interns de les fulles (ChimeraX).
- β-turns(Coils): Format per un total de 3527 àtoms, 3475 bonds (enllaços) i 477 residus repartatis en 2 estructures(Human LIG1 i Human PCNA), també, aquesta estructura està constituida per 151 pseudoenllaços que tots aquests representen ponts d’hidrogen
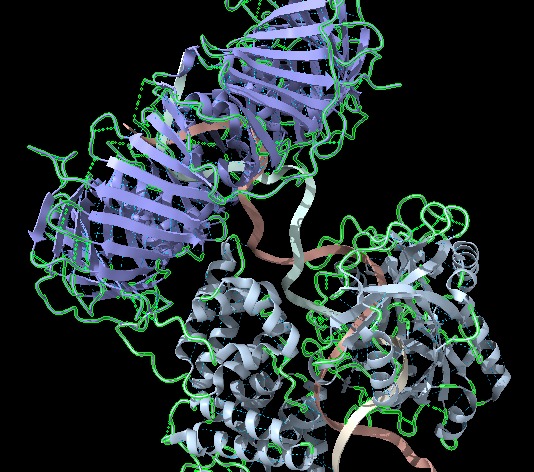
Figura 5: Imatge pròpia que mostra els llaços (ChimeraX).
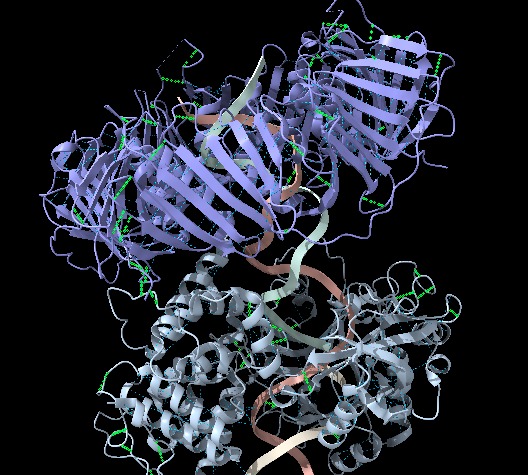
Figura 6: Imatge pròpia que mostra els ponts d’hidrogen interns dels llaços (ChimeraX).
Motius d’estructura supersecundària: Si que trobem estructures supersecundàries, l’estructura Human PCNA està formada quasi en la seva totalitat per β-meander motifs, compostos de dues o més cadenes β antiparal·leles consecutives unides entre si per hairpin loops.
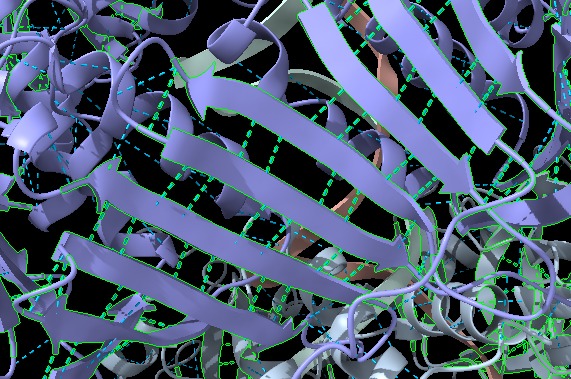
Figura 7: Imatge pròpia que mostra l’estructura β-meander motif i els ponts d’hidrogen que forma (ChimeraX).
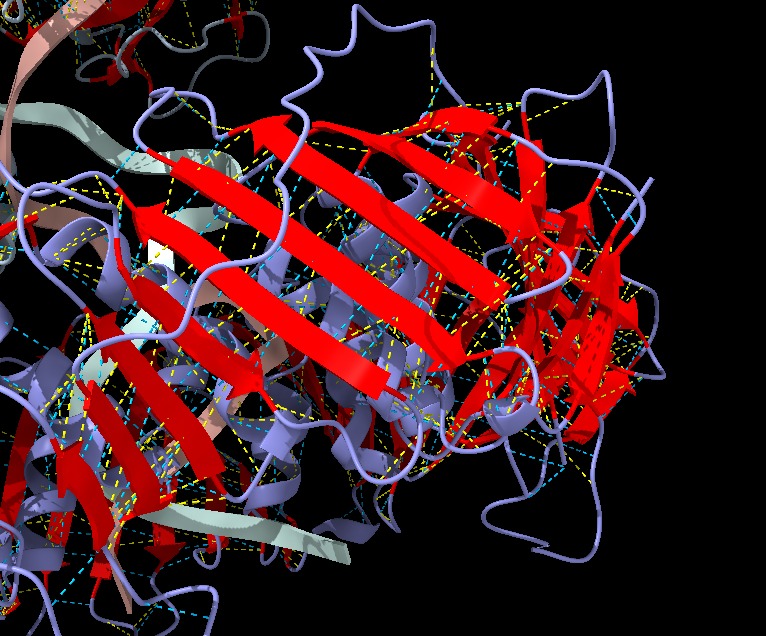
Figura 8: Imatge pròpia que mostra les interaccions de van der Waals del β-meander motif (ChimeraX).
L’estructura Human LIG1 forma algunes Helix-turn-helix, aquests motius li conferèixin la capacitat a la LIG1 d’unir-se al DNA; el monòmer incorpora dues hèlixs α, unides per una cadena curta d’aminoàcids, que s’uneixen al solc gran de l’ADN.
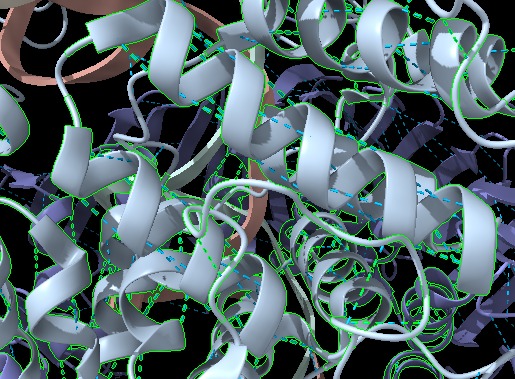
Figura 9: Imatge pròpia que mostra l’estructura Helix-turn-helix i els ponts d’hidrogen que forma (ChimeraX).
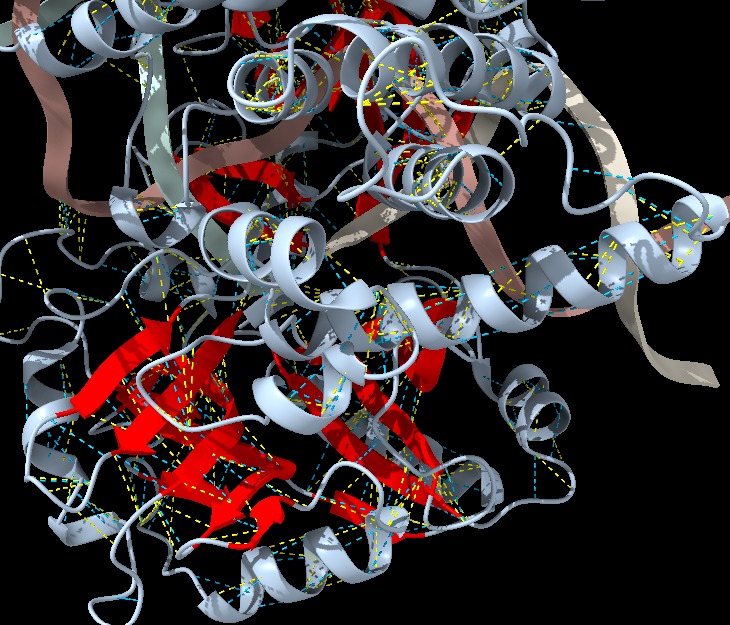
fFigura 10: Imatge pròpia que mostra les interaccions de van der Waals del Helix-turn-helix (ChimeraX).
Estructura terciària: El tipus de plegament de l’estructura terciària de la Human PCNA és:
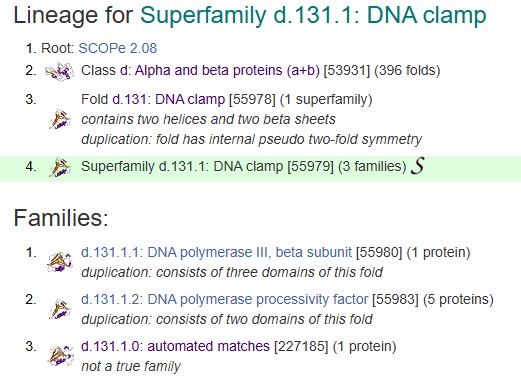
Figura 11: Codi i Jerarquía del plegament de la Human PCNA.
El tipus de plegament de l’estructura terciària de la Human LIG1 és:
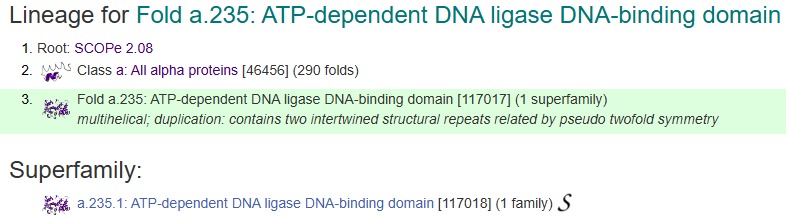
Figura 12: Codi i Jerarquía del plegament de la LIG1.
3. Funció de la proteïna Centre actiu: Per trobar el centre actiu hem buscat el substrat d’aquest, què és l’adenosina monofosfat (AMP).
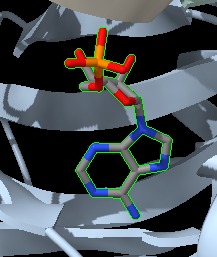
Figura 13: Imatge pròpia sobre el substrat AMP (ChimeraX).
Mitjançant el substrat les proteïnes que es trobin al costat de la AMP, formin ponts d’hidrogen o interaccions electroestàtiques fortes i siguin conegudes per estar conservades en altres ADN lligases seran els residus clau que formen part del centre actiu, com és el cas de: Lisina 568, Glutamat 720 i Glutamat 621, Arginina 573,Tirosina 567 (Tyr 567) i Fenilalanina 860 (Phe 860), entre d’altres com pot ser la Metionina 723. D’aquests podem destacar la lisina 568 què és un residu clau, formant un enllaç covalent amb l’AMP en el nostre enzim.
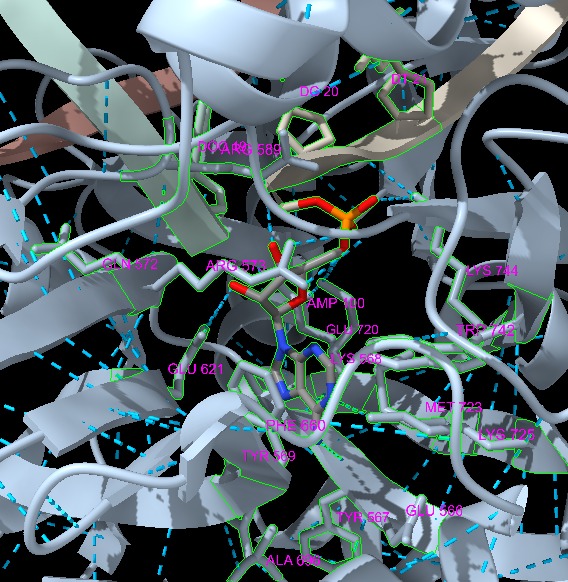
Figura 14: Imatge pròpia sobre els residus a 5Å del substrat amb els ponts d’hidrogen corresponent. Funció proteïna:
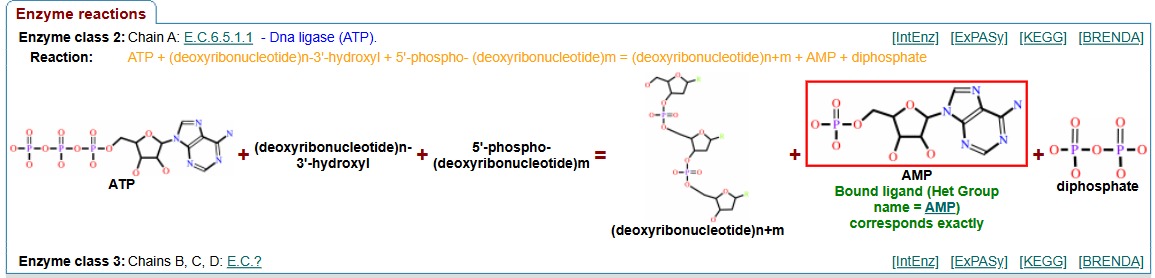
Figura 15: Reacció de la ligasa 1 humana.
El DNA ligasa catalitza la unió entre dos fragments d’ADN formant un enllaç fosfodièster. Aquest enllaç uneix l’extrem 3’-OH i el 5’-P. Per a dur a terme aquest procés, consumeix una molècula d’ATP, alliberant AMP i PPi. La PCNA és una altra proteïna que s’uneix a la LIG1 per fixar la ligasa a la cadena d’ADN i garantir el seu funcionament correcte.
Relació seqüència-estructura-funció:
Relació seqüència-estructura-funció:
La LIG1 està conformada per tres dominis diferents:
-
Domini N-terminal: el qual és l’utilitzat per tal d’interaccionar amb altres proteïnes com la PCNA, el que permet la localització de la ligasa en els llocs de reparació i replicació del DNA. El motiu que actua per tal d’unir-se a la PCNA és el PIPN-term, el qual conté residus que interaccionen amb la PCNA, a més a més, aquest motiu, a diferència d’altres, té una estructura desordenada i flexible, és per això que podrà acoblar-se d’una millor forma a la PCNA. Aquest domini està format per residus polars, els quals faciliten la interacció entre diferents proteïnes, a més d’aportar-hi flexibilitat. És en aquest domini on trobem també el motiu PIP DBD, el qual serà l’encarregat de mantenir la unió entre LIG1 i PCNA, una vegada el motiu PIPN-term deixi d’interaccionar entre aquests dos monòmers quan el DNA entri al complex. Sent PIP DBD un motiu amb baixa afinitat per la PCNA, conferint flexibilitat i dinamisme a LIG1 per realitzar la seva funció.
-
Domini central catalític: Lloc catalític el qual és l’encarregat de realitzar la reacció de lligació de l’ADN. Aquest domini conté residus conservats de lisina, els quals s’uneixen al AMP i són especials per a la catàlisi. Aquest domini és altament conservat amb regions hèlix i lamines beta que estabilitzen la reacció amb l’ADN.
-
Domini C-terminal: Aquest és important per tal d’estabilitzar el complex ADN-ligasa, assegurant la correcta orientació durant la reacció de la ligasa. Conté residus hidrofòbics i amb càrrega, els quals ajuden a estabilitzar la interacció amb la doble hèlix d’ADN.
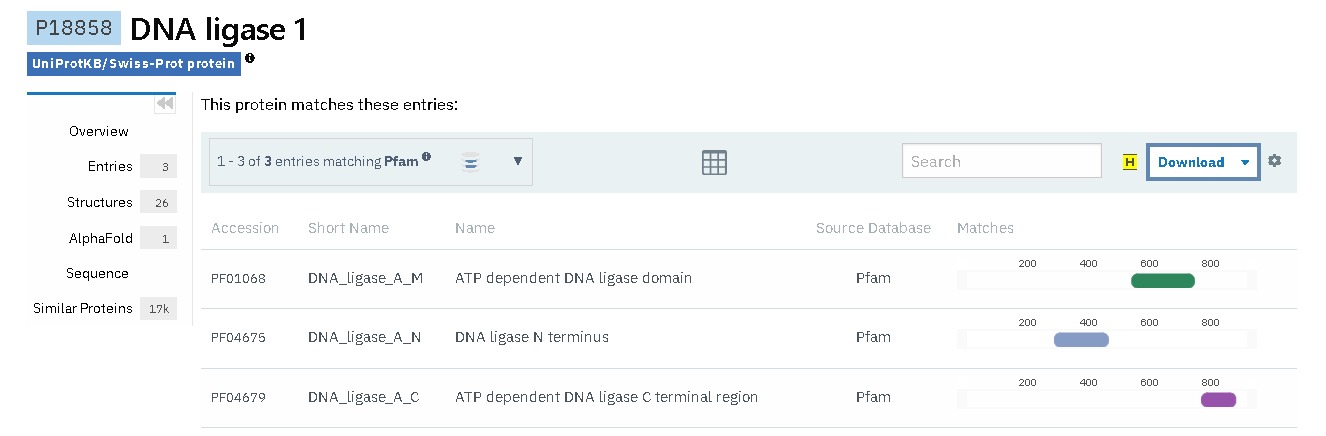
Figura 16: Dominis de la DNA Ligase I obtinguda del PFAM.
Per a la PCNA tenim només dos dominis:
- Domini N-terminal i Domini C-terminal: Els dominis N-terminal i C-terminal de PCNA són topològicament idèntics. Tres molècules de PCNA estan estretament associades per formar un anell tancat que envolta l’ADN dúplex.
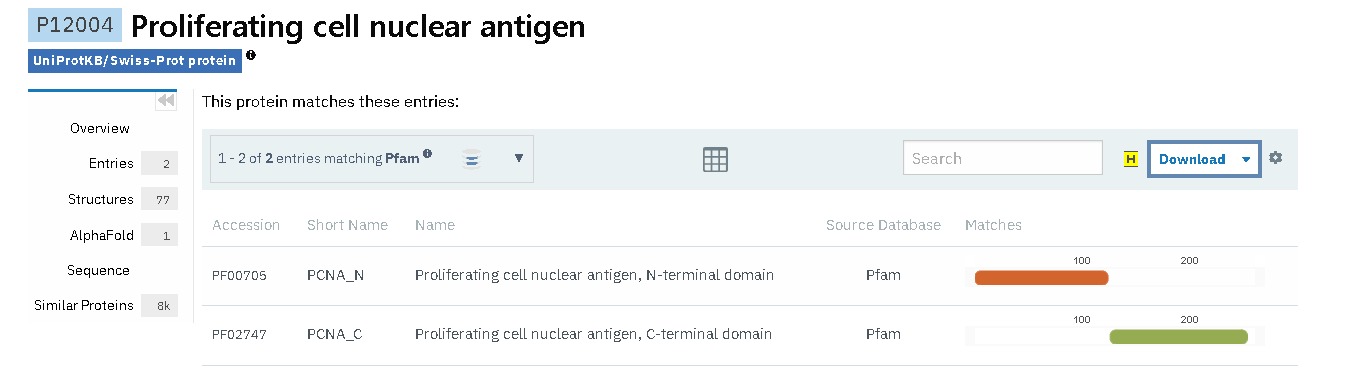
Figura 17: Dominis de la proteína PCNA obtinguda del PFAM.
La relació seqüència-estructura-funció del complex Lig1–DNA–PCNA és clau durant la síntesi de cadena retardada, l’ADN Ligasa 1 (Lig1) coopera amb la pinça lliscant PCNA per segellar els nicks entre els fragments d’Okazaki generats per Pol δ i Flap endonucleasa 1 (FEN1).
La unió de la PCNA a la regió N-terminal de la LIG1 ocorre a través del motiu PIPN-term, que actua com un primer ancoratge a PCNA. Abans de la regió d’unió a l’ADN (PIPDBD) de la LIG1 s’involucri, PIPN-term manté la LIG1 unida a PCNA, encara que en una varietat d’orientacions a causa de la flexibilitat conformacional del domini N-terminal. El motiu PIPN-term és una seqüència específica a la regió N-terminal de la lliga 1 (LIG1) que conté un PIP-box (Proliferating Cell Nuclear Antigen-Interacting Protein box). Aquest motiu permet la interacció inicial de LIG1 amb PCNA, ja que PIPN-term s’uneix al segon monòmer de PCNA, facilitant així el reclutament i estabilització de la unió.
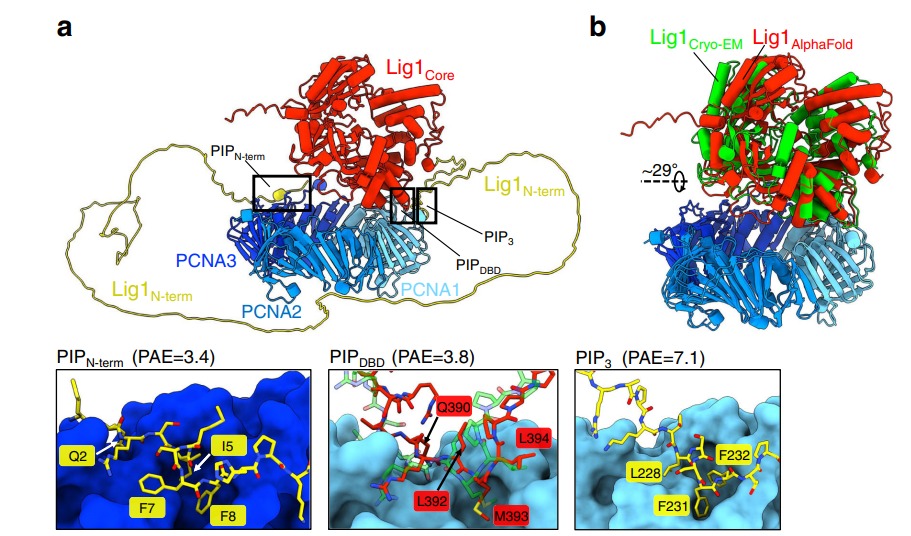
Figura 18: Predicció AlphaFold del complex Lig1-PCNA.
El complex LIG1−PCNA repara els nicks a l’ADN mitjançant un procés coordinat en què també participa FEN1(Flap Endonuclease 1). Tot comença quan FEN1, unit a un dels monòmers de PCNA, talla els fragments sobrants de l’ADN a la regió del nick i el manté doblegat en una posició exposada sobre la cara frontal de l’anell de PCNA. Aquesta disposició deixa l’ADN accessible per a la interacció següent amb la lligasa (LIG1). A continuació, LIG1 s’uneix a un altre monòmer lliure de PCNA mitjançant el domini PIPDBD, cosa que facilita la transferència de l’ADN des de FEN1 cap al seu lloc actiu. La flexibilitat del domini OBD de LIG1 permet que l’ADN passi d’un lloc a un altre sense dificultat, un procés conegut com a handoff. Durant aquest pas intermedi, la conformació de LIG1 s’ajusta per rebre l’ADN, assegurant que el domini DBD-AdD estigui obert i llest per abraçar la molècula entrant. Un cop l’ADN és completament envoltat per la lligasa, el domini OBD es tanca sobre el fil, estabilitzant-lo dins de la seva estructura. Finalment, LIG1 catalitza la formació de l’enllaç fosfodièster, segella el nick i restaura la continuïtat de la doble hèlix. D’aquesta manera, PCNA actua com a plataforma d’intercanvi que permet la transferència de l’ADN des de FEN1 a LIG1, assegurant una reparació eficient i precisa de l’ADN.
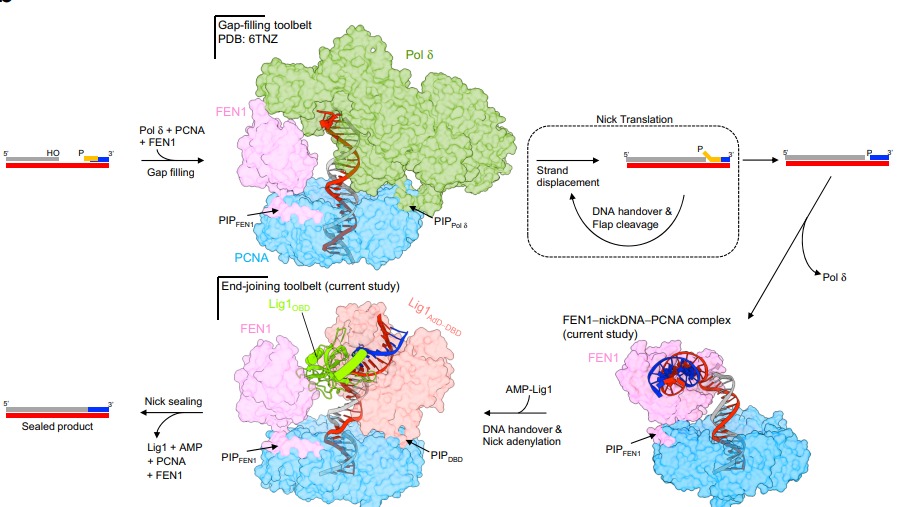
Figura 19: Bases estructurals proposades per a la funció dirigida per PCNA de Pol δ, FEN1 i Lig1 en la maduració del fragment d’Okazaki en humans.
Bibliografía
Georgescu, R. E., Yao, N. Y., & O’Donnell, M. E. (2022). Mechanism of human Lig1 regulation by PCNA in Okazaki fragment maturation. Nature Communications, 13, 7782. https://doi.org/10.1038/s41467-022-35475-z
InterPro. (s.f.). ATP5F1A protein domain analysis. European Bioinformatics Institute (EBI). Recuperado el 2 de marzo de 2025, de https://www.ebi.ac.uk/interpro/protein/UniProt/P18858/entry/pfam/#table
InterPro. (s.f.). ATP5F1B protein domain analysis. European Bioinformatics Institute (EBI). Recuperado el 2 de marzo de 2025, de https://www.ebi.ac.uk/interpro/protein/UniProt/P12004/entry/pfam/#table
PDBsum. (s.f.). Structural summaries of proteins. European Bioinformatics Institute (EBI). Recuperado el 2 de marzo de 2025, de https://www.ebi.ac.uk/thornton-srv/databases/pdbsum/
RCSB PDB. (s.f.). 7QNZ: Cryo-EM structure of human mitochondrial ATP synthase. RCSB Protein Data Bank. Recuperado el 2 de marzo de 2025, de https://www.rcsb.org/structure/7QNZ
UniProt. (s.f.). P18858 - ATP5F1A (Homo sapiens). UniProt. Recuperado el 2 de marzo de 2025, de https://www.uniprot.org/uniprotkb/P18858/entry
UniProt. (s.f.). P12004 - ATP5F1B (Homo sapiens). UniProt. Recuperado el 2 de marzo de 2025, de https://www.uniprot.org/uniprotkb/P12004/entry