QIEP
Grup H · Relacions estructura-funció: Receptor β2 adrenèrgic
Grup H
Grup H · Pràctica 1. Relacions estructura-funció: Receptor ß-2 adrenèrgic
Grup H: Estel Boix, Carla Masip, Marc Pardeiro
Índex
Introducció a la proteïna
Seqüència donada: DYKDDDDAMGQPGNGSAFLLAPNRSHAPDHDVTQQRDEVWVVGMGIVMSLIVLAIVFGNVLVITAIAKFERL QTVTNYFITSLACADLVMGLAVVPFGAAHILMKMWTFGNFWCEFWTSIDVLCVTASIWTLCVIAVDRYFAIT SPFKYQSLLTKNKARVIILMVWIVSGLTSFLPIQMHWYRATHQEAINCYAEETCCDFFTNQAYAIASSIVSF YVPLVIMVFVYSRVFQEAKRQLNIFEMLRIDEGLRLKIYKDTEGYYTIGIGHLLTKSPSLNAAKSELDKAIG RNTNGVITKDEAEKLFNQDVDAAVRGILRNAKLKPVYDSLDAVRRAALINMVFQMGETGVAGFTNSLRMLQQ KRWDEAAVNLAKSRWYNQTPNRAKRVITTFRTGTWDAYKFCLKEHKALKTLGIIMGTFTLCWLPFFIVNIVH VIQDNLIRKEVYILLNWIGYVNSGFNPLIYCRSPDFRIAFQELLCLRRSSLKHHHHHH
Nom de la proteïna: Receptor ß-2 adrenèrgic
Organisme: Homo sapiens
Codi UNIPROT: P07550
Gen: ADRB2
Estructura:
Codi PDB:
-
5D5A (domini amb millor resolució)
-
2R4R i 2RH1 (demés dominis)
Existeixen múltiples entrades corresponents a aquesta proteïna, com ara 2R4R, 2RH1 i 5D5A, que representen diferents determinacions estructurals en diverses condicions experimentals. Per aquest treball s’ha escollit l’estructura amb codi PDB 5D5A, ja que presenta una millor resolució (2.48 Å) i una cobertura més completa de la seqüència respecte a altres estructures disponibles. Al tenir millor resolució que tots els dominis ens permetrà analitzar l’estructura secundària amb més detall i concreció.
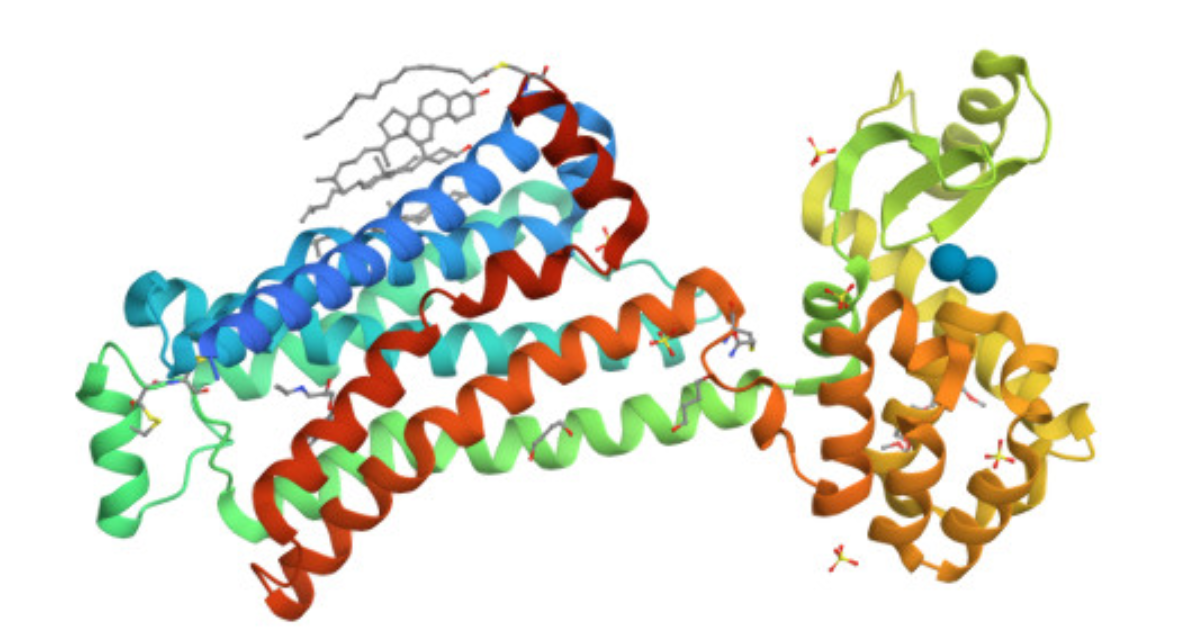 Figura 1. Estructura de la proteïna al PDB.
Figura 1. Estructura de la proteïna al PDB.
Funció:
L’ADRB2 és un receptor acoblat a proteïnes G per a catecolamines que pot activar tant les proteïnes Gs com Gi, generant vies de senyalització diferents. Té una afinitat aproximadament 30 vegades més alta per l’epinefrina que per la norepinefrina. Al cor, l’activació per epinefrina i norepinefrina indueix una taxa de contracció ràpida i lenta dels cardiomiòcits, respectivament. Les dues catecolamines activen principalment la via Gs/PKA, que modula la contracció dels miòcits. A més, l’epinefrina promou l’acoblament d’ADRB2 a les proteïnes G(i) per exercir efectes cardioprotectors, especialment en situacions d’hipòxia i estrès oxidatiu mitjançant la via PI3K/Akt. Finalment, ADRB2 també pot regular el pH cel·lular de manera independent de PKA modulant l’activitat de l’intercanviador Na⁺/H⁺ (SLC9A3).
Treball amb l’aplicació ChimeraX
Estructures secundàries
Detecteu les diferents estructures secundàries de la proteïna i determineu-ne el tipus (fulles, hèlix, llaços i les seves diferents variants). Mireu de descriure amb un cert detall els diferents tipus d’interaccions que podeu trobar dins aquestes estructures secundàries (mostreu els ponts d’hidrogen interns d’aquestes estructures secundàries).
La interacció més important són els ponts d’hidrogen (342) (figura 2), que es formen en la interacció entre el grup carbonil i el grup amida d’aminoàcids. Són interaccions intramoleculars (a la mateixa cadena) que estabilitzen les hèlixs (menys flexible). També podem trobar interaccions de Van der Waals, entre àtoms molt propers per estabilitzar l’empaquetament de la proteïna i interaccions hidrofòbiques, que tenen més importància en estructura terciària.
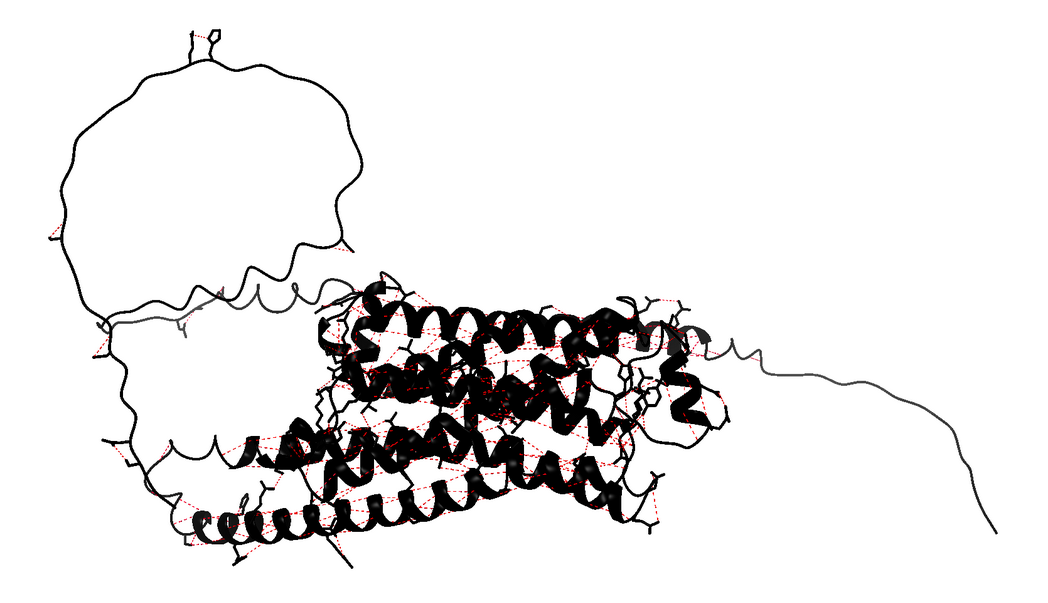 Figura 2. Imatge de les interaccions de ponts d’hidrogen al nostre receptor ADRB2.
Figura 2. Imatge de les interaccions de ponts d’hidrogen al nostre receptor ADRB2.
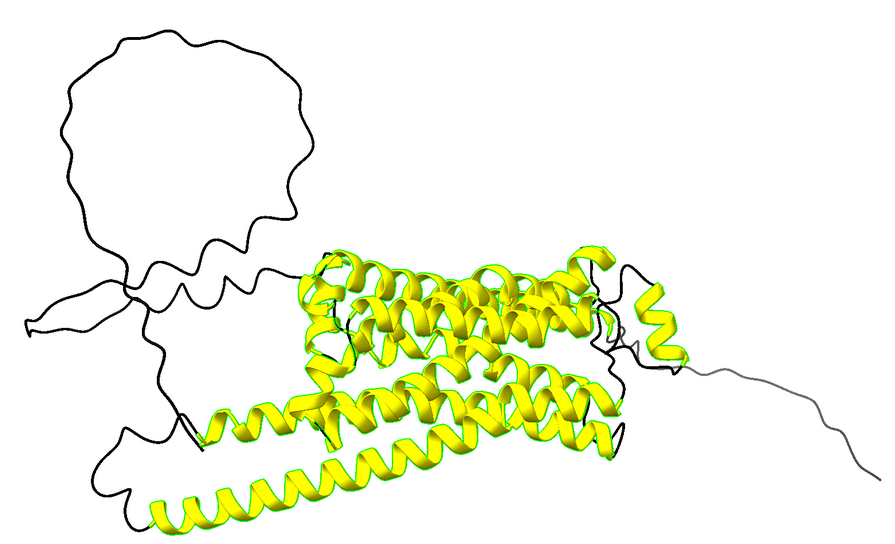
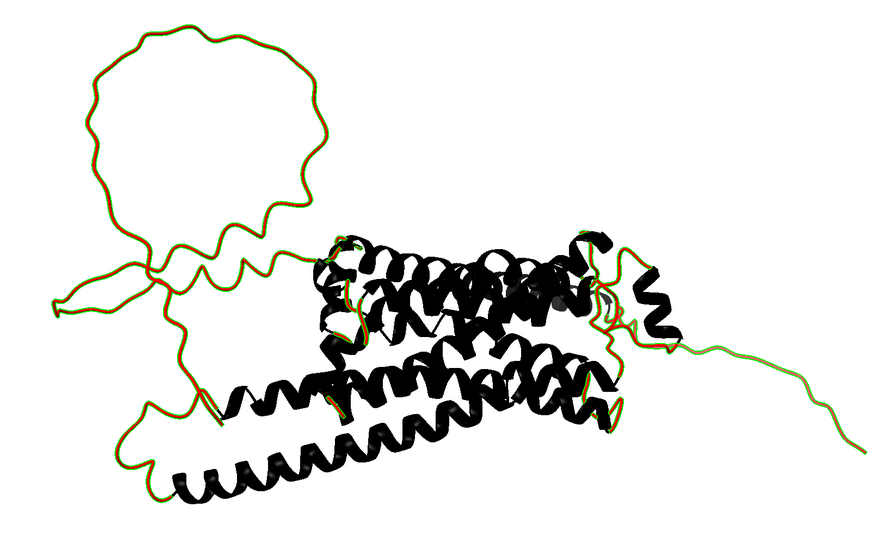 Figura 3. Imatges dels diferents tipus d’estructura secundària, la figura a representa les hèlix i la figura b representa els coils.
Figura 3. Imatges dels diferents tipus d’estructura secundària, la figura a representa les hèlix i la figura b representa els coils.
Al visualitzar la seqüència de cada subunitat de manera individual, les zones marcades en color groc són hèlixs alfa, mentre que les marcades en negre llima són coil.
Estructures supersecundàries
Podeu detectar-hi motius d’estructura supersecundària? Mostreu les interaccions (ponts d’hidrogen, van der Waals) entre els diferents elements que constitueixen aquestes estructures supersecundàries.
Segons la classificació de la base de dades SCOPe, la proteïna β2-adrenèrgica (ADRB2) pertany a la família f.13.1.3: amine receptor-like, dins del grup dels receptors acoblats a proteïnes G (GPCR).
S’hi identifiquen quatre dominis estructurals corresponents a diferents estructures resoltes experimentalment al Protein Data Bank: 2r4r (figura 4), 2rh1 (figura 5), 5d5a (figura 6) i 5x7d (figura 7). Aquests dominis presenten una arquitectura molt similar i corresponen a diferents determinacions estructurals del mateix receptor en diverses condicions experimentals (diferent resolució i presència de lligands o proteïnes fusionades).
Interaccions estabilitzadores Dins l’estructura supersecundària es poden identificar diferents tipus d’interaccions: Ponts d’hidrogen: estabilitzen les hèlixs α mitjançant interaccions entre els grups carbonil (C=O) i amida (N-H) del backbone peptídic. Interaccions hidrofòbiques: predominants a les regions transmembrana, on residus apolars interaccionen amb la bicapa lipídica i entre ells, contribuint a l’estabilitat del feix d’hèlixs. Interaccions de van der Waals: entre cadenes laterals compactades dins del nucli de la proteïna, afavorint un empaquetament eficient.
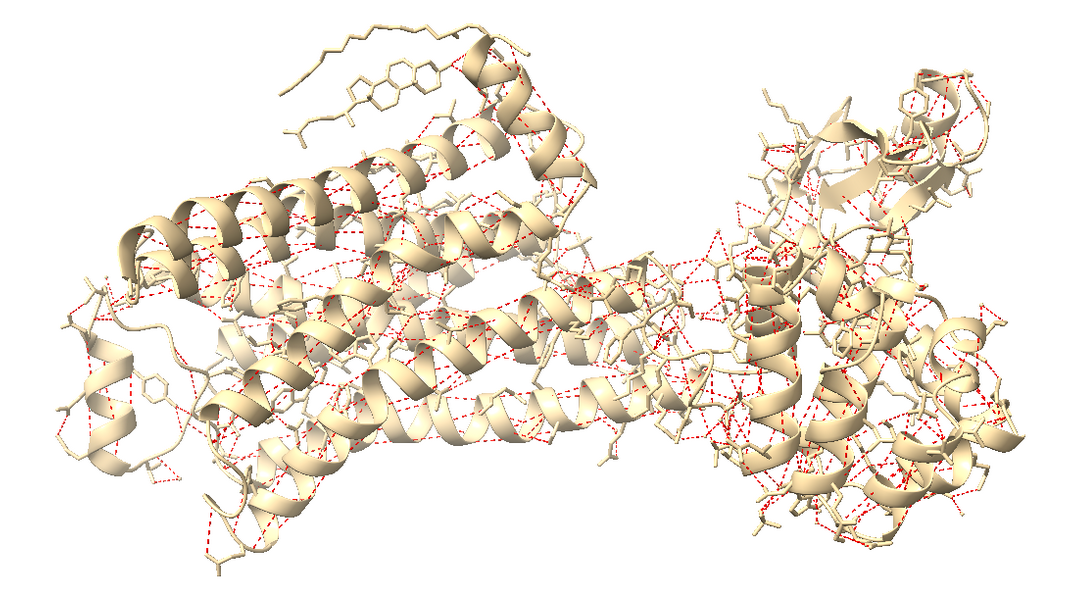
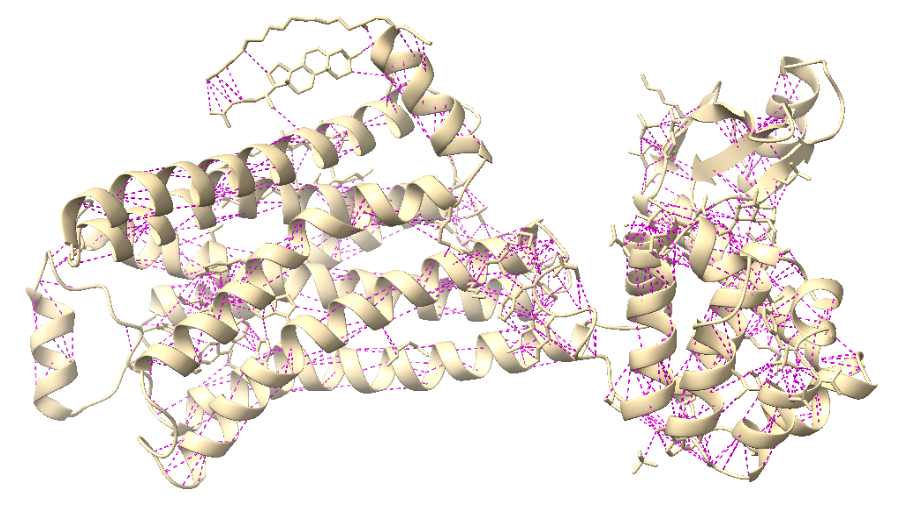 Figura 4. La figura a representa en vermell els ponts d’hidrogen del domini 2r4r (color beige) i la figura b representa les interaccions de VdW en rosa.
Figura 4. La figura a representa en vermell els ponts d’hidrogen del domini 2r4r (color beige) i la figura b representa les interaccions de VdW en rosa.
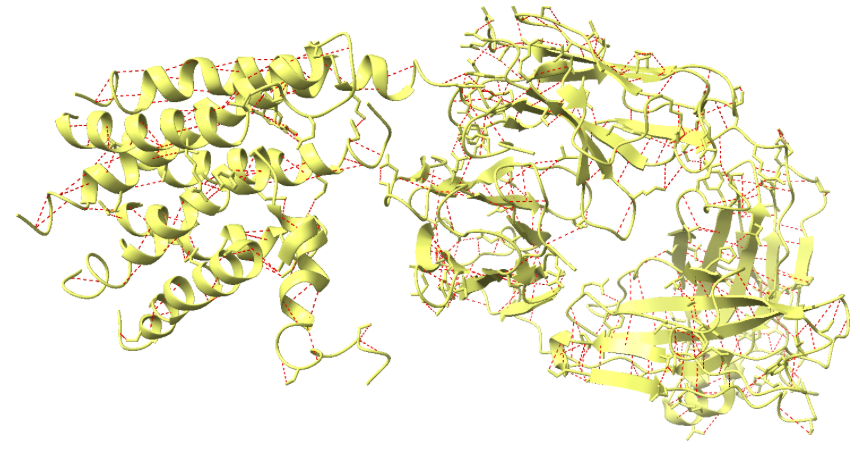
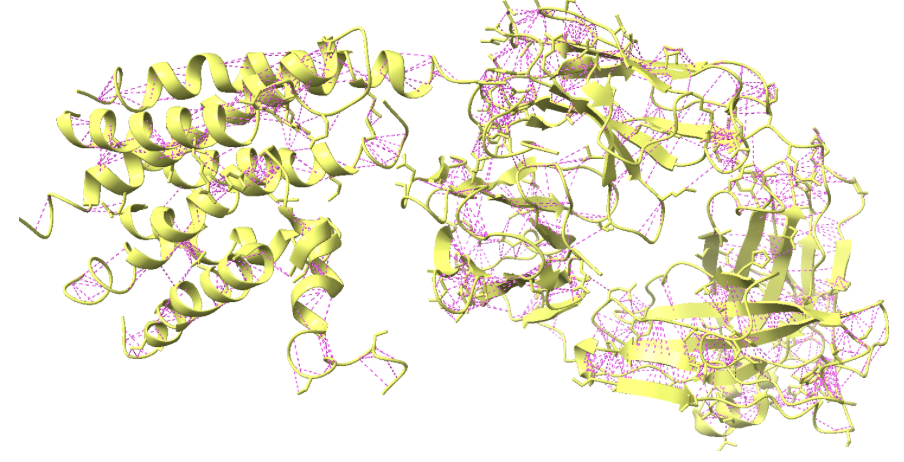 Figura 5. La figura a representa en vermell els ponts d’hidrogen del domini 2rh1 (color groc) i la figura b representa les interaccions de VdW en rosa.
Figura 5. La figura a representa en vermell els ponts d’hidrogen del domini 2rh1 (color groc) i la figura b representa les interaccions de VdW en rosa.
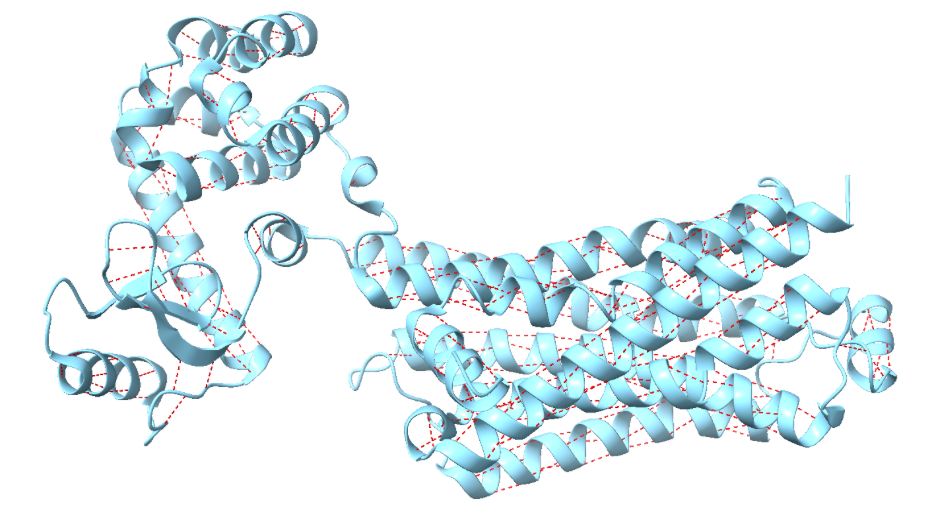
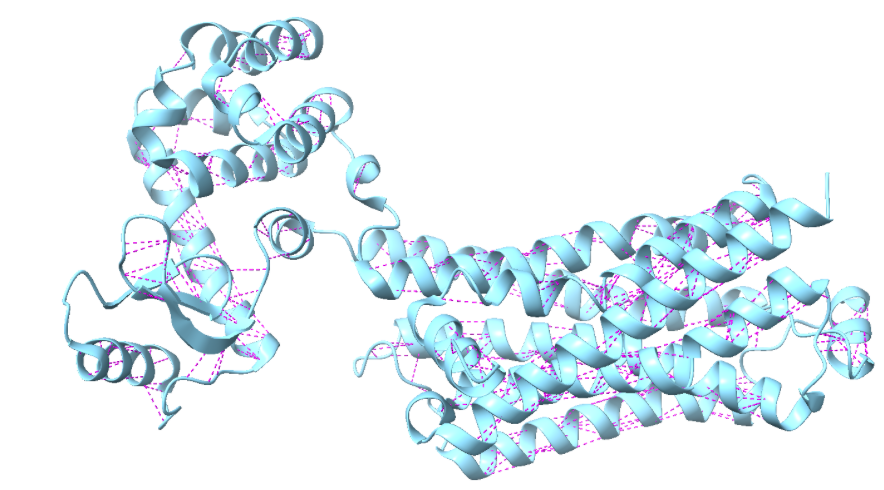 Figura 6. La figura a representa en vermell els ponts d’hidrogen del domini 5d5a (color blau) i la figura b representa les interaccions de VdW en rosa.
Figura 6. La figura a representa en vermell els ponts d’hidrogen del domini 5d5a (color blau) i la figura b representa les interaccions de VdW en rosa.
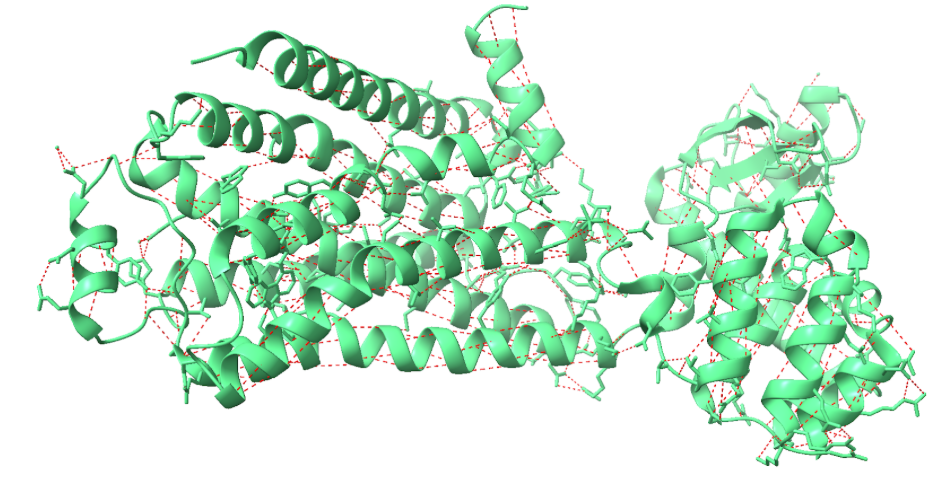
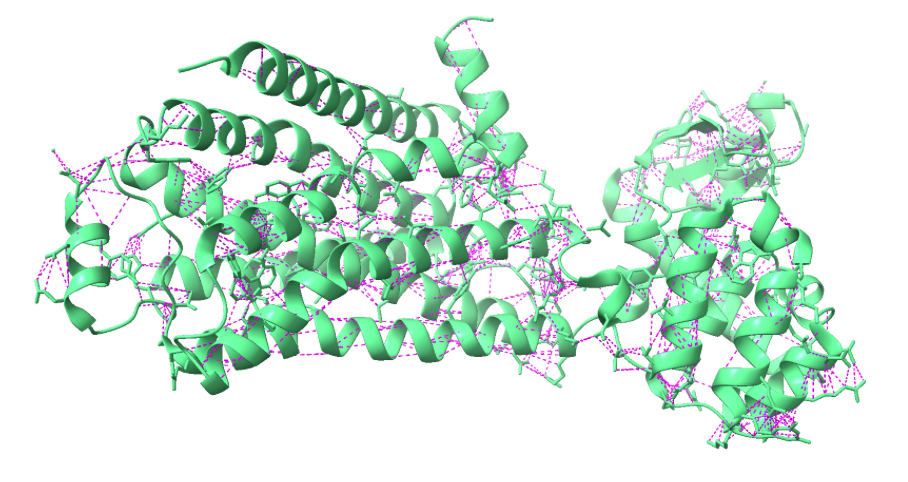 Figura 7. La figura a representa en vermell els ponts d’hidrogen del domini 5x7d (color verd) i la figura b representa les interaccions de VdW en rosa.
Figura 7. La figura a representa en vermell els ponts d’hidrogen del domini 5x7d (color verd) i la figura b representa les interaccions de VdW en rosa.
Estructura terciària
L’estructura terciària de la proteïna, a quin tipus de plegament correspon? Busqueu el plegament a la base de dades SCOP, anoteu el codi que us dona aquesta base de dades per al plegament i mostreu la jerarquía d’aquest plegament. En cas que existeixi estructura quaternària, discutiu-la també.
L’anàlisi de l’estructura terciària de la proteïna mitjançant CATH indica que pertany a la classe α, amb el codi CATH: 1.10.530.40 (figura 8), que correspon a una arquitectura basada en un feix d’hèlixs α transmembrana. El codi CATH (1.10.530.40) es desglossa en els diferents nivells jeràrquics: classe (1, principalment α), arquitectura (10, Orthogonal Bundle), topologia o plegament (530, Lysozyme) i superfamília homòloga (40).
Segons ECOD (P07550_F1_nD1), la proteïna s’inclou dins del grup: G protein-coupled receptor-like, que indica una relació evolutiva amb altres receptors de membrana implicats en processos de senyalització cel·lular.
Pel que fa als dominis (figura 9), la proteïna presenta diversos dominis a les hèlixs α, que conformen el nucli funcional del receptor, amb regions extracel·lulars i intracel·lulars.
Respecte l’estructura quaternària és principalment monomèrica, tot i que en alguns casos pot formar oligòmers.
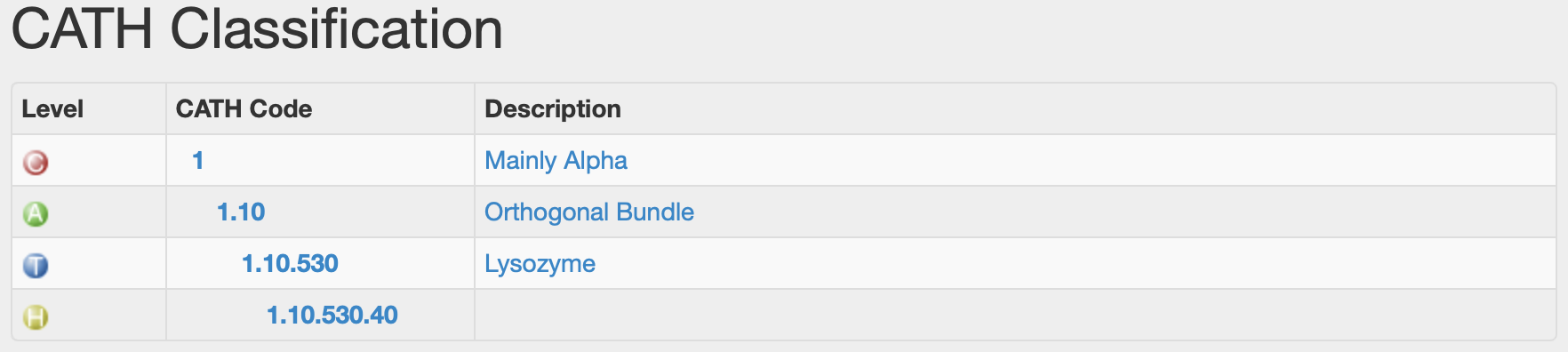 Figura 8. CATH Classification.
Figura 8. CATH Classification.
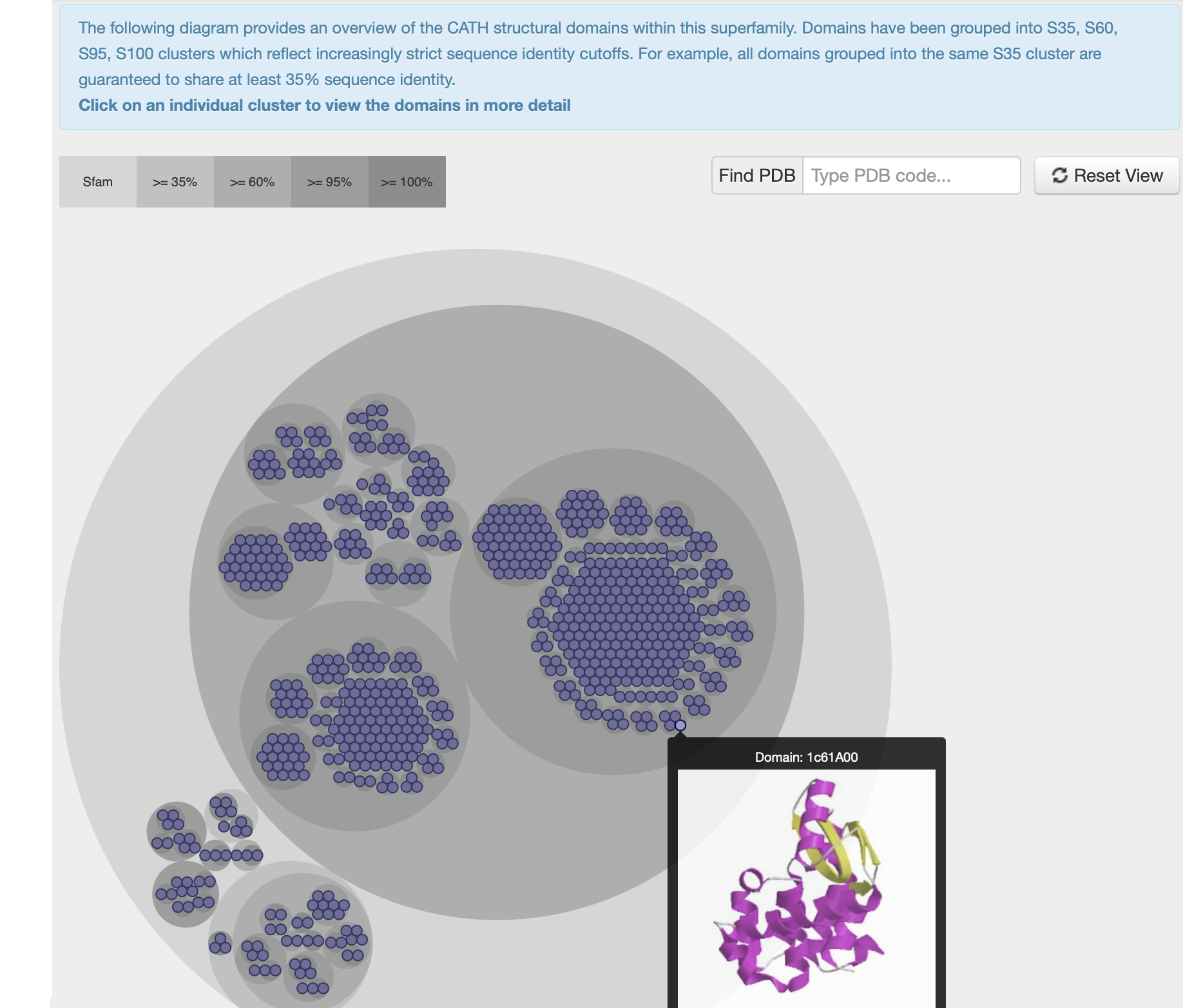 Figura 9. CATH Domains.
Figura 9. CATH Domains.
Centre actiu
Identifiqueu el centre actiu de la proteïna. Quins residus són rellevants, a partir de la literatura? L’estructura que heu explorat, inclou algun substrat o inhibidor? Podeu descriure les interaccions que presenten entre ells els residus del centre actiu i, eventualment, d’aquests amb el possible substrat/inhibidor (ponts d’hidrogen, van der Waals, càrregues, etc)?
El centre actiu correspon al lloc d’unió del lligand situat dins del feix de les 7 hèlixs α. Aquest lloc hidrofòbic que permet la unió de molècules senyalitzadores/inhibidors, característica dels receptors acoblats a proteïna G.
Segons UniProt, residus com Asp113, Ser203, Ser207 i Asn312 són rellevants en la interacció amb el lligand. L’Asp113, participa en interaccions electroestàtiques amb el lligand, mentre que les serines i l’asparagina contribueixen a la formació de ponts d’hidrogen, clau per a l’estabilització del complex. L’estructura analitzada inclou un inhibidor, el carazolol, unit al receptor. Aquest lligand ocupa el lloc d’unió a les hèlixs i interacciona amb els residus del centre actiu.
Les interaccions inclouen ponts d’hidrogen entre el lligand i residus polars així com interaccions electroestàtiques. També es produeixen interaccions de van der Waals entre el lligand i els residus hidrofòbics que recobreixen la cavitat d’unió, contribuint a l’estabilització del complex receptor-lligand.
Funció de la proteïna
Cerqueu informació sobre la funció fa aquesta proteïna. Podeu mostrar el mecanisme detallat que segueix si es tracta d’un enzim? (mireu la figura 6.5.1 d’aquest enllaç per entendre a què ens referim amb el mecanisme de reacció d’un enzim)
La proteïna β2-adrenèrgica (ADRB2) és un receptor de membrana de la família dels receptors acoblats a proteïnes G (GPCR) que s’uneix principalment a catecolamines com l’epinefrina i la norepinefrina. La seva funció principal és transmetre senyals extracel·lulars cap a l’interior de la cèl·lula, regulant diversos processos fisiològics. Quan s’activa, ADRB2 pot acoblar-se a diferents proteïnes G: Via Gs: activa l’adenilat ciclasa, augmenta els nivells de AMPc i activa la PKA → regula processos com la contracció cardíaca i la relaxació del múscul llis (per exemple, broncodilatació). Via Gi: inhibeix l’adenilat ciclasa i activa vies com PI3K/Akt → associada a efectes cardioprotectors i supervivència cel·lular.
En el cor, modula la contractilitat dels cardiomiòcits. En el pulmó, indueix relaxació del múscul llis bronquial (important en tractaments de l’asma). I també pot participar en la regulació del metabolisme i del pH cel·lular.
No és un enzim, per tant no catalitza una reacció, sinó que actua com a receptor i transductor de senyal.
Modificacions post-traduccionals afectadors
Cerqueu informació sobre modificacions post-translacionals que es coneguin que afecten la proteïna o bé proteïnes similars. Identifiqueu els residus que podrien ser-ne diana.
L’ADRB2 (receptor β2-adrenèrgic) està regulat per diverses modificacions post-traduccionals que modulen la seva activitat. La modificació més rellevant és la fosforilació, que té lloc en residus de serina i treonina, principalment a la regió C-terminal. Aquesta fosforilació és mediada per PKA i per quinases específiques de GPCR (GRKs), i afavoreix la unió de β-arrestines, promovent la desensibilització i la internalització del receptor. Entre els residus més destacats es troben Ser262, Ser355 i Ser356 .
Una altra modificació important és la palmitoilació, que consisteix en l’addició d’un àcid gras a residus de cisteïna, com Cys341. Aquesta modificació regula la unió del receptor a la membrana.
També presenta glicosilació en residus d’asparagina situats a l’extrem N-terminal (com Asn6 i Asn15), la qual és essencial per a l’estabilitat, el correcte plegament i l’expressió del receptor a la membrana plasmàtica. Finalment, la ubiquitinació en residus de lisina regula la degradació del receptor i el seu trànsit intracel·lular, contribuint al control dels nivells de receptor a la superfície cel·lular.
Relació seqüència-estructura-funció
Relació seqüència-estructura-funció: Com relacionaríeu l’estructura que heu analitzat amb la funció de la proteïna? Quins elements estructurals participen en aquesta funció? Quins residus en concret són claus per a la funció? Cerqueu eventuals variants de la proteïna que tinguin implicacions funcionals i comenteu els seus efectes a nivell molecular.
Relació entre seqüència, estructura i funció: La funció de la proteïna ADRB2 està directament relacionada amb la seva estructura.La seqüència d’aminoàcids determina que es formi una estructura amb set hèlixs α transmembrana, típiques dels receptors acoblats a proteïnes G (GPCR). Aquestes hèlixs formen una mena de “butxaca” al centre de la proteïna, que és on s’uneixen els lligands. Quan el lligand s’uneix, la proteïna canvia lleugerament de forma, i això permet activar les proteïnes G dins de la cèl·lula.
Elements estructurals implicats: Els principals elements estructurals que participen en la funció són: 7 hèlixs α transmembrana (TM1-TM7): Formen el nucli del receptor i el lloc d’unió del lligand. Regió extracel·lular: Participa en el reconeixement del lligand. Regió intracel·lular: Interacciona amb les proteïnes G per transmetre el senyal. Butxaca central (lloc d’unió): Espai format entre les hèlixs on s’uneix el lligand.
Residus clau per a la funció: Alguns aminoàcids són especialment importants: Asp113 (TM3): Interacciona amb el lligand (interaccions electrostàtiques). És essencial per a la unió. Ser203, Ser204 i Ser207 (TM5): Formen ponts d’hidrogen amb el lligand. Asn312 (TM7): Ajuda a estabilitzar la unió del lligand.
Aquests residus estan situats dins la butxaca d’unió i són clau per activar el receptor.
Variants i efectes funcionals: Hi ha variants (mutacions) en aquesta proteïna que poden afectar la seva funció: Mutacions al lloc d’unió→ poden disminuir l’afinitat pel lligand→ el receptor respon pitjor Mutacions a la regió intracel·lular→ poden afectar la interacció amb proteïnes G→ alteren la transmissió del senyal Mutacions en residus reguladors→ poden afectar processos com la fosforilació→ poden provocar desensibilització o activació anormal
A nivell molecular, aquestes variants poden canviar la forma de la proteïna o les seves interaccions, i això altera la resposta cel·lular (per exemple, la resposta a l’adrenalina).
Bibliografia
-
Bank, R. P. D. (s. f.). RCSB PDB - 5D5A: In meso in situ serial X-ray crystallography structure of the Beta2-adrenergic receptor at 100 K. https://www.rcsb.org/structure/5D5A
-
CATH Superfamily 1.10.530.40. (s. f.). https://www.cathdb.info/version/v4_4_0/superfamily/1.10.530.40/classification
-
Database, A. P. S. (s. f.). AlphaFold Protein Structure Database. https://alphafold.ebi.ac.uk/entry/P07550
-
Green, S. A., Turki, J., Innis, M., & Liggett, S. B. (1994). Amino-Terminal Polymorphisms of the Human .beta.2-Adrenergic Receptor Impart Distinct Agonist-Promoted Regulatory Properties. Biochemistry, 33(32), 9414-9419. https://doi.org/10.1021/bi00198a006
-
Hall, R. A., Premont, R. T., Chow, C., Blitzer, J. T., Pitcher, J. A., Claing, A., Stoffel, R. H., Barak, L. S., Shenolikar, S., Weinman, E. J., Grinstein, S., & Lefkowitz, R. J. (1998). The β2-adrenergic receptor interacts with the Na+/H+-exchanger regulatory factor to control Na+/H+ exchange. Nature, 392(6676), 626-630. https://doi.org/10.1038/33458
-
Site-directed mutagenesis and continuous expression of human beta-adrenergic receptors. Identification of a conserved aspartate residue involved in agonist binding and receptor activation. (1988, 25 marzo). PubMed. https://pubmed.ncbi.nlm.nih.gov/2831218/
- Structural Classification of Proteins—extended (SCOPe). (n.d.). SCOP entry: sunid 310689. Retrieved March 27, 2026, from https://scop.berkeley.edu/sunid=310689
- UniProt. (s. f.). UniProt. https://www.uniprot.org/uniprotkb/P07550/entry
- Xu, X., Kaindl, J., Clark, M. J., Hübner, H., Hirata, K., Sunahara, R. K., Gmeiner, P., Kobilka, B. K., & Liu, X. (2020). Binding pathway determines norepinephrine selectivity for the human β1AR over β2AR. Cell Research, 31(5), 569-579. https://doi.org/10.1038/s41422-020-00424-2