QIEP
Complex 8T5E: constructe d’unió al pèptid BIM
Grup A · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC A | 2025-2026 | seqüència problema
MSGEEERKEKREKVRAGLKRAIAELPAEVAARCLALLDDASDEEFIEAVLEVLEAMREALVAMAREGRLDAVRRATSHIN
EVLVDAAELALEKGREYFRRLCLIVCDMMIELIRLEPEQTPELRRIRERLEEIRRRLEGSG
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 141 aminoàcids. Cisteïnes: 33, 102, 106.
Identificació i estructura de referència
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 8T5E entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 3.0 Å. La longitud de la seqüència analitzada és de 141 aminoàcids. Segons les dades de RCSB/SIFTS, l’entitat 1, Bim_fulldiff, no té un registre UniProt propi perquè és un constructe dissenyat. El mateix PDB, però, sí que enllaça l’entitat 2, el pèptid BIM/BCL2L11, amb UniProt O43521, amb cobertura completa del pèptid dins l’estructura però només parcial respecte de la proteïna BIM completa.
| Camp | Valor |
|---|---|
| UniProt / gen | constructe Bim_fulldiff: sense registre UniProt propi; pèptid associat BIM/BCL2L11: O43521, gen BCL2L11 |
| EC / BRENDA | no assignat |
| Estructura principal | 8T5E entitat 1; difracció de raigs X, 3.0 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
| Dominis i plegament | constructe helicoidal de disseny per reconeixement de pèptids; no hi ha una jerarquia CATH/ECOD natural assignable directament |
| Estructura secundària i lectura ChimeraX | hèlix: 7, regions no assignades: 1; exemples: hèlix 5-23; hèlix 26-39; hèlix 44-67; hèlix 68-81; hèlix 82-94; hèlix 94-114; hèlix 124-138; regions no assignades 1-4, 24-25, 40-43, 115-123, 139-141 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | cisteïnes a [33, 102, 106] |
Funcionalment, el constructe s’interpreta com una proteïna dissenyada per reconèixer un pèptid helicoidal BIM. La lectura biològica s’ha de separar en dues parts: la superfície artificial d’unió del disseny i el paper apoptòtic del pèptid BIM natural. 8T5E correspon al constructe Bim_fulldiff en complex amb un pèptid BIM helicoidal; el mapatge UniProt correspon al pèptid de l’entitat 2, no a la cadena dissenyada de l’entitat 1. La identitat funcional de l’entitat analitzada es formula, per tant, com a reconeixement proteïna-pèptid.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | constructe d’unió al pèptid BIM; nom de l’entitat PDB: Bim_fulldiff |
| Estructura de referència | 8T5E |
| Longitud | 141 aa |
| Trets rellevants | 3 Cys; complex proteïna-pèptid |
Arquitectura molecular
El model mostra un paquet d’hèlixs que genera una superfície complementària per al pèptid BIM. L’element estructural rellevant no és un centre actiu, sinó una interfície: distribució d’hidrofòbics, càrregues de superfície i geometria de contacte.
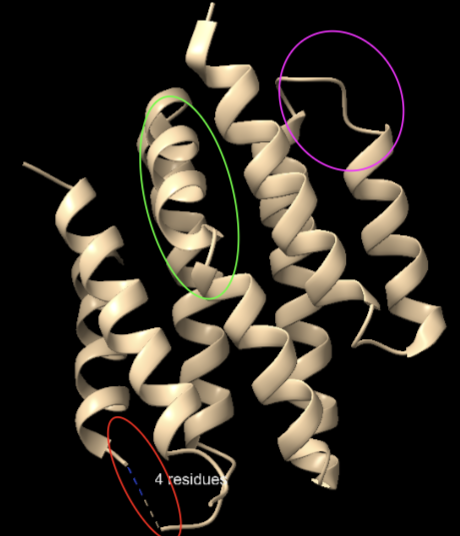
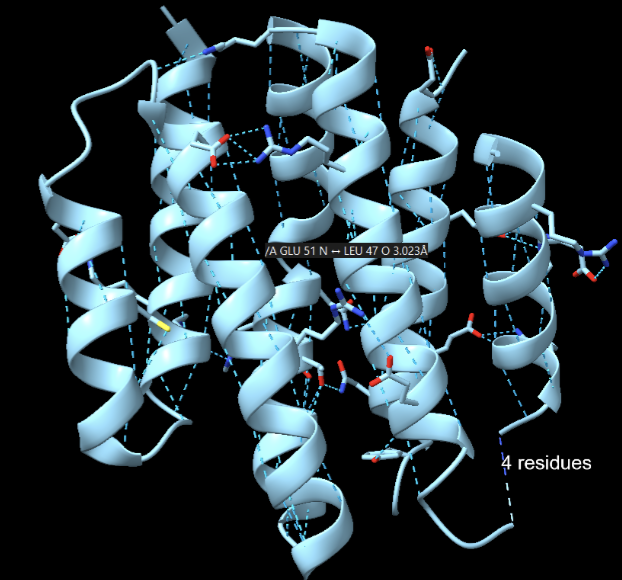
Lloc funcional i mecanisme
La funció molecular directa és la unió al pèptid BIM. Les conseqüències sobre apoptosi pertanyen al context biològic del pèptid natural i no es poden atribuir al constructe sense assaigs funcionals addicionals.
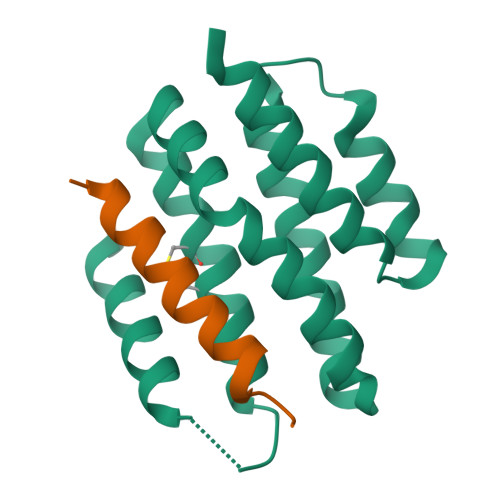
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Vazquez Torres et al., 2024).
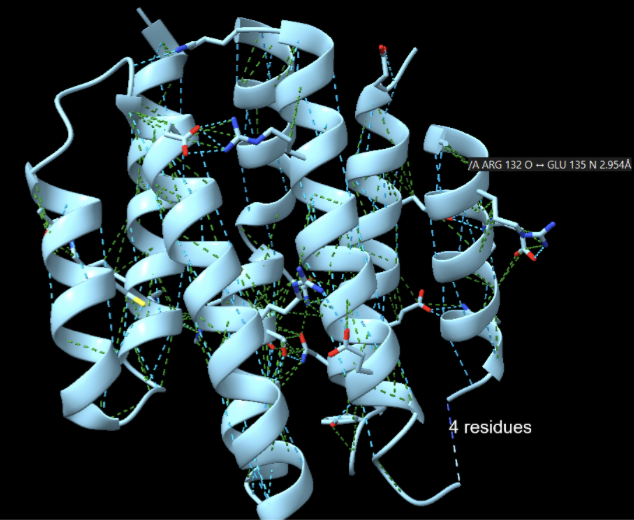
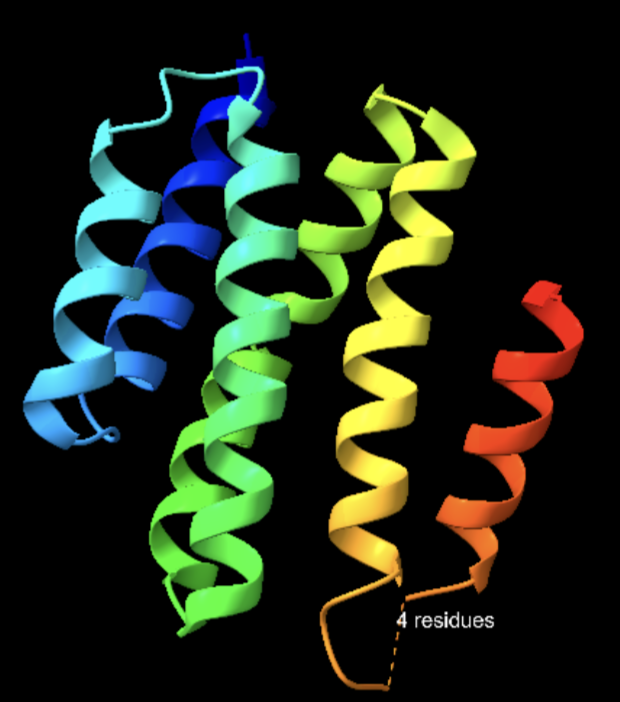
Modificacions i variants
No hi ha un registre UniProt natural directe associat a l’entitat 1 de 8T5E. Les modificacions posttraduccionals i variants de BIM/BCL2L11 anotades a UniProt O43521 descriuen la proteïna natural o el pèptid associat, no el constructe Bim_fulldiff. Només s’han de projectar sobre l’estructura quan es manté separada la numeració del pèptid de la numeració del constructe.
Relació seqüència-estructura-funció
La interpretació seqüència-estructura-funció se centra en separar residus del constructe i residus del pèptid. Els primers defineixen la superfície d’unió; els segons expliquen quins residus de BIM són reconeguts.
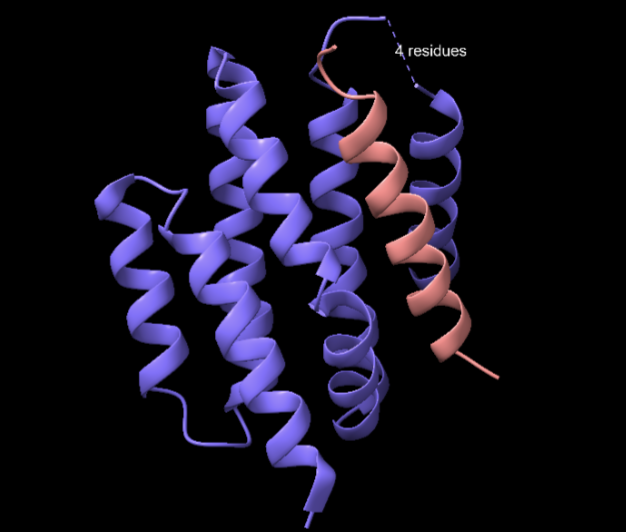
Referències
- Vazquez Torres, S. et al. (2024). De novo design of high-affinity binders of bioactive helical peptides. Nature. doi: 10.1038/s41586-023-06953-1.