QIEP
Proteïna de disseny de novo 8YL8
Grup B · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC B | 2025-2026 | seqüència problema
PDFTGARERFLAGDVTIVLLIAESHDAPYRLANPEDPEADLSDEQLERALAAYLTLVETLFPELYAEMKAALAAAKTPEE
KIAVFREYNARFLAEFDALIDQAFARLKADSLTLKIHLSQGKGSYEIIFPPEVQADPERAAAIEALWKPTLDQLLAVLQE
KHKGKPATTVTYEISAETLRAAVAALARAAEAALRRKVGSLESSGLEVLFQ
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 211 aminoàcids.
Identificació i estructura de referència
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 8YL8 entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 2.21 Å. La longitud de la seqüència analitzada és de 211 aminoàcids. No s’ha trobat cap referència UniProt directa per a la millor entitat PDB; la seqüència s’ha de tractar com a constructe o proteïna de disseny si no hi ha una cerca addicional que en justifiqui una assignació natural.
| Camp | Valor |
|---|---|
| UniProt / gen | cap registre UniProt directe per al constructe; gen: no anotat o no aplicable |
| EC / BRENDA | no assignat |
| Estructura principal | 8YL8 entitat 1; difracció de raigs X, 2.21 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
| Dominis i plegament | proteïna de disseny de novo amb arquitectura principalment helicoidal i elements beta locals; sense família natural CATH/ECOD assignable directament |
| Estructura secundària i lectura ChimeraX | làmina β: 1, hèlix: 11, regions no assignades: 1; exemples: làmina β 124-128, 111-118, 168-175; hèlix 5-13; hèlix 16-25; hèlix 36-40; hèlix 42-61; hèlix 61-75; hèlix 77-108; hèlix 130-135 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | No s’ha detectat cap etiqueta de purificació, residu ambigu o alerta específica de cisteïnes a partir de la seqüència sola. |
Funcionalment, és una proteïna de disseny de novo. No té gen natural ni número EC; la interpretació s’ha de basar en l’arquitectura, l’estabilitat del plegament i la publicació estructural associada. La seqüència assignada coincideix completament amb l’entitat experimental 8YL8. No hi ha entrada UniProt natural ni classificació EC associada, de manera que la proteïna s’interpreta com un constructe de disseny i no com un homòleg funcional anotat.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | Proteïna de disseny de novo |
| Estructura de referència | 8YL8 |
| Longitud | 211 aa |
| Trets rellevants | sense Cys; sense EC assignat |
Arquitectura molecular
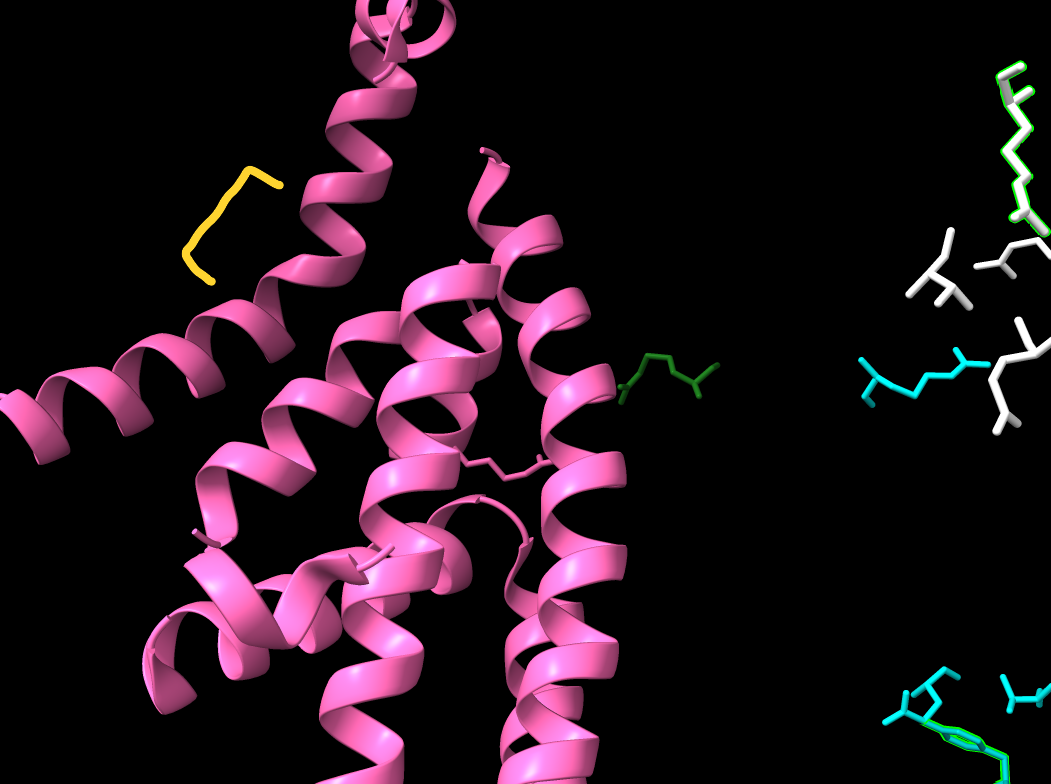
L’estructura combina un nucli principalment helicoidal amb elements beta locals. La lectura estructural es basa en l’empaquetament del nucli, la distribució de residus polars a superfície i les possibles interfícies oligomèriques.

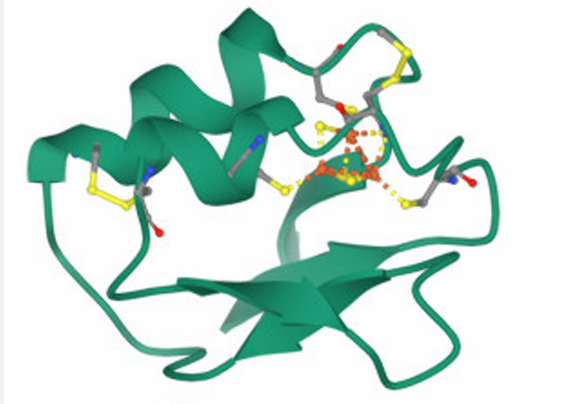
Lloc funcional i mecanisme
No es proposa una funció natural. La informació funcional disponible és estructural: estabilitat del plegament, geometria de superfície i eventual capacitat d’oligomerització o interacció derivada del disseny.
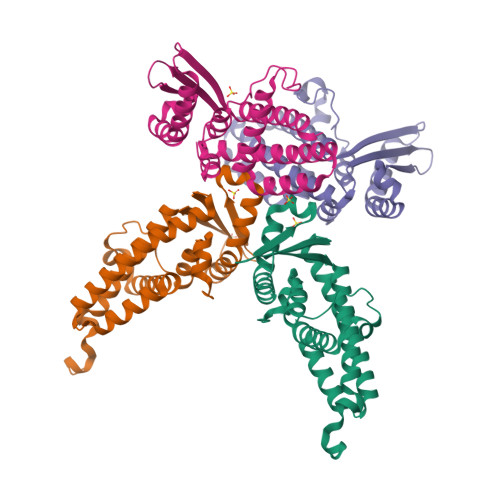
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Frank et al., 2024).
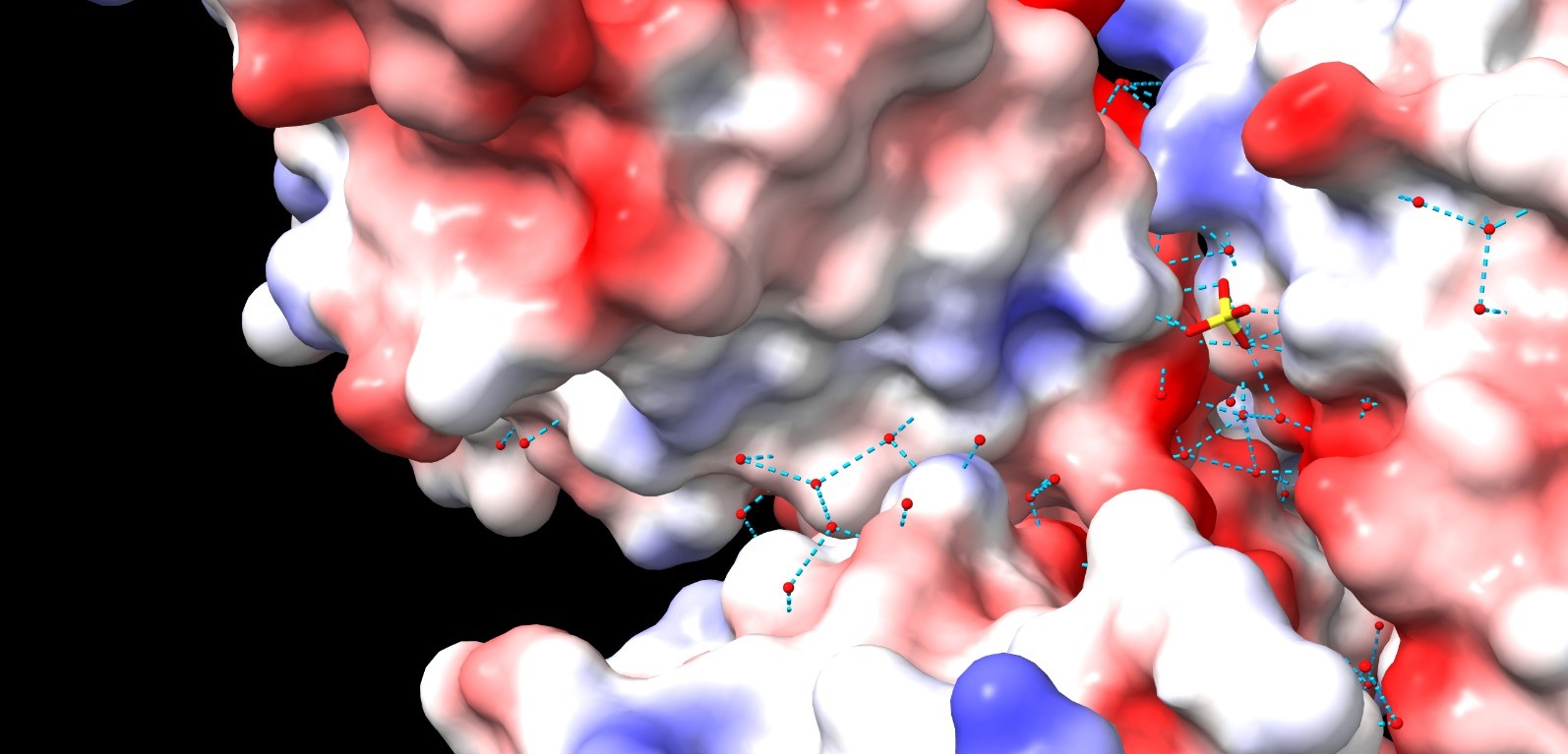

Modificacions i variants
No hi ha un registre UniProt natural directe associat a la millor entitat PDB. En aquest cas no és correcte importar modificacions posttraduccionals o variants d’una proteïna natural sense un alineament explícit; les variants rellevants són les pròpies del disseny, de la interfície o del centre funcional definit a la publicació estructural.
Relació seqüència-estructura-funció
En una proteïna de novo, la relació seqüència-estructura-funció és sobretot una relació seqüència-plegament. Les posicions hidrofòbiques sostenen el nucli; les posicions polars i carregades determinen solubilitat i reconeixement superficial.
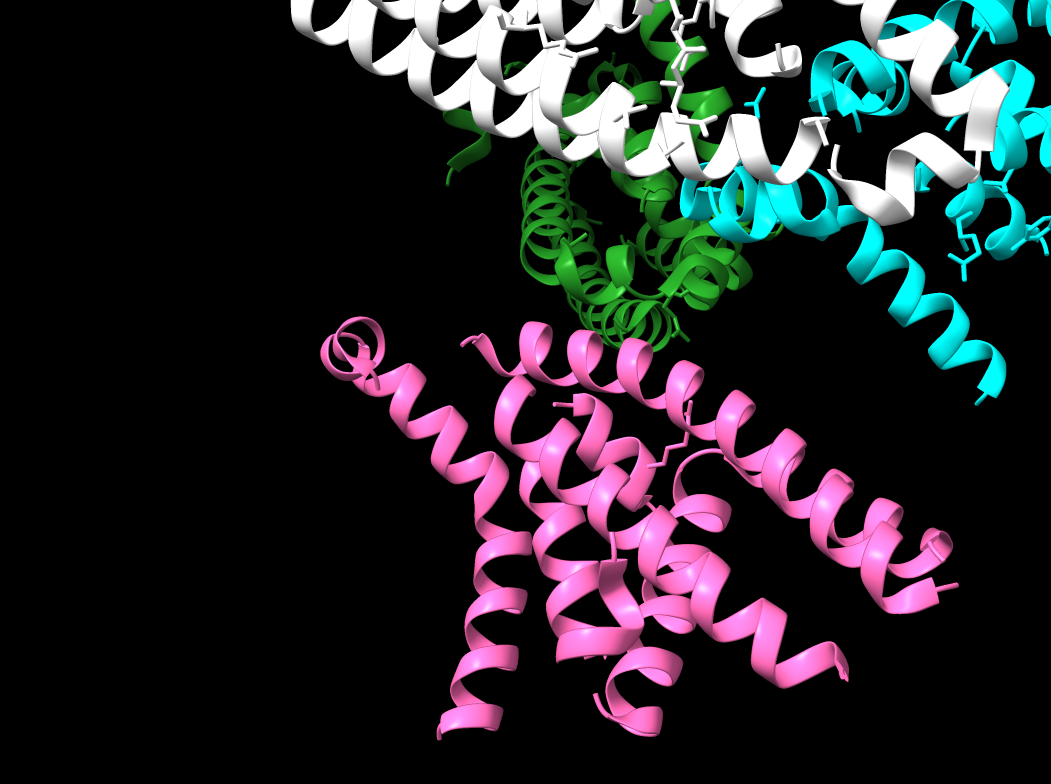




Referències
- Frank, C. et al. (2024). Scalable protein design using optimization in a relaxed sequence space. Science. doi: 10.1126/science.adq1741.