QIEP
D_3_212: proteïna simètrica de disseny
Grup C · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC C | 2025-2026 | seqüència problema
SGSGSTEEEEALLRWFQTLLAKFDELVKQLGDPRLLEEARRLQERLEEAKKRGDKRTIKQLAALLQMFVLIAQIFQLVEE
LGDPKLLEQAKRLLERLKEAVERGDEETIKELLDLAHMTYLIAQIFQLVEQLGDPRLLELAKELLKRLKEAQERGDRRTI
ERLLRLVQMTYLIAQIFQLVRQLGDPRLLETAKTLLTLLKLAFEEGDELLIKSLLTLVAETYRQAAAEQ
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 229 aminoàcids.
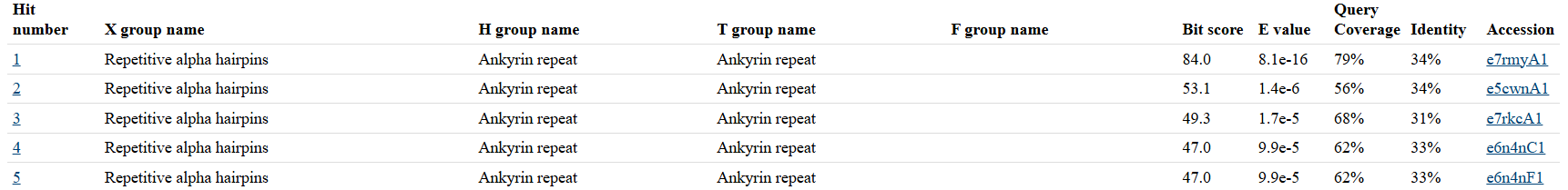
Identificació i estructura de referència
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 7RMX entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 1.65 Å. La longitud de la seqüència analitzada és de 229 aminoàcids. No s’ha trobat cap referència UniProt directa per a la millor entitat PDB; la seqüència s’ha de tractar com a constructe o proteïna de disseny si no hi ha una cerca addicional que en justifiqui una assignació natural.
| Camp | Valor |
|---|---|
| UniProt / gen | cap registre UniProt directe per al constructe; gen: no anotat o no aplicable |
| EC / BRENDA | no assignat |
| Estructura principal | 7RMX entitat 1; difracció de raigs X, 1.65 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
| Dominis i plegament | constructe helicoidal simètric D3 amb cavitat central; l’anotació automàtica ECOD no substitueix la descripció de disseny |
| Estructura secundària i lectura ChimeraX | hèlix: 9, regions no assignades: 1; exemples: hèlix 6-31; hèlix 32-53; hèlix 54-82; hèlix 83-104; hèlix 105-133; hèlix 134-155; hèlix 156-184; hèlix 185-205 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | No s’ha detectat cap etiqueta de purificació, residu ambigu o alerta específica de cisteïnes a partir de la seqüència sola. |
Funcionalment, D_3_212 és un constructe simètric de disseny. El punt central és la geometria de la cavitat i de la simetria D3, no una funció enzimàtica natural. 7RMX cobreix tota la seqüència assignada. D_3_212 és una proteïna de disseny simètrica; no s’interpreta com una proteïna de Golgi ni com una proteïna natural amb funció cel·lular anotada.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | D_3_212 |
| Estructura de referència | 7RMX |
| Longitud | 229 aa |
| Trets rellevants | constructe helicoidal; simetria D3 |
Arquitectura molecular
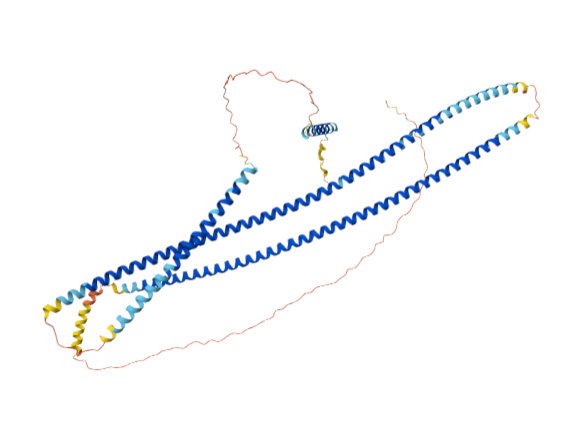
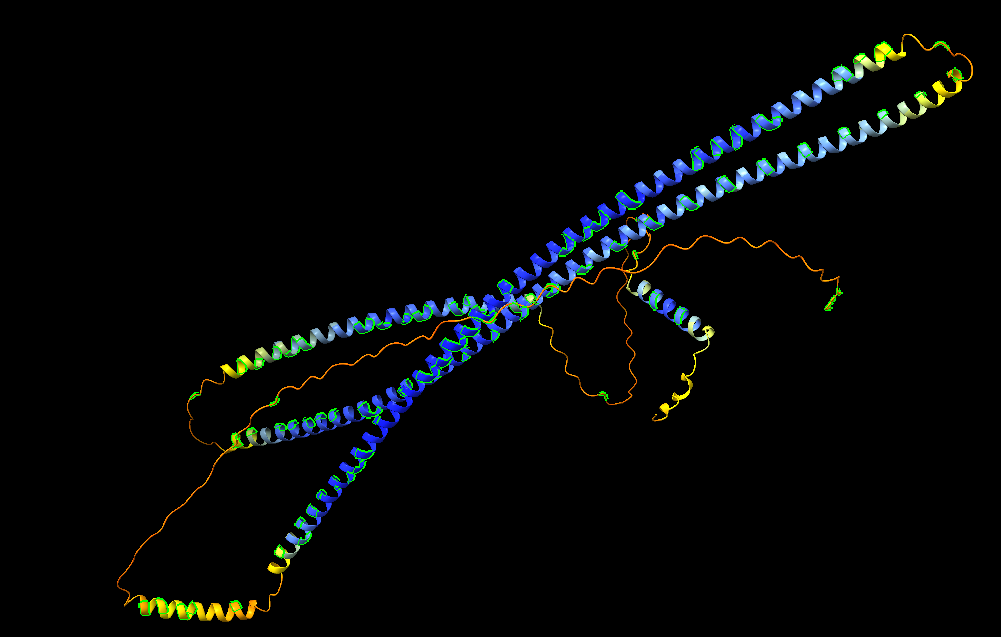
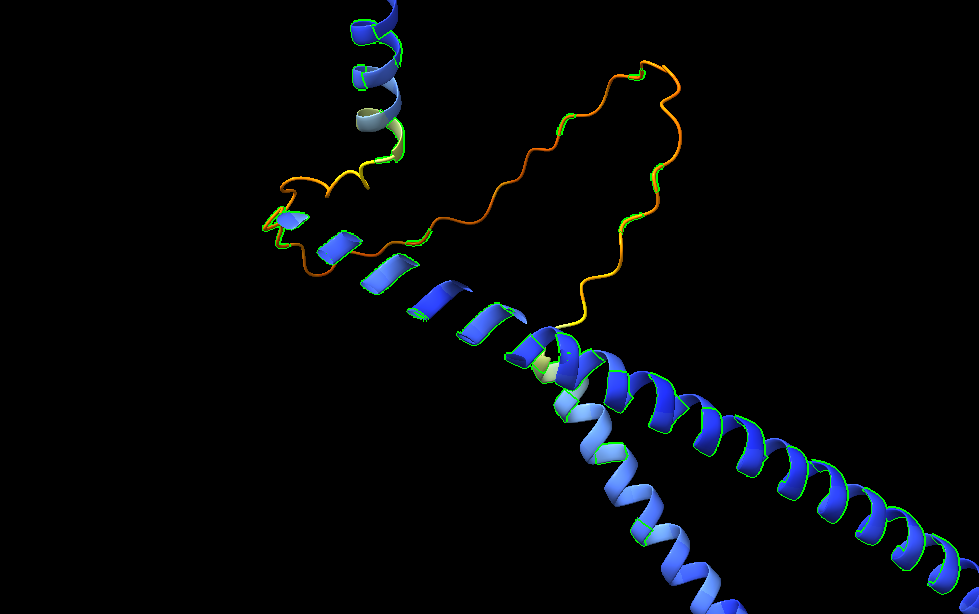
El plegament és helicoidal i organitzat per simetria D3. La repetició d’elements helicoidals crea interfícies regulars que estabilitzen el conjunt i fan del sistema un exemple clar de disseny per simetria.

Lloc funcional i mecanisme
La funció experimental principal és arquitectònica: generar un objecte molecular estable i simètric. Qualsevol funció cel·lular queda fora de la interpretació si no hi ha evidència independent.
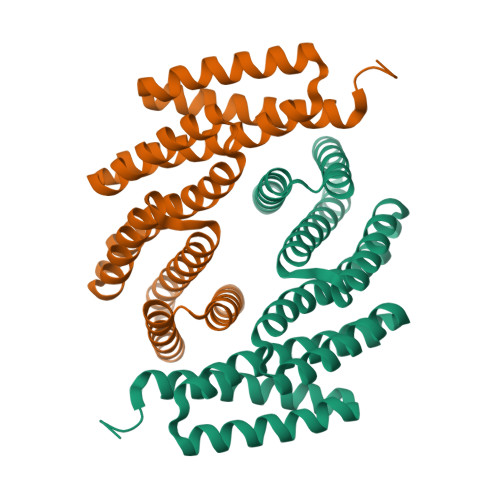
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Hicks et al., 2022).
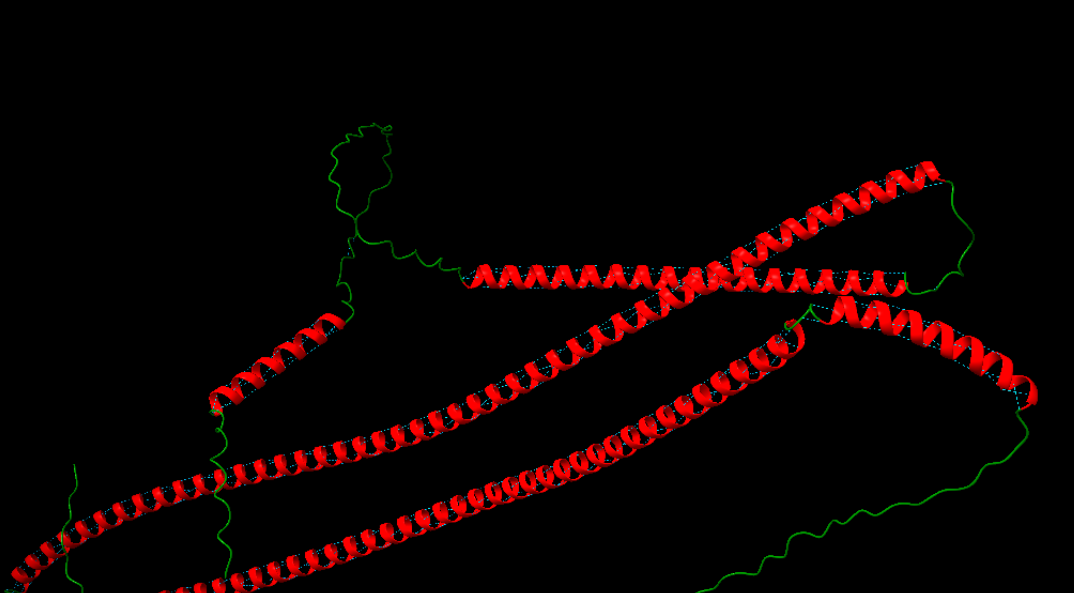
Modificacions i variants
No hi ha un registre UniProt natural directe associat a la millor entitat PDB. En aquest cas no és correcte importar modificacions posttraduccionals o variants d’una proteïna natural sense un alineament explícit; les variants rellevants són les pròpies del disseny, de la interfície o del centre funcional definit a la publicació estructural.
Relació seqüència-estructura-funció
Els residus que apunten cap al nucli i cap a les interfícies simètriques expliquen la forma global. La seqüència es llegeix com un patró d’empaquetament repetitiu que dona lloc a l’arquitectura D3.
Referències
- Hicks, D. R. et al. (2022). De novo design of protein homodimers containing tunable symmetric protein pockets. PNAS. doi: 10.1073/pnas.2113400119.