QIEP
DYNA_1b7 en complex amb dinorfina A
Grup D · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC D | 2025-2026 | seqüència problema
MSGKEEEIEKEFEEKKKIIEENLKEAEEEGEEEAAEKLKEALKKLEEAIKLHREGANPVEVELEEVTAIILNNLAVLLRE
GEEELAKELEKAIKLLEEKKDAPEEERLKAIAIAIIRSVLVLIKWEGGKDEETIEEIEEILENRENLSLEELREAYVRAE
IAYLIESGIDPEAAKKVREKYERGAPLEELLKDIEKIEKEAKKREEEKKGSHHHHHH
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 217 aminoàcids.
Identificació i estructura de referència
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 9CCE entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 3.15 Å. La longitud de la seqüència analitzada és de 217 aminoàcids. Segons RCSB/SIFTS, l’entitat 1, DYNA_1b7, no té un registre UniProt propi; l’entitat 2 del mateix PDB correspon al pèptid dinorfina A i mapeja a UniProt P01213, proencefalina-B/prodinorfina, gen PDYN.
| Camp | Valor |
|---|---|
| UniProt / gen | constructe DYNA_1b7: sense registre UniProt propi; pèptid dinorfina A associat: P01213, gen PDYN |
| EC / BRENDA | no assignat |
| Estructura principal | 9CCE entitat 1; difracció de raigs X, 3.15 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
| Dominis i plegament | feix helicoidal dissenyat per reconeixement de regió desordenada/dinorfina; sense jerarquia natural CATH/ECOD directa |
| Estructura secundària i lectura ChimeraX | hèlix: 9, regions no assignades: 1; exemples: hèlix 6-29; hèlix 31-55; hèlix 57-80; hèlix 82-98; hèlix 103-126; hèlix 131-143; hèlix 148-167; hèlix 172-183 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | etiqueta d’histidines 212-217 (HHHHHH) |
Funcionalment, DYNA_1b7 és un constructe d’unió a dinorfina A. La prodinorfina/PDYN aporta el context biològic del pèptid, però la funció del model estructural és el reconeixement proteïna-pèptid. 9CCE entitat 1 cobreix tota la seqüència assignada i correspon a DYNA_1b7; el mapatge UniProt P01213 correspon al pèptid associat de l’entitat 2 i no a la identitat del constructe dissenyat.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | DYNA_1b7 |
| Estructura de referència | 9CCE |
| Longitud | 217 aa |
| Trets rellevants | His 212-217; complex amb pèptid dinorfina |
Arquitectura molecular
L’estructura és un conjunt helicoidal que presenta una superfície d’unió per a dinorfina A. La interpretació separa cadenes del constructe, cadenes del pèptid i etiqueta d’histidines terminal.
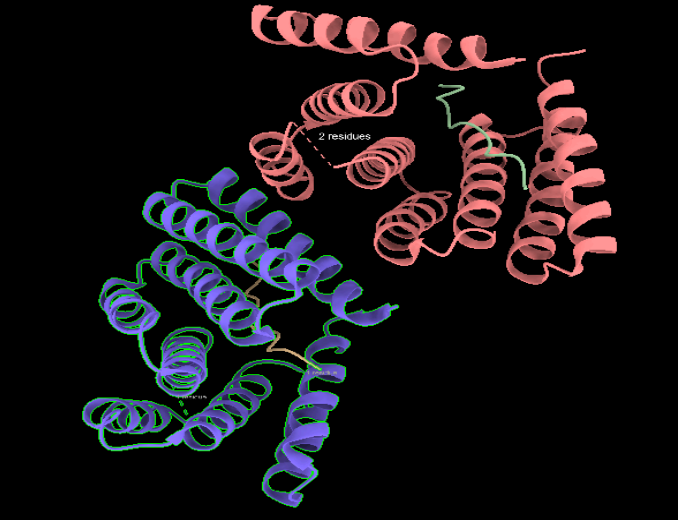
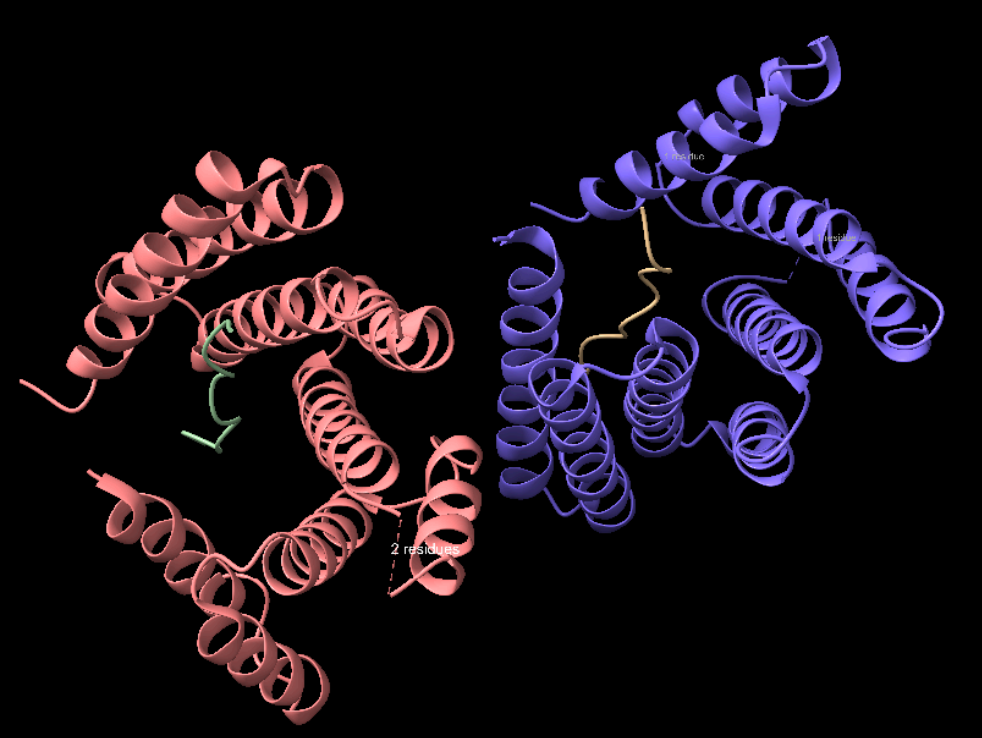
Lloc funcional i mecanisme
La funció molecular és el reconeixement del pèptid. No es tracta d’un enzim ni d’un precursor opioide; és un sistema de disseny per estudiar interaccions proteïna-pèptid amb geometria definida.

La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Wu et al., 2025).
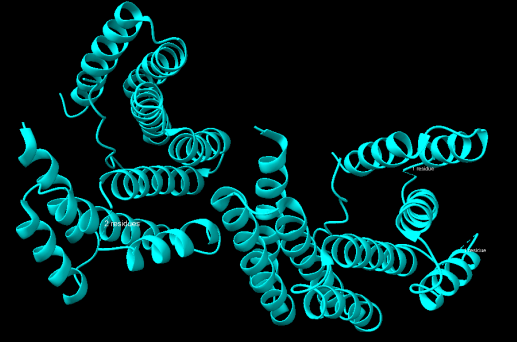
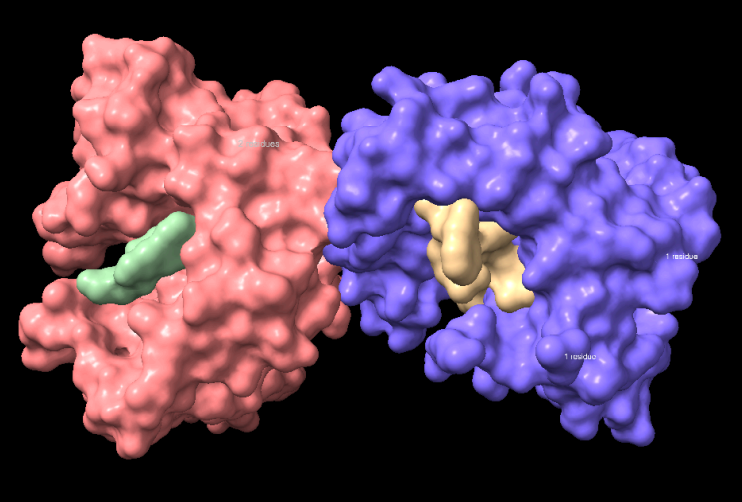
Modificacions i variants
La seqüència assignada és un constructe de reconeixement de dinorfina A i no la prodinorfina humana completa. Les variants de PDYN i les modificacions del precursor només tenen sentit com a context del pèptid natural; no s’han de traslladar al constructe sense separar entitat, cadena i numeració. L’etiqueta d’histidines terminal forma part del constructe experimental.
Relació seqüència-estructura-funció
Els residus d’interfície del constructe expliquen la complementarietat amb la dinorfina A. La numeració del pèptid i la numeració del constructe s’han de mantenir separades per evitar atribucions funcionals incorrectes.
Referències
- Wu, K. et al. (2025). Design of intrinsically disordered region binding proteins. Science. doi: 10.1126/science.adr8063.