QIEP
RA95.5-8F: retro-aldolasa dissenyada
Grup F · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC F | 2025-2026 | seqüència problema
MPRYLKGWLEDVVQLSLRRPSVHASRQRPIISLNERILEFNKRNITAIIAYYLRKSPSGLDVERDPIEYAKYMEPYAVGL
SIKTEEKYFDGSYEMLRKIASSVSIPILMNDFIVKESQIDDAYNLGADTVLLIVEILTERELESLLEYARGYGMEPLILI
NDENDLDIALRIGARFITIYSMNFETGEINKENQRKLISMIPSNVVKVPLLDFFEPNEIEELRKLGVNAFMISSSLMRNP
EKIKELIEGSLEHHHHHH
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 258 aminoàcids.
Identificació i estructura de referència
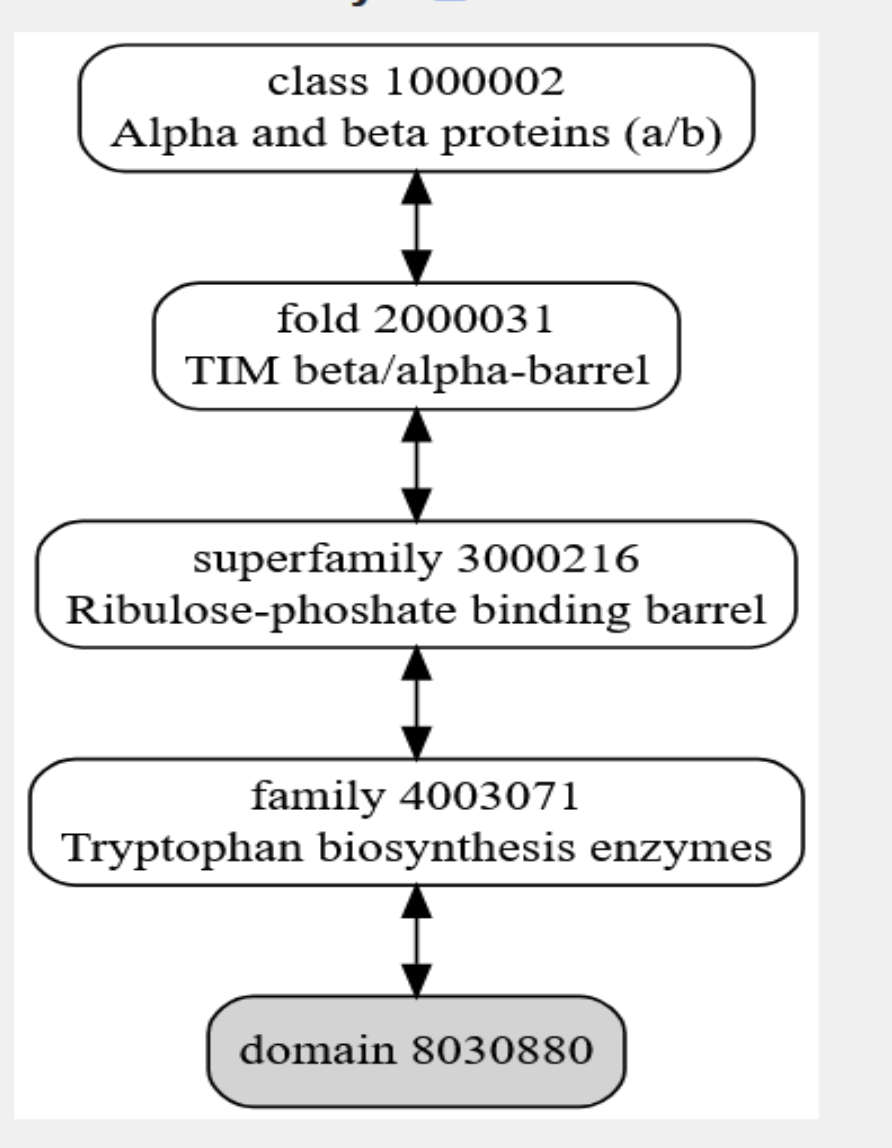
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 5AN7 entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 1.1 Å. La longitud de la seqüència analitzada és de 258 aminoàcids. Registre UniProt candidat Q06121 (indole-3-glicerol fosfat sintasa), vinculat a l’entitat PDB recomanada. Gen: trpC.
| Camp | Valor |
|---|---|
| UniProt / gen | Q06121; gen: trpC |
| EC / BRENDA | 4.1.1.48. Consulteu BRENDA a partir del número EC indicat. |
| Estructura principal | 5AN7 entitat 1; difracció de raigs X, 1.1 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
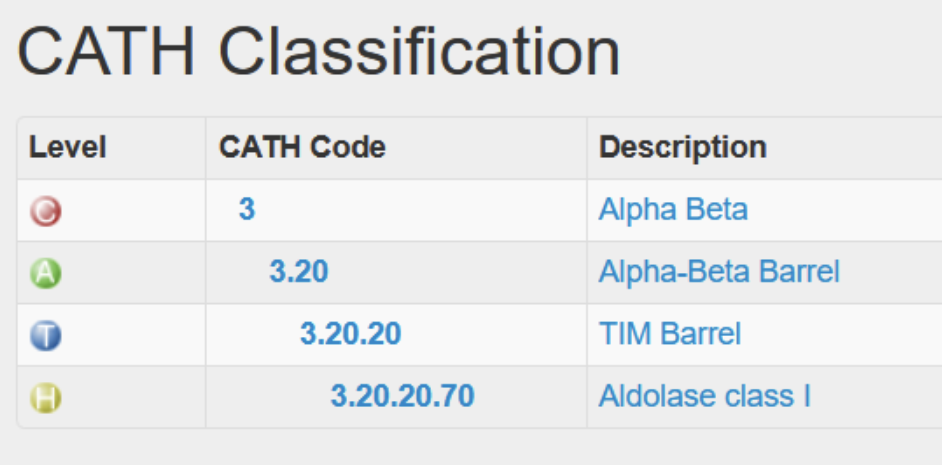
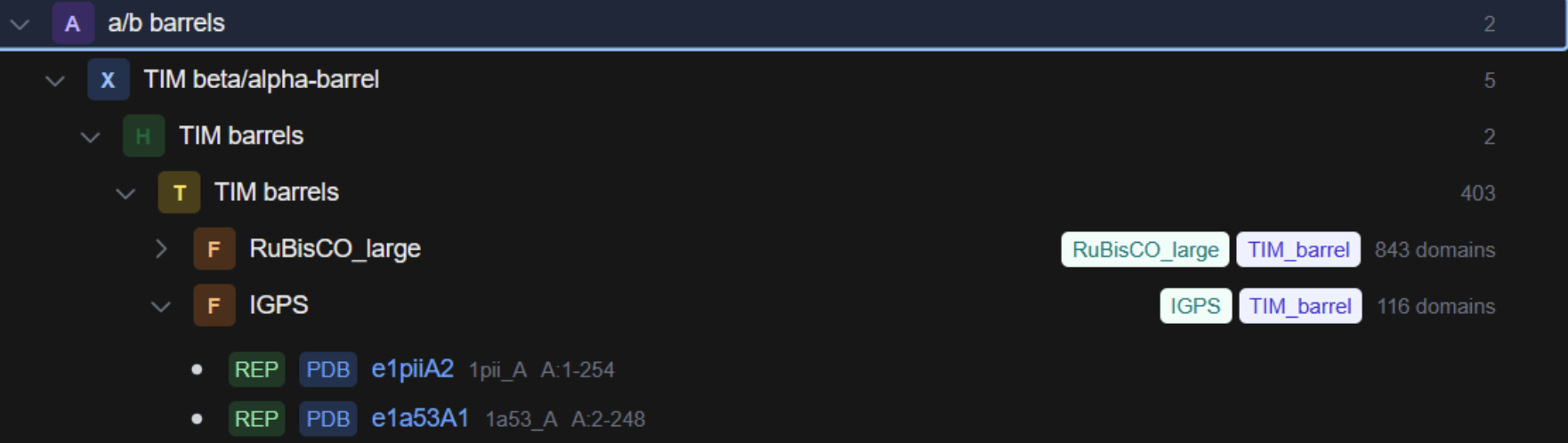
| Dominis i plegament | bastida de barril TIM/aldolasa de classe I, CATH 3.20.20.70, remodelada per activitat retro-aldolasa |
| Estructura secundària i lectura ChimeraX | làmina β: 1, hèlix: 12, regions no assignades: 1; exemples: làmina β 48-52, 230-232, 206-211, 176-179, 157-160, 129-133, 107-110, 79-83, 48-52; hèlix 6-18; hèlix 32-44; hèlix 65-74; hèlix 92-101; hèlix 115-126; hèlix 135-137; hèlix 138-152 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | etiqueta d’histidines 253-258 (HHHHHH) |
Funcionalment, RA95.5-8F és una retro-aldolasa dissenyada sobre una bastida d’indole-3-glicerol fosfat sintasa. La funció natural IGPS/trpC i l’EC 4.1.1.48 són context de la bastida, no la funció principal del constructe evolucionat. 5AN7 és la coincidència exacta de la seqüència assignada. El context IGPS/trpC descriu la bastida evolutiva, però la identitat del constructe és una retro-aldolasa dissenyada.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | RA95.5-8F |
| Estructura de referència | 5AN7 |
| Longitud | 258 aa |
| Trets rellevants | His 253-258; barril TIM |
Arquitectura molecular
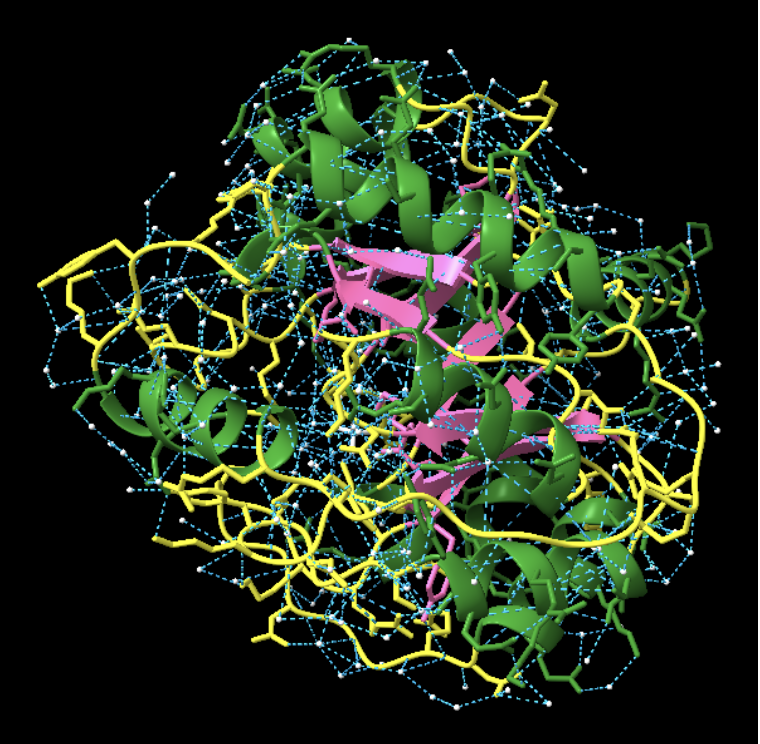
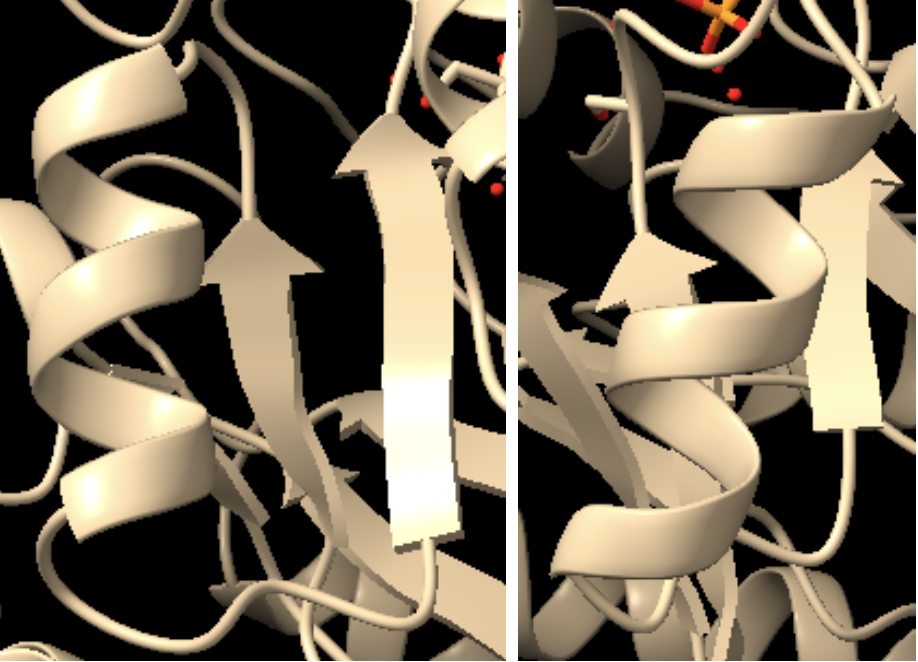
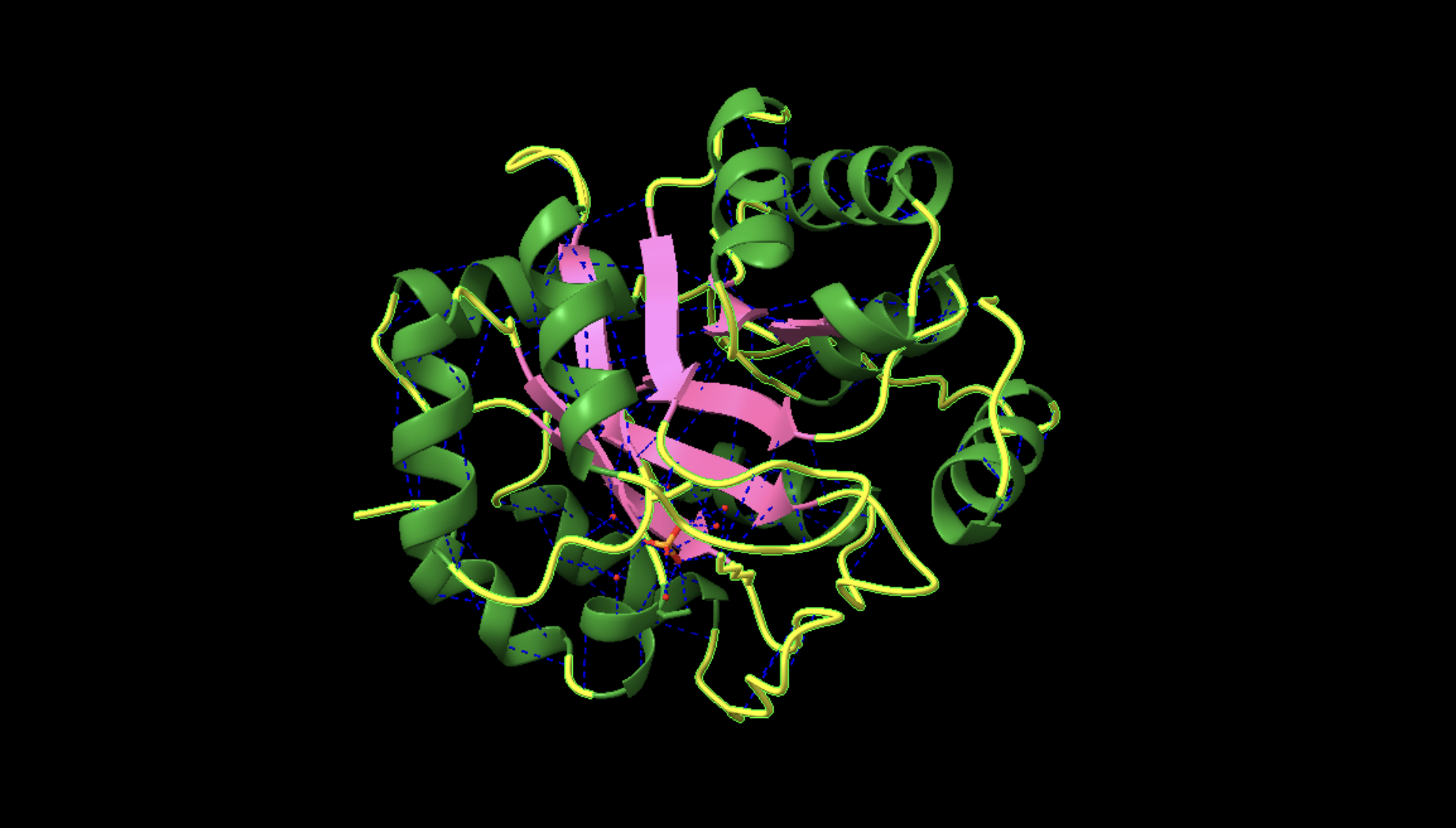
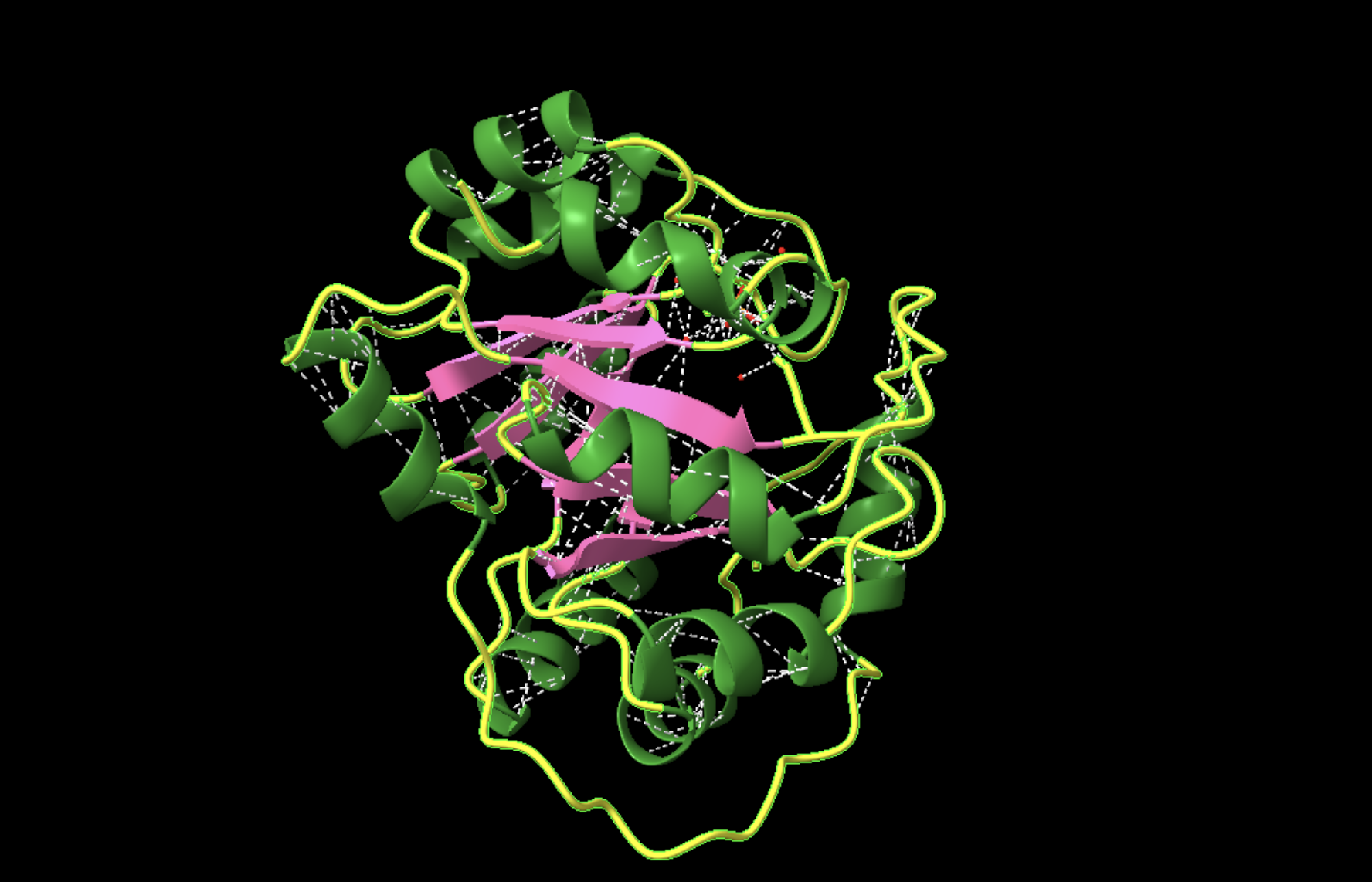
La proteïna adopta un barril TIM, amb làmines β internes i hèlixs externes. Aquesta arquitectura és compatible amb cavitats catalítiques profundes i apareix repetidament en disseny d’enzims.
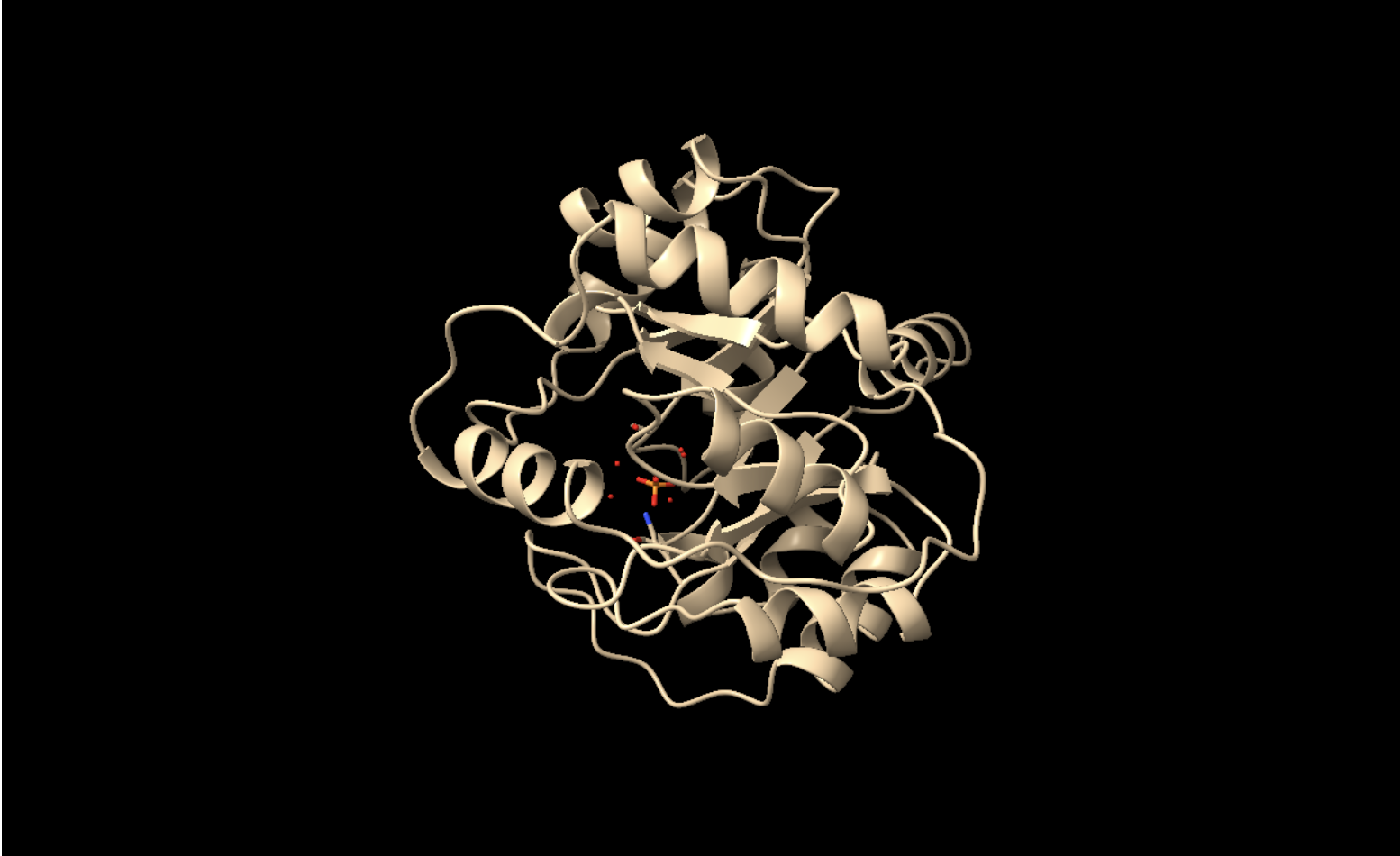
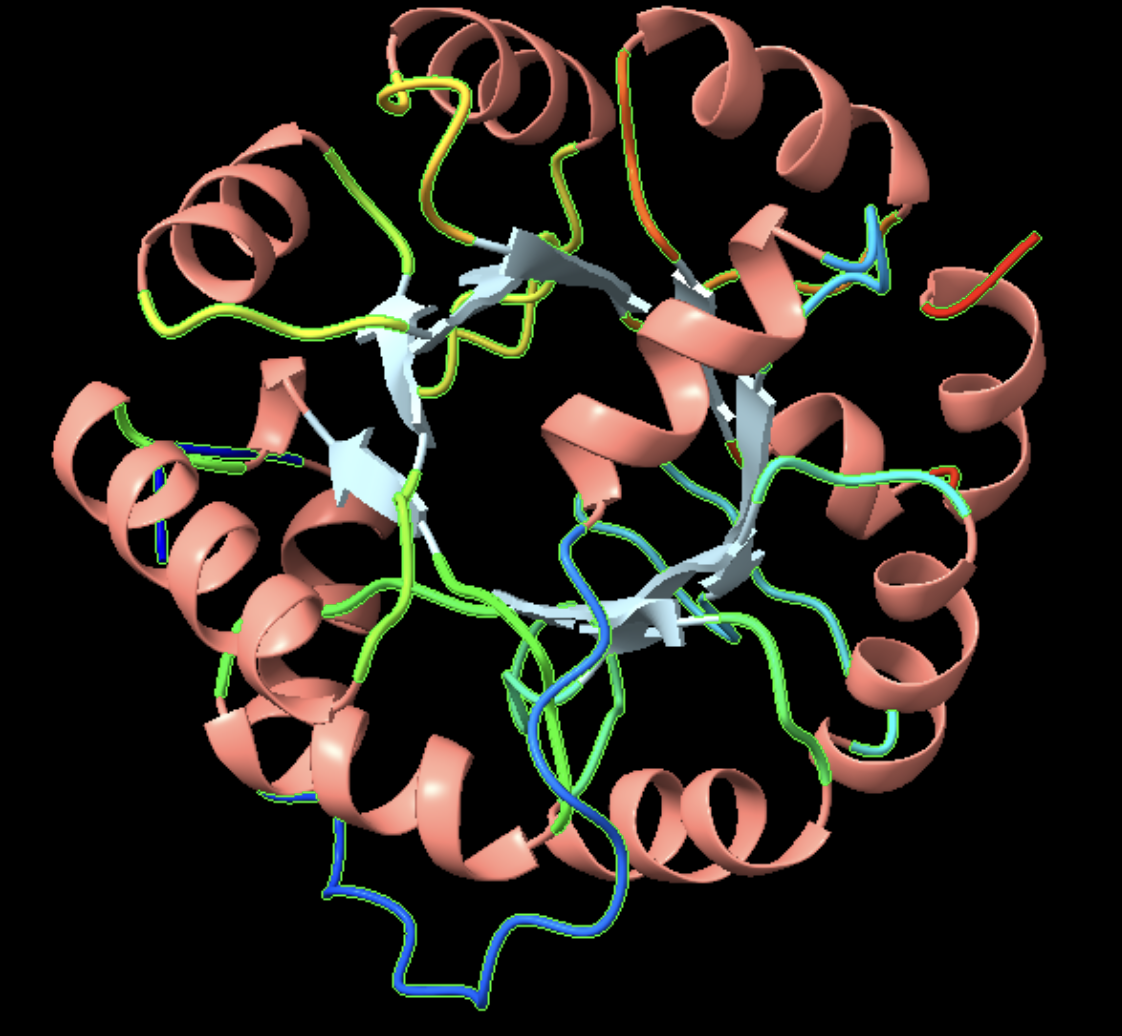
Lloc funcional i mecanisme
La funció rellevant és la reacció retro-aldòlica dissenyada. La cavitat catalítica no s’ha d’interpretar com a centre actiu d’IGPS, sinó com una reprogramació química sobre una bastida TIM.
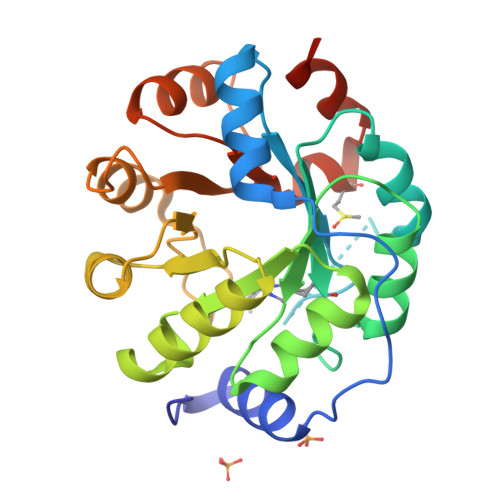
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Obexer et al., 2017).
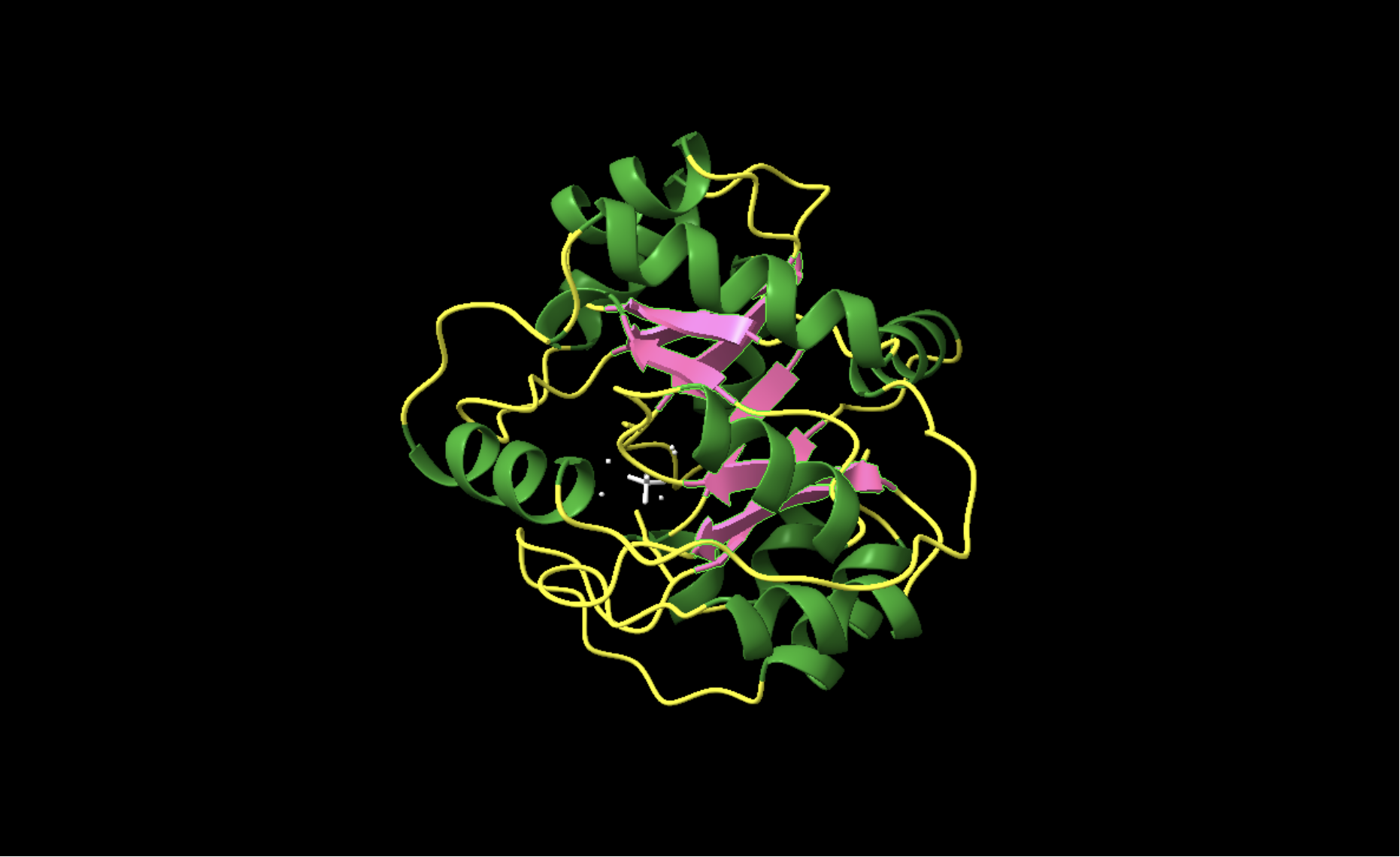
Modificacions i variants
RA95.5-8F és un constructe evolucionat; no s’hi han d’importar variants o modificacions posttraduccionals de la IGPS natural sense alineament. Les mutacions rellevants són les que remodelen la cavitat retro-aldolasa i cal discutir-les segons la numeració del PDB 5AN7.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció requereix separar residus conservats de la bastida, mutacions de disseny i residus directament implicats en la cavitat catalítica.
Referències
- Obexer, R. et al. (2017). Emergence of a catalytic tetrad during evolution of a highly active artificial aldolase. Nature Chemistry. doi: 10.1038/nchem.2596.