QIEP
Domini hemo del citocrom P450 BM3
Grup K · Química i Enginyeria de Proteïnes 2025-2026
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>JC K | 2025-2026 | seqüència problema
MTIKEMPQPKTFGELKNLPLLNTDKPVQALMKIADELGEIFKFEAPGRVTRYISSQRLVKEACDESRFDKNLSQARKFVR
DFAGDGLATSWTHEKNWKKARNILLPRLSQQAMKGYHAMMVDIAVQLVQKWERLNSDEHIEVPEDMTRLTLDTIGLCGFN
YRINSFYRDQPHPFITSMVRALDEVMNKLQRANPDDPAYDENKRQFQEDIKVMNDLVDKIIADRKASGEQSDDLLTHMLH
GKDPETGEPLDDENIRYQIITFLIAGHETTSGLLTFALYFLVKNPHVLQKAAEEAARVLVDPVPSYKQVKQLKYVGMVLN
EALRIWPTAPAFSLYAKEDTMLGGEYPLEKGDELMVLIPQLHRDKTVWGDDVEEFRPERFENPSAIPQHAFKPFGNGQRA
CIGQQFALHEATLVLGMMLKHFDFEDHTNYELDIEETLTLKPKGFVIKAKSKKIPLGGIPSPSTLEHHHHHH
Seqüència extreta del fitxer FASTA oficial de selecció 2025-2026. Longitud: 472 aminoàcids. Cisteïnes: 63, 157, 401.
Identificació i estructura de referència
La seqüència anterior defineix la molècula analitzada i evita confondre el nom abreujat del sistema amb una proteïna natural completa. La cerca a RCSB PDB proporciona com a estructura de referència 3QI8 entitat 1, amb cobertura de la seqüència 100.0%, identitat 100.0% i resolució 3.2 Å. La longitud de la seqüència analitzada és de 472 aminoàcids. 3QI8 no exposa un mapatge UniProt directe per a aquesta entitat a RCSB/SIFTS, però estructures molt properes del domini hemo de BM3 mapen a UniProt P14779, citocrom P450/NADPH–P450 reductasa bifuncional, gen cyp102A1.
| Camp | Valor |
|---|---|
| UniProt / gen | context de BM3: P14779, gen cyp102A1; 3QI8 entitat 1 sense mapatge SIFTS directe |
| EC / BRENDA | no assignat |
| Estructura principal | 3QI8 entitat 1; difracció de raigs X, 3.2 Å |
| Cobertura i identitat | 100.0% de cobertura; 100.0% d’identitat |
| Dominis i plegament | domini hemo de citocrom P450, CATH 1.10.630.10; variant evolucionada del domini P450 de BM3 |
| Estructura secundària i lectura ChimeraX | làmina β: 4, hèlix: 22, regions no assignades: 1; exemples: làmina β 42-45, 48-53, 353-357, 331-336, 68-70; làmina β 140-141, 446-451, 422-425; làmina β 340-342, 346-348; làmina β 434-436, 440-442; hèlix 12-16; hèlix 17-22; hèlix 25-37; hèlix 55-63 |
| Lligands o cofactors a revisar | No s’han identificat lligands no polimèrics en aquesta entrada PDB; els pèptids, cadenes associades o socis polimèrics s’han de revisar per separat. |
| Trets de constructe | etiqueta d’histidines 467-472 (HHHHHH); cisteïnes a [63, 157, 401] |
Funcionalment, és una variant del domini hemo de P450 BM3. La funció natural és la monooxigenació d’àcids grassos amb activació d’oxigen al ferro-hemo; les mutacions de variants evolucionades modulen accés de substrat, estat electrònic i acoblament catalític. 3QI8 és la coincidència exacta de la seqüència assignada. 2IJ2 és una estructura propera i d’alta resolució que pot aportar detall atòmic si es manté el remapeig amb la seqüència.
| Paràmetre | Valor |
|---|---|
| Proteïna o constructe | P450 BM3 hemo |
| Estructura de referència | 3QI8 / 2IJ2 |
| Longitud | 472 aa |
| Trets rellevants | His 467-472; citocrom P450 |
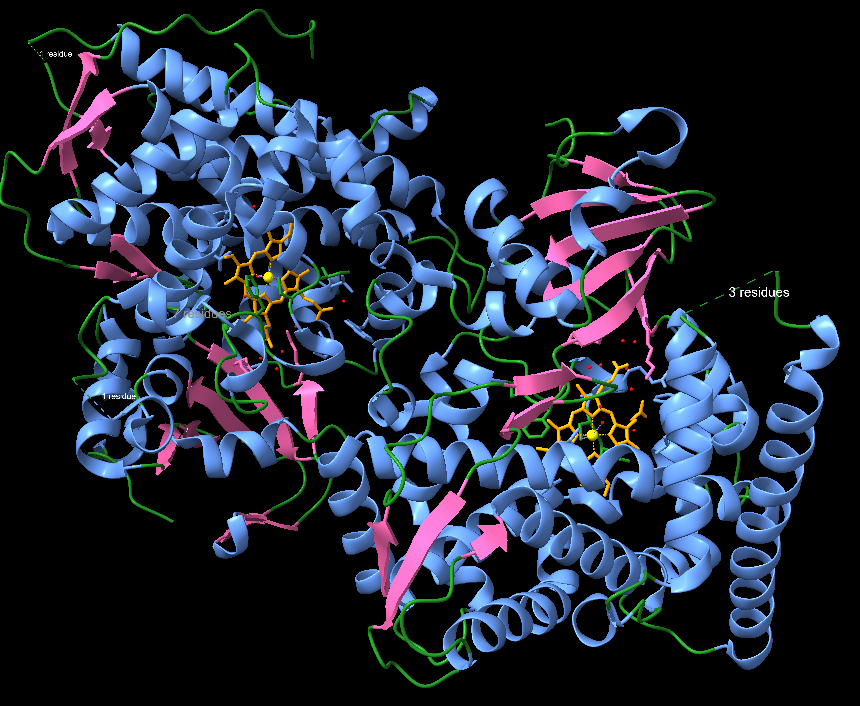
Arquitectura molecular
El domini hemo de BM3 presenta el plegament P450, amb hèlixs que envolten el grup hemo i defineixen canals d’accés al substrat.
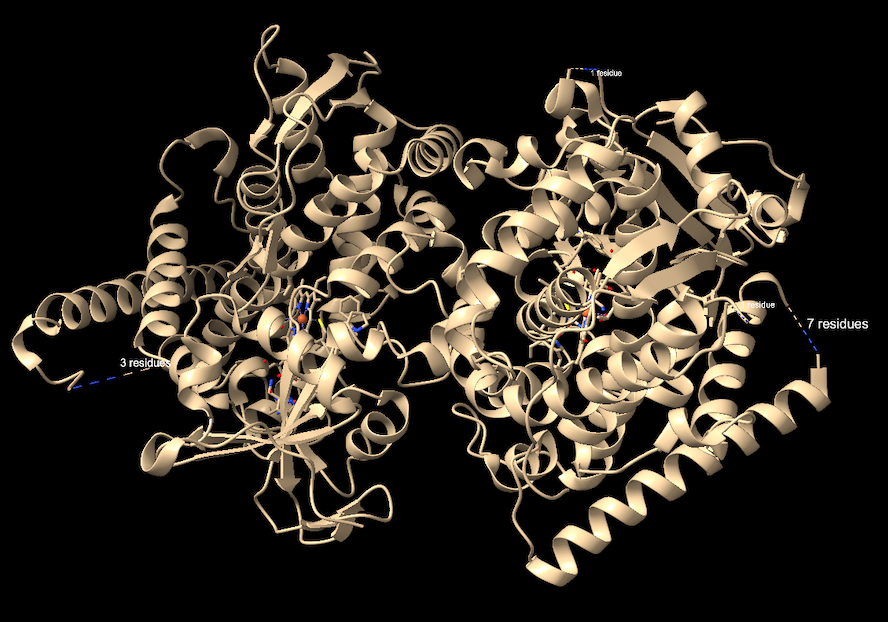
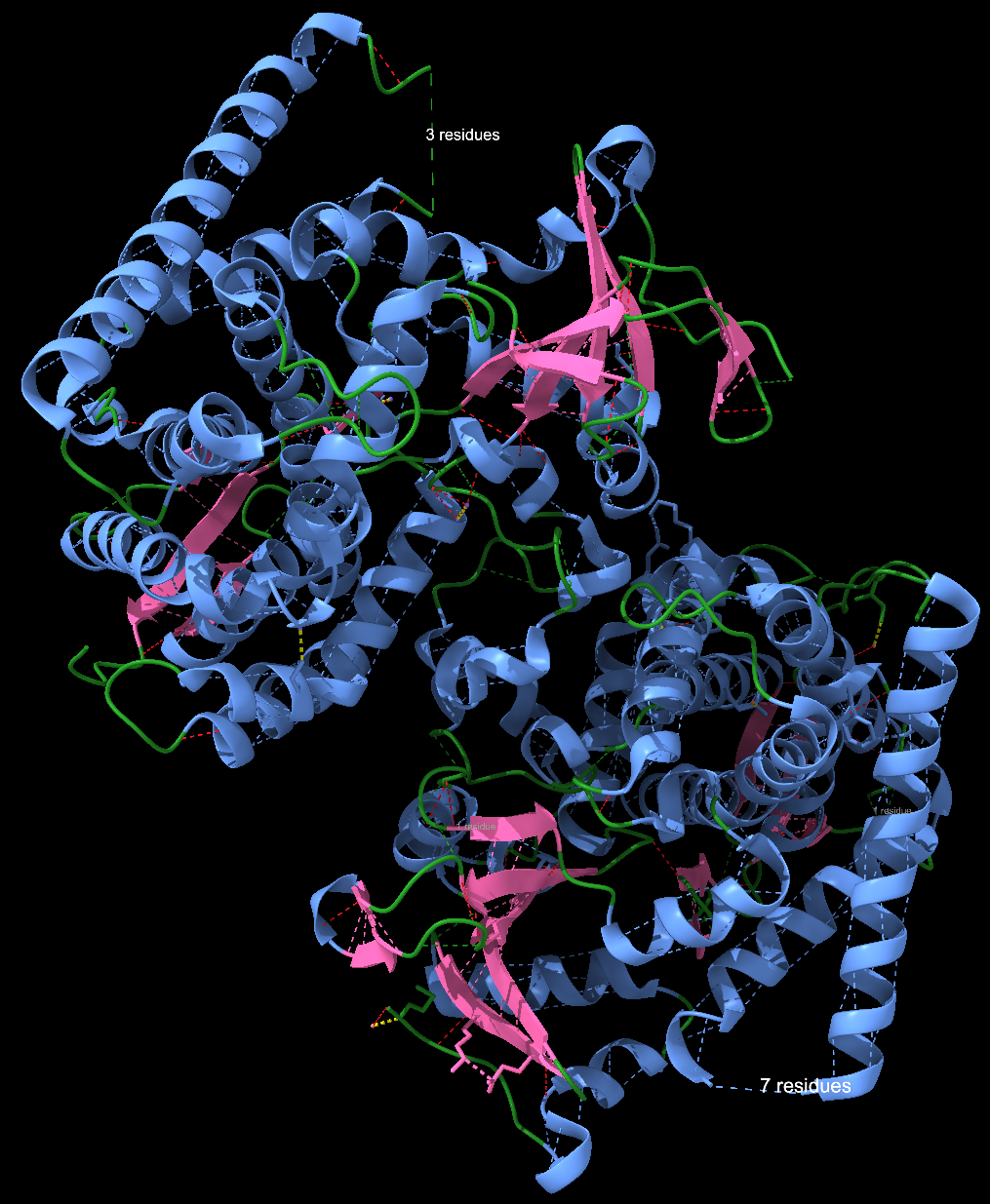
Lloc funcional i mecanisme
La funció natural de BM3 és la hidroxilació d’àcids grassos. El domini hemo activa oxigen i transfereix un àtom d’oxigen al substrat; els dominis reductasa aporten electrons en la proteïna completa.
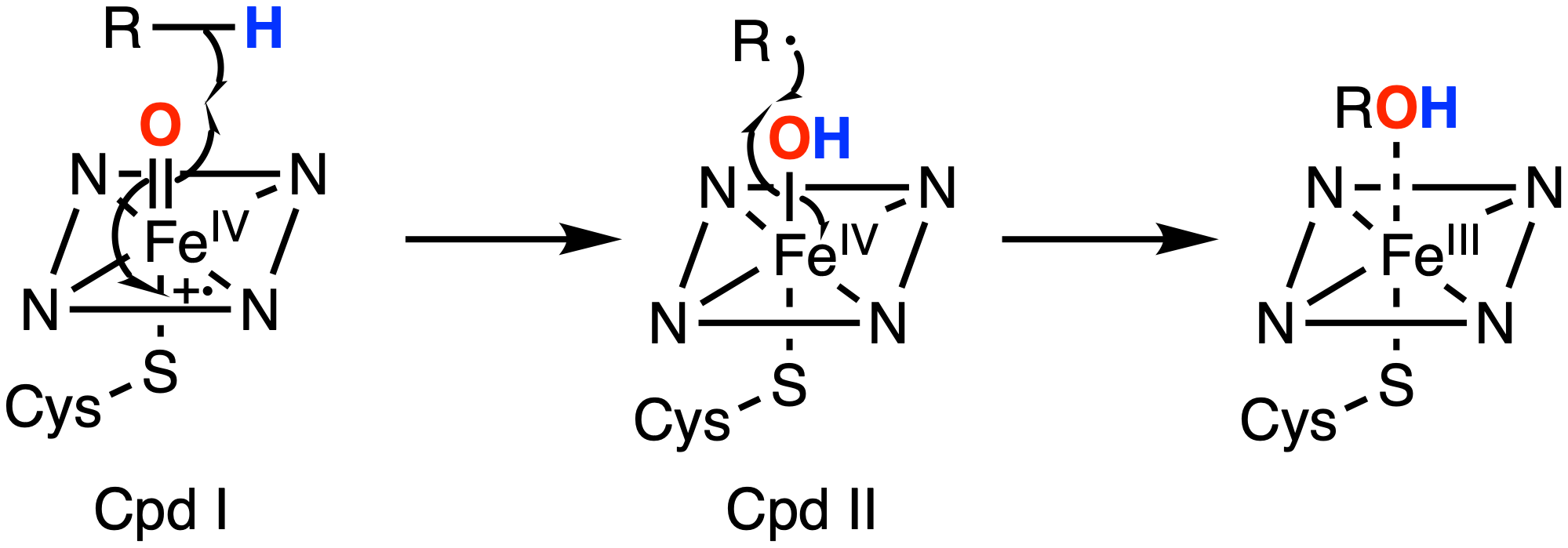
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Whitehouse et al., 2012).
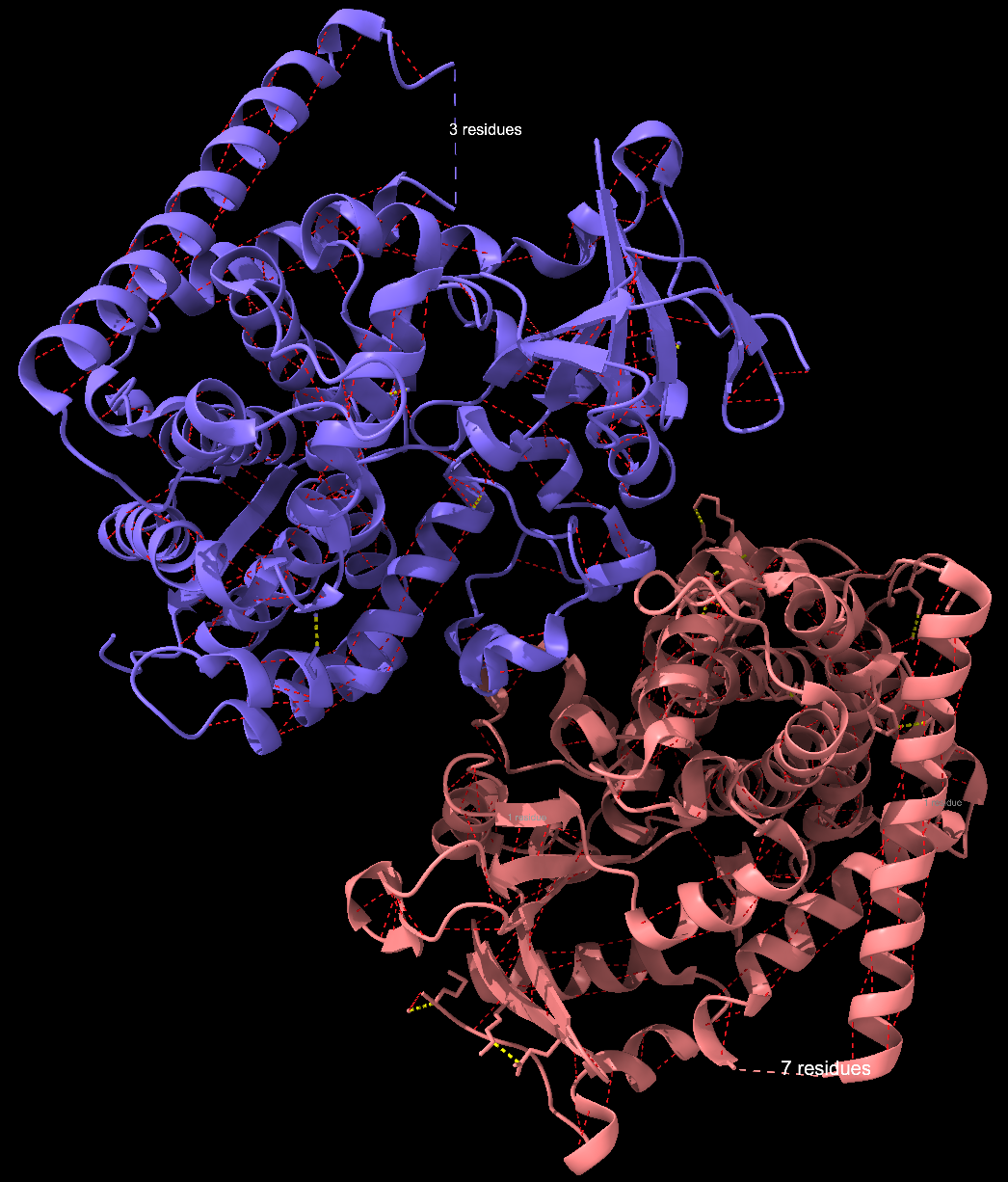
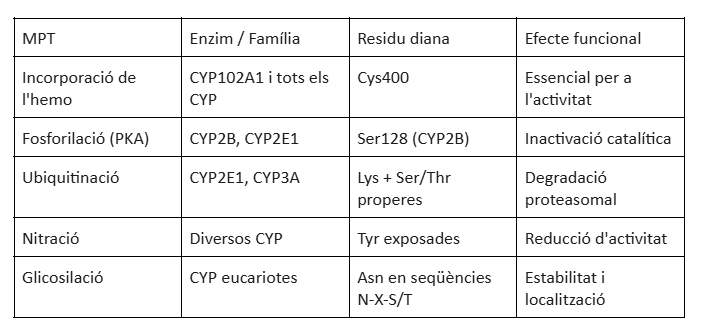
Modificacions i variants
En aquesta variant del domini hemo de BM3, els canvis funcionals s’han d’interpretar com a mutacions d’enginyeria al voltant de l’hemo, el canal de substrat i l’acoblament electrònic. Les anotacions de BM3 completa sobre reductasa o dominis flavínics no s’han de projectar sobre el domini hemo aïllat.
Relació seqüència-estructura-funció
La interpretació molecular connecta hemo, residus de la butxaca, canals d’entrada i mutacions. Quan es fa servir 2IJ2, les posicions s’han de remapejar respecte de 3QI8.
Referències
- Whitehouse, C. J. C.; Bell, S. G.; Wong, L. -L. (2012). P450BM3 (CYP102A1): connecting the dots. Chemical Society Reviews. doi: 10.1039/C1CS15192D.