QIEP
Translocasa SecA
Grup G · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>sp|P10408|SECA_ECOLI Protein translocase subunit SecA OS=Escherichia coli (strain K12) OX=83333 GN=secA PE=1 SV=2 | 2024-2025 | seqüència problema
MLIKLLTKVFGSRNDRTLRRMRKVVNIINAMEPEMEKLSDEELKGKTAEFRARLEKGEVLENLIPEAFAVVREASKRVFG
MRHFDVQLLGGMVLNERCIAEMRTGEGKTLTATLPAYLNALTGKGVHVVTVNDYLAQRDAENNRPLFEFLGLTVGINLPG
MPAPAKREAYAADITYGTNNEYGFDYLRDNMAFSPEERVQRKLHYALVDEVDSILIDEARTPLIISGPAEDSSEMYKRVN
KIIPHLIRQEKEDSETFQGEGHFSVDEKSRQVNLTERGLVLIEELLVKEGIMDEGESLYSPANIMLMHHVTAALRAHALF
TRDVDYIVKDGEVIIVDEHTGRTMQGRRWSDGLHQAVEAKEGVQIQNENQTLASITFQNYFRLYEKLAGMTGTADTEAFE
FSSIYKLDTVVVPTNRPMIRKDLPDLVYMTEAEKIQAIIEDIKERTAKGQPVLVGTISIEKSELVSNELTKAGIKHNVLN
AKFHANEAAIVAQAGYPAAVTIATNMAGRGTDIVLGGSWQAEVAALENPTAEQIEKIKADWQVRHDAVLEAGGLHIIGTE
RHESRRIDNQLRGRSGRQGDAGSSRFYLSMEDALMRIFASDRVSGMMRKLGMKPGEAIEHPWVTKAIANAQRKVESRNFD
IRKQLLEYDDVANDQRRAIYSQRNELLDVSDVSETINSIREDVFKATIDAYIPPQSLEEMWDIPGLQERLKNDFDLDLPI
AEWLDKEPELHEETLRERILAQSIEVYQRKEEVVGAEMMRHFEKGVMLQTLDSLWKEHLAAMDYLRQGIHLRGYAQKDPK
QEYKRESFSMFAAMLESLKYEVISTLSKVQVRMPEEVEELEQQRRMEAERLAQMQQLSHQDDDSAAAAALAAQTGERKVG
RNDPCPCGSGKKYKQCHGRLQ
Seqüència recuperada de UniProt P10408. Longitud: 901 aminoàcids. Cisteïnes: 98, 885, 887, 896.
Identificació i estructura de referència
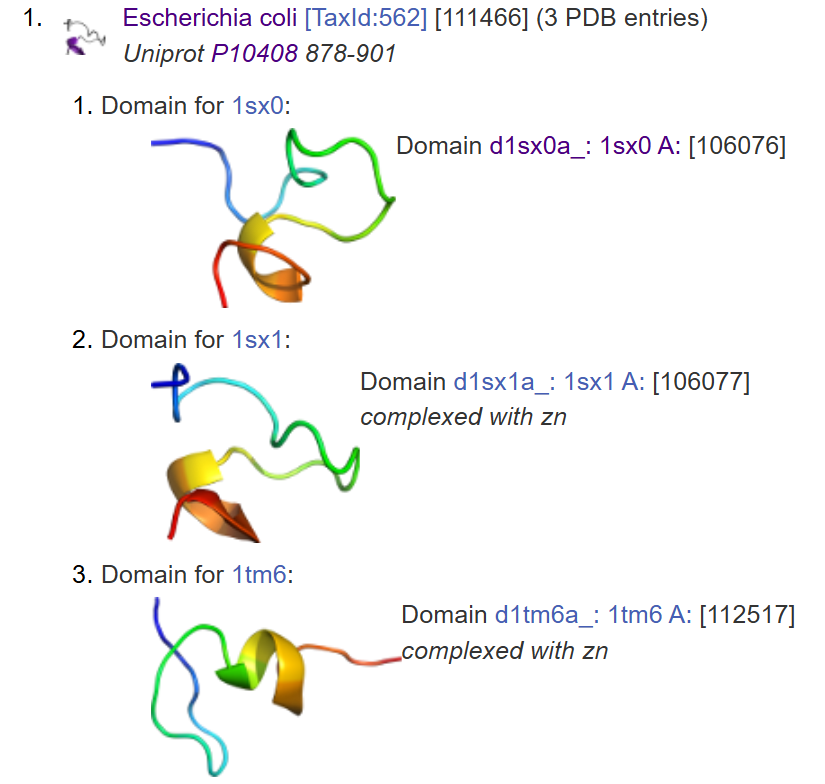
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a traslocasa SecA. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | P10408; gen: secA |
| EC / BRENDA | 7.4.2.8 |
| Estructura principal | 2FSF |
| Plegament o família | ATPasa motora amb dominis NBD/HSD/HWD/PPXD que canvien de disposició durant el cicle de translocació |
| Estructura secundària i lectura ChimeraX | motor SecA amb dominis NBD i dominis de moviment; cal relacionar estat nucleotídic, solc de preproteïna i canvis conformacionals |
| Lligands, cofactors o lloc funcional | ATP/ADP i interacció amb preproteïna/SecYEG; no és un lloc catalític d’un enzim soluble convencional sinó un motor ATP-dependent |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. SecA és una ATPasa de translocació que acobla hidròlisi d’ATP i transport de proteïnes a través del sistema Sec.
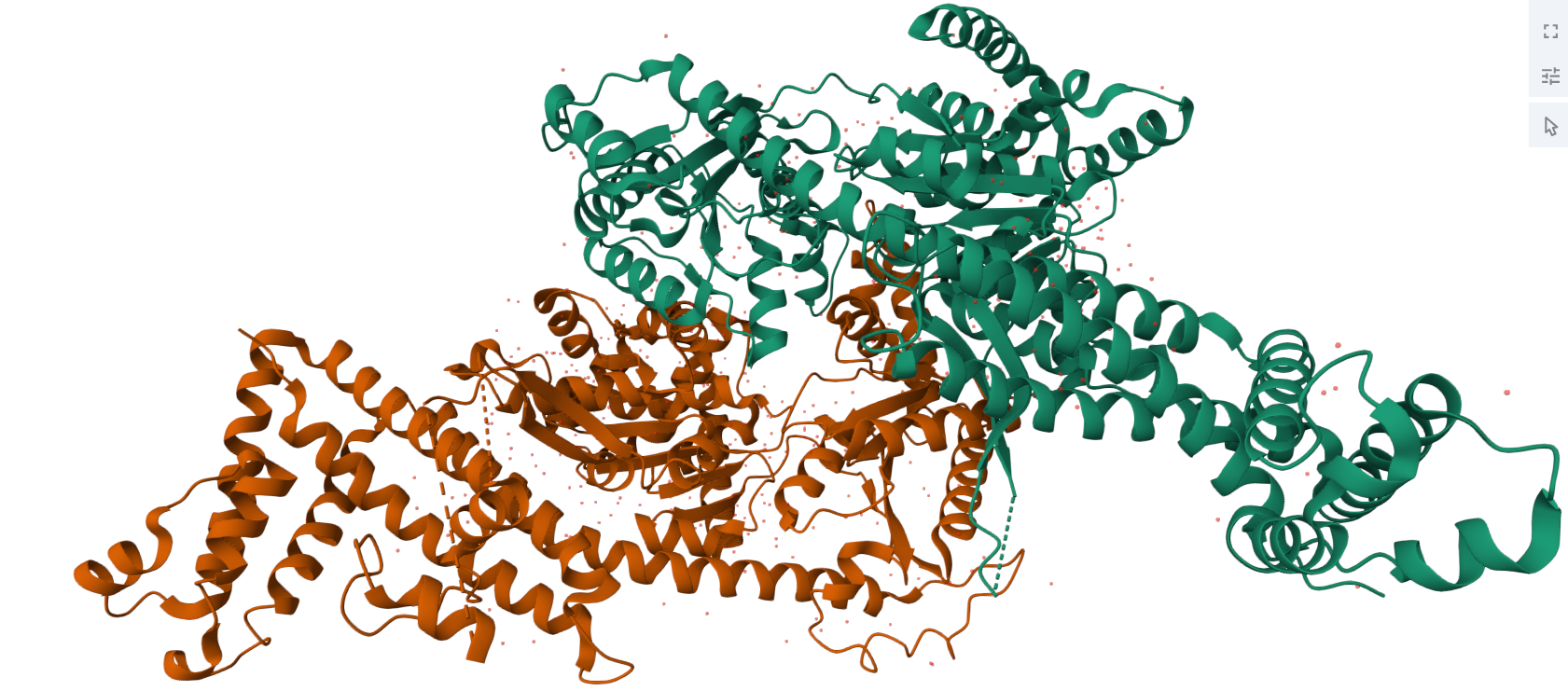
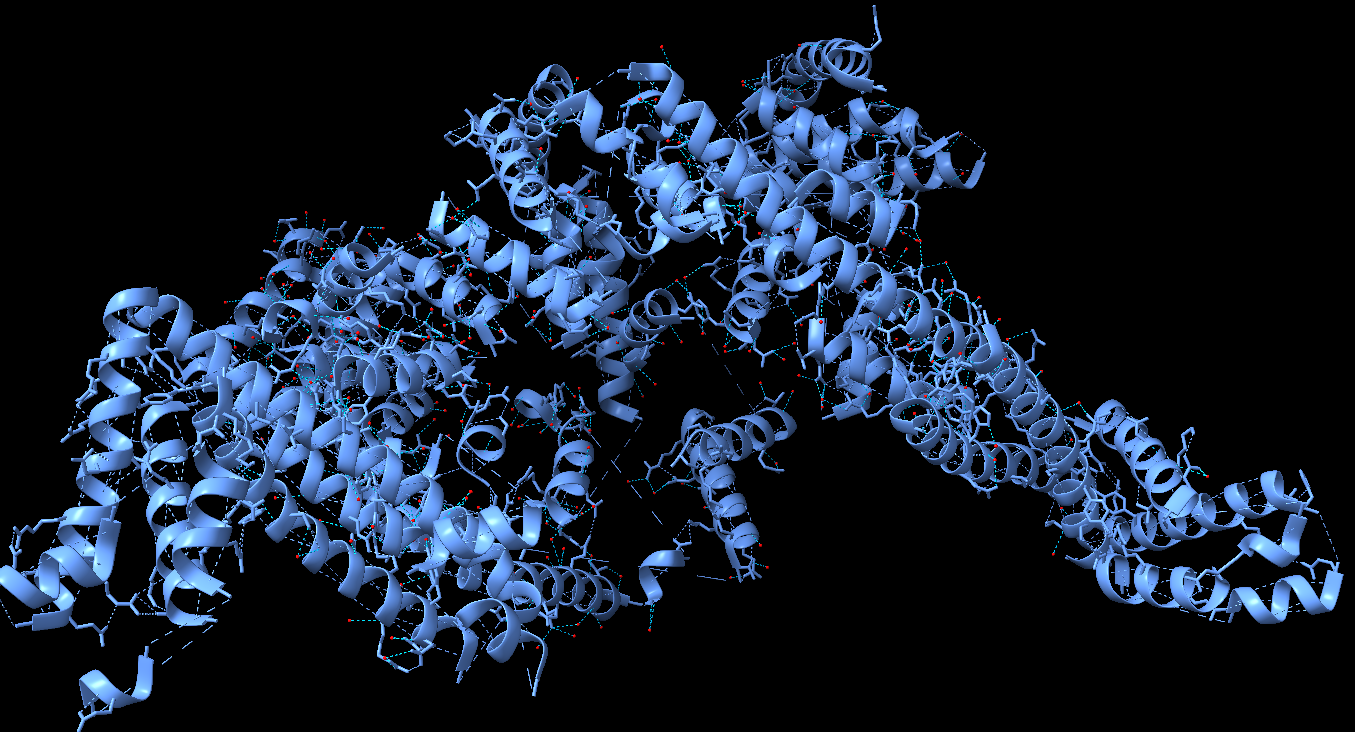
Arquitectura molecular
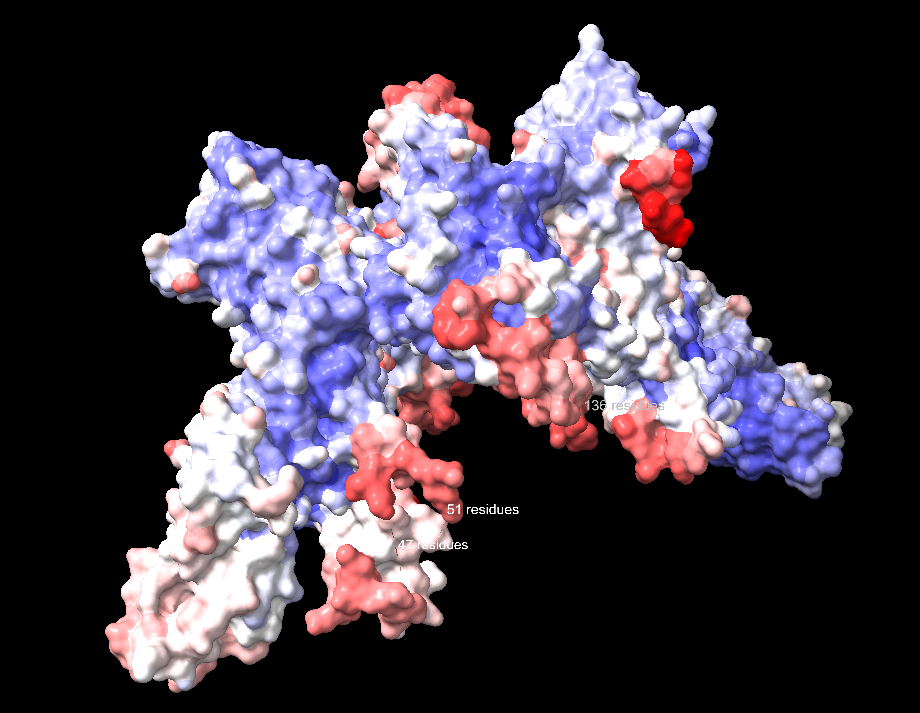
SecA combina dominis d’unió a ATP amb superfícies que contacten el translocó SecYEG i la proteïna client. L’estructura s’entén com una ATPasa motora modular.
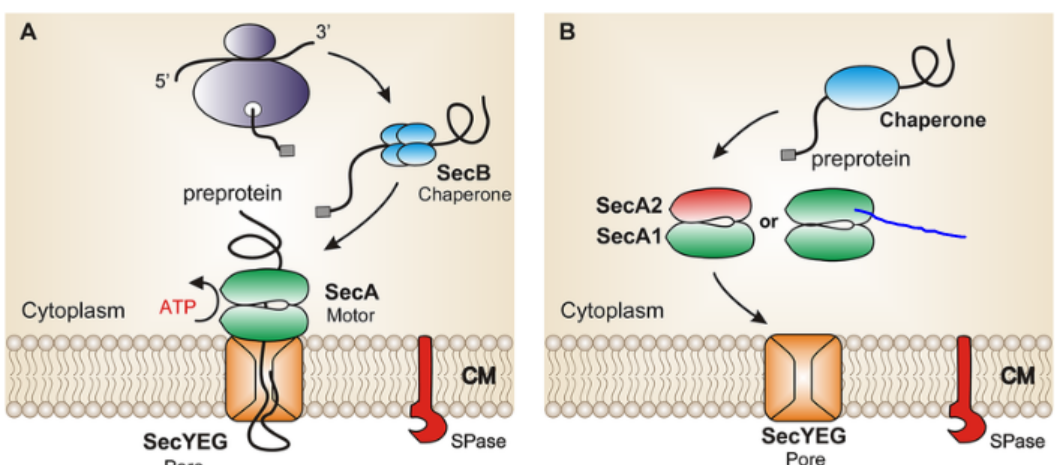
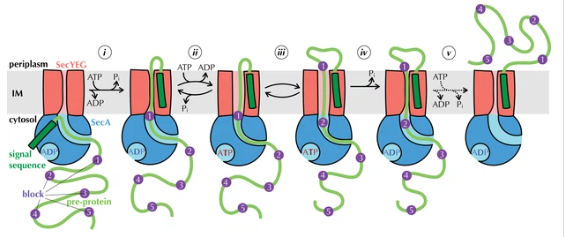
Lloc funcional i mecanisme
La hidròlisi d’ATP impulsa canvis conformacionals que afavoreixen el pas de segments polipeptídics pel canal de translocació.

La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Hunt et al., 2002).
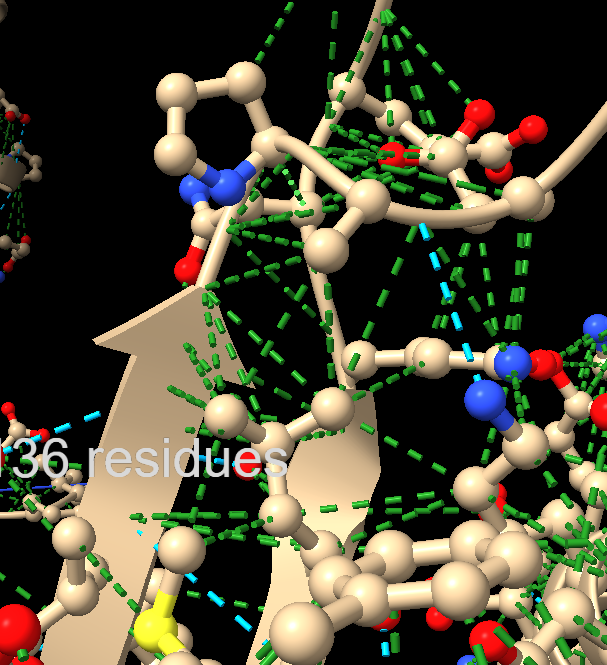
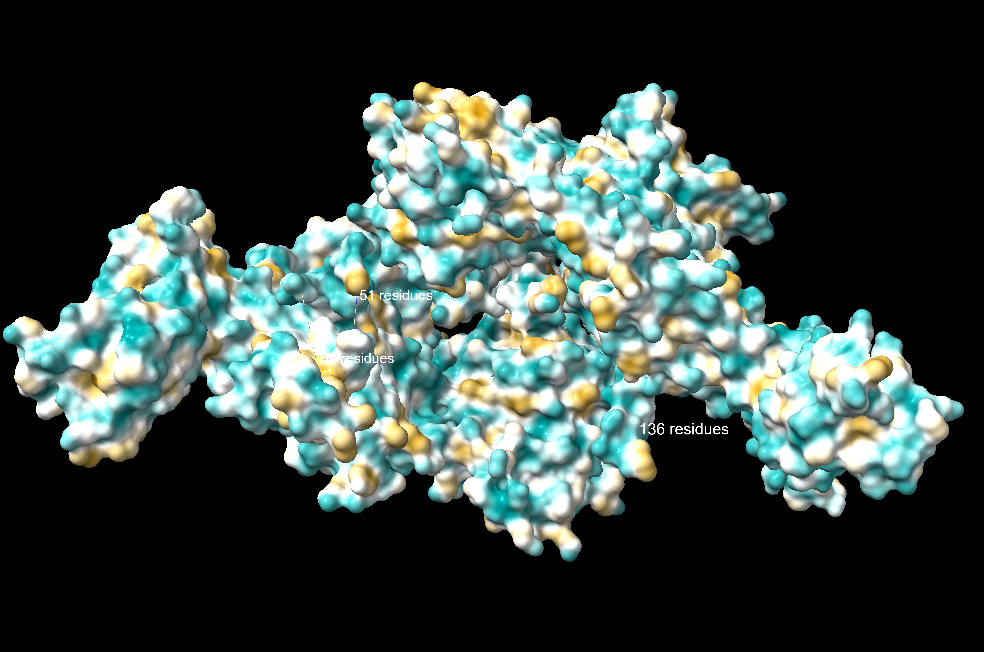
Modificacions i variants
La lectura funcional se centra en variants de dominis i estat nucleotídic; les modificacions posttraduccionals no són el component principal de SecA bacteriana. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.

Referències
- Hunt, J. F. et al. (2002). Nucleotide control of interdomain interactions in the conformational reaction cycle of SecA. Science. doi: 10.1126/science.1074424. També és útil la referència estructural de SecA dimèrica: Papanikolau, Y. et al. (2007), doi: 10.1016/j.jmb.2006.12.049.