QIEP
Amina oxidasa
Grup H · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>sp|P21397|AOFA_HUMAN Amine oxidase [flavin-containing] A OS=Homo sapiens OX=9606 GN=MAOA PE=1 SV=1 | 2024-2025 | seqüència problema
MENQEKASIAGHMFDVVVIGGGISGLSAAKLLTEYGVSVLVLEARDRVGGRTYTIRNEHVDYVDVGGAYVGPTQNRILRL
SKELGIETYKVNVSERLVQYVKGKTYPFRGAFPPVWNPIAYLDYNNLWRTIDNMGKEIPTDAPWEAQHADKWDKMTMKEL
IDKICWTKTARRFAYLFVNINVTSEPHEVSALWFLWYVKQCGGTTRIFSVTNGGQERKFVGGSGQVSERIMDLLGDQVKL
NHPVTHVDQSSDNIIIETLNHEHYECKYVINAIPPTLTAKIHFRPELPAERNQLIQRLPMGAVIKCMMYYKEAFWKKKDY
CGCMIIEDEDAPISITLDDTKPDGSLPAIMGFILARKADRLAKLHKEIRKKKICELYAKVLGSQEALHPVHYEEKNWCEE
QYSGGCYTAYFPPGIMTQYGRVIRQPVGRIFFAGTETATKWSGYMEGAVEAGERAAREVLNGLGKVTEKDIWVQEPESKD
VPAVEITHTFWERNLPSVSGLLKIIGFSTSVTALGFVLYKYKLLPRS
Seqüència recuperada de UniProt P21397. Longitud: 527 aminoàcids. Cisteïnes: 165, 201, 266, 306, 321, 323, 374, 398, 406.
Identificació i estructura de referència
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a amina oxidasa. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | P21397; gen: AOC/amine oxidase segons organisme |
| EC / BRENDA | 1.4.3.4 |
| Estructura principal | 2Z5Y |
| Plegament o família | enzim de coure amb cofactor TPQ derivat d’una tirosina interna |
| Estructura secundària i lectura ChimeraX | enzim de coure amb cofactor TPQ; cal situar Cu, TPQ i canal d’accés de l’amina dins del plegament |
| Lligands, cofactors o lloc funcional | Cu i TPQ al centre actiu; el substrat amina forma una base de Schiff i es converteix en aldehid amb producció de peròxid d’hidrogen |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. Les amina oxidases oxiden amines i generen aldehids, amoníac i peròxid d’hidrogen mitjançant cofactors especialitzats.
Arquitectura molecular
Les amina oxidases presenten cavitats d’accés al substrat connectades amb cofactors orgànics o metàl·lics. La forma del canal contribueix a la selectivitat.

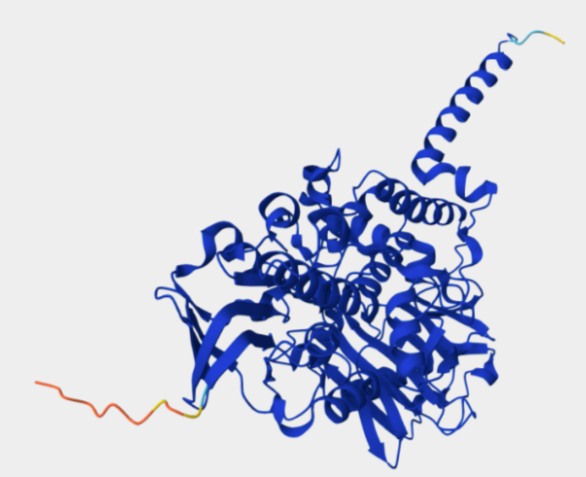
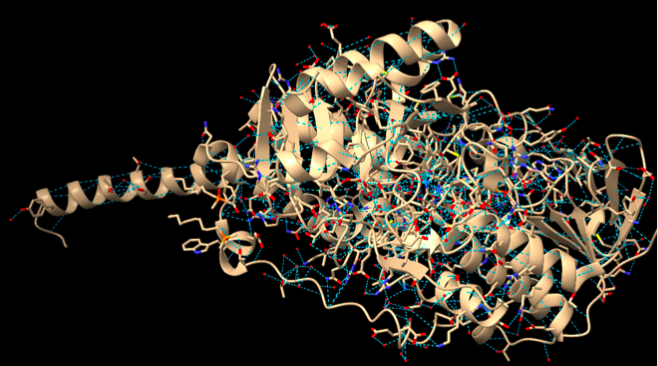
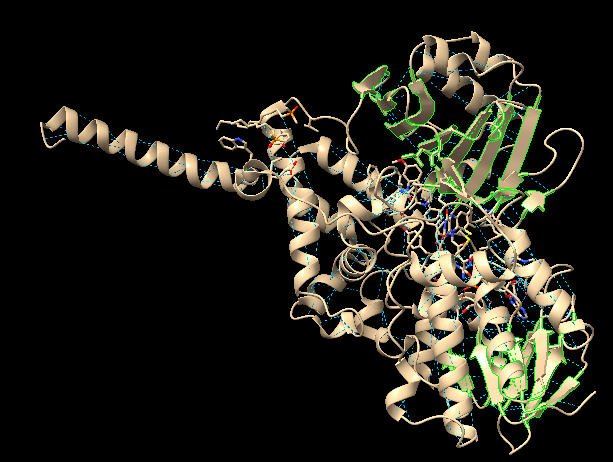
Lloc funcional i mecanisme
L’oxidació d’amines genera aldehid, amoníac i peròxid d’hidrogen. La posició del cofactor i dels residus àcid-base controla la transferència d’electrons i protons.
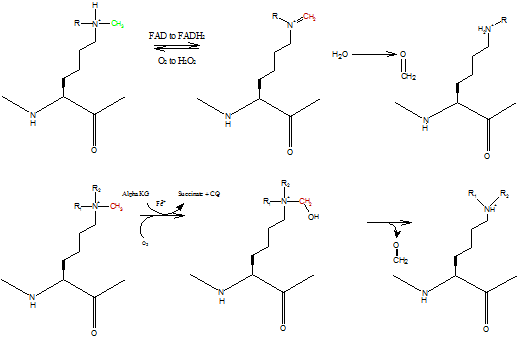
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Mure et al., 2002).
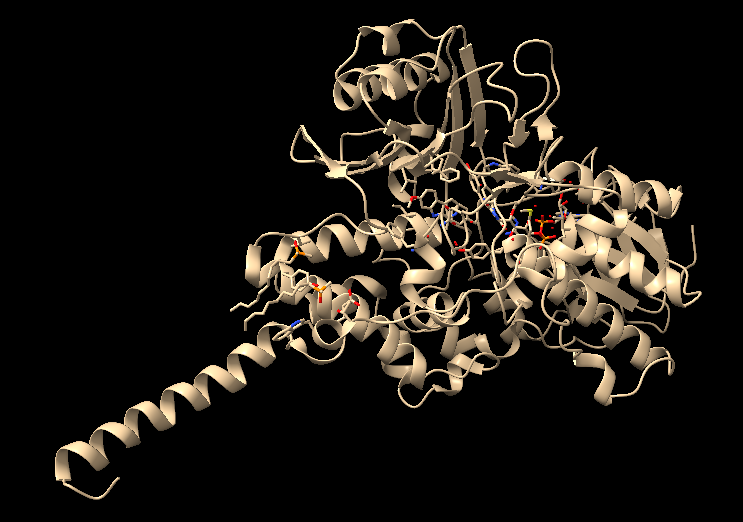
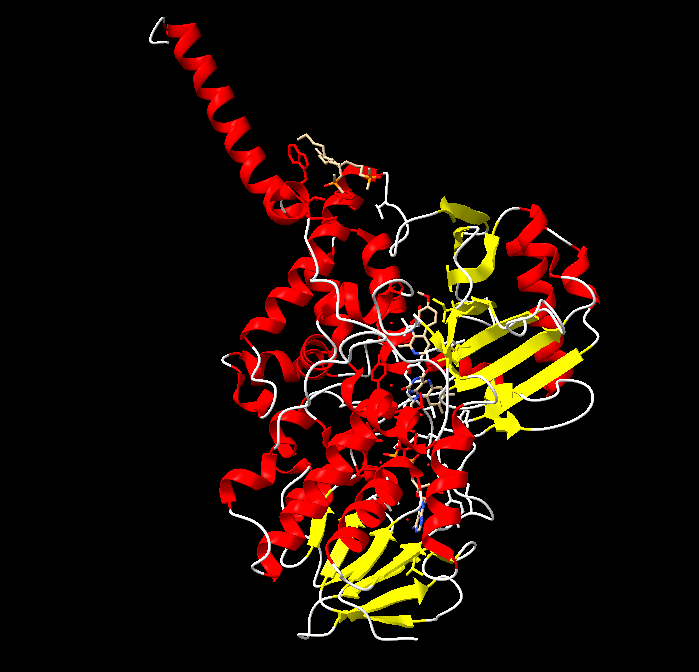
Modificacions i variants
La modificació essencial és la biogènesi de TPQ a partir de tirosina; cal numerar el residu segons la seqüència exacta. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
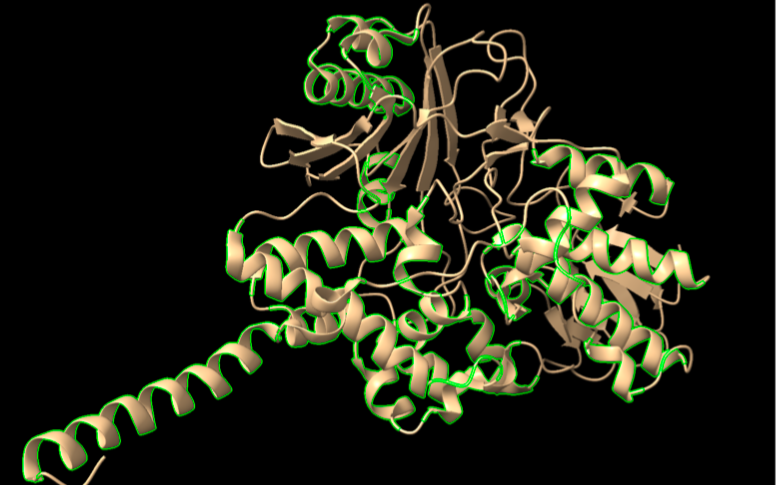
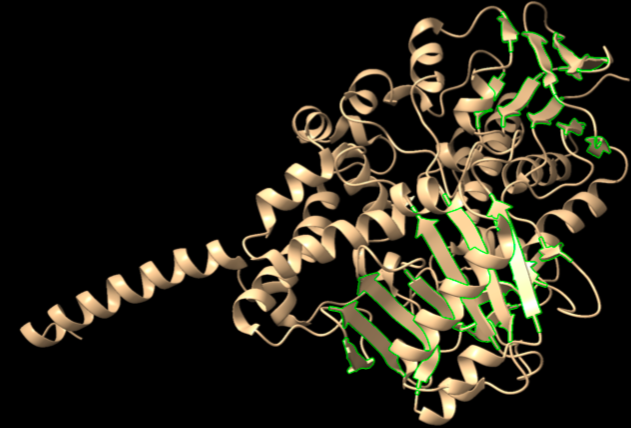
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.
Referències
- Mure, M.; Mills, S. A.; Klinman, J. P. (2002). Catalytic Mechanism of the Topa Quinone Containing Copper Amine Oxidases. Biochemistry. doi: 10.1021/bi020246b.