QIEP
Epoxi hidrolasa microsomal 1
Grup J · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>sp|P07099|HYEP_HUMAN Epoxide hydrolase 1 OS=Homo sapiens OX=9606 GN=EPHX1 PE=1 SV=1 | 2024-2025 | seqüència problema
MWLEILLTSVLGFAIYWFISRDKEETLPLEDGWWGPGTRSAAREDDSIRPFKVETSDEEIHDLHQRIDKFRFTPPLEDSC
FHYGFNSNYLKKVISYWRNEFDWKKQVEILNRYPHFKTKIEGLDIHFIHVKPPQLPAGHTPKPLLMVHGWPGSFYEFYKI
IPLLTDPKNHGLSDEHVFEVICPSIPGYGFSEASSKKGFNSVATARIFYKLMLRLGFQEFYIQGGDWGSLICTNMAQLVP
SHVKGLHLNMALVLSNFSTLTLLLGQRFGRFLGLTERDVELLYPVKEKVFYSLMRESGYMHIQCTKPDTVGSALNDSPVG
LAAYILEKFSTWTNTEFRYLEDGGLERKFSLDDLLTNVMLYWTTGTIISSQRFYKENLGQGWMTQKHERMKVYVPTGFSA
FPFELLHTPEKWVRFKYPKLISYSYMVRGGHFAAFEEPELLAQDIRKFLSVLERQ
Seqüència recuperada de UniProt P07099. Longitud: 455 aminoàcids. Cisteïnes: 80, 182, 232, 304.
Identificació i estructura de referència
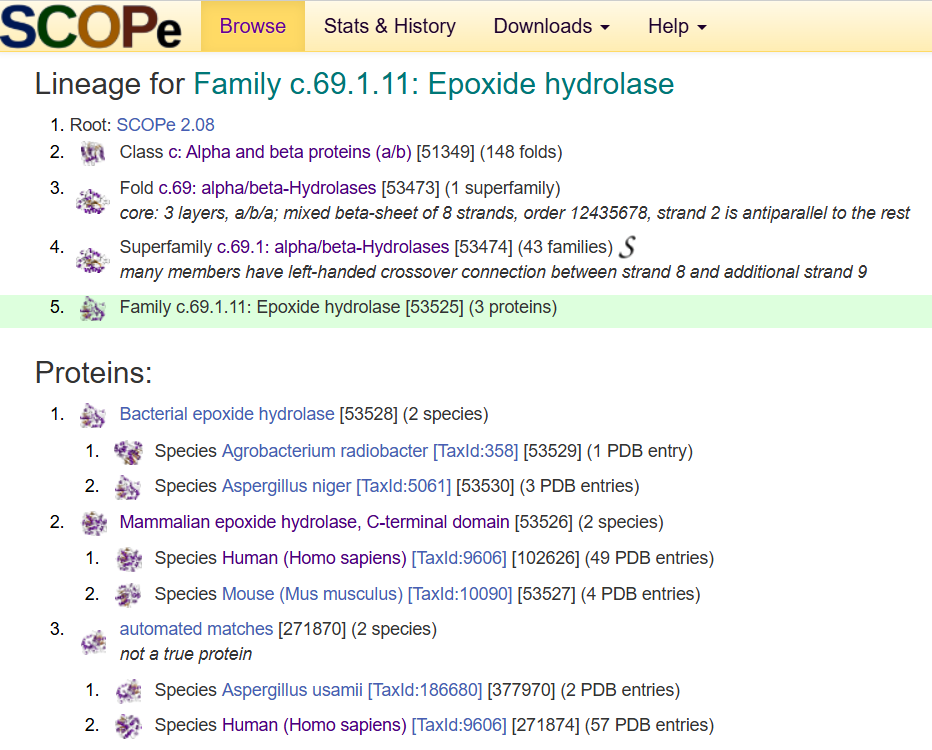
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a epoxi hidrolasa microsomal 1. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | P07099; gen: EPHX1 |
| EC / BRENDA | 3.3.2.9 / 3.3.2.3 |
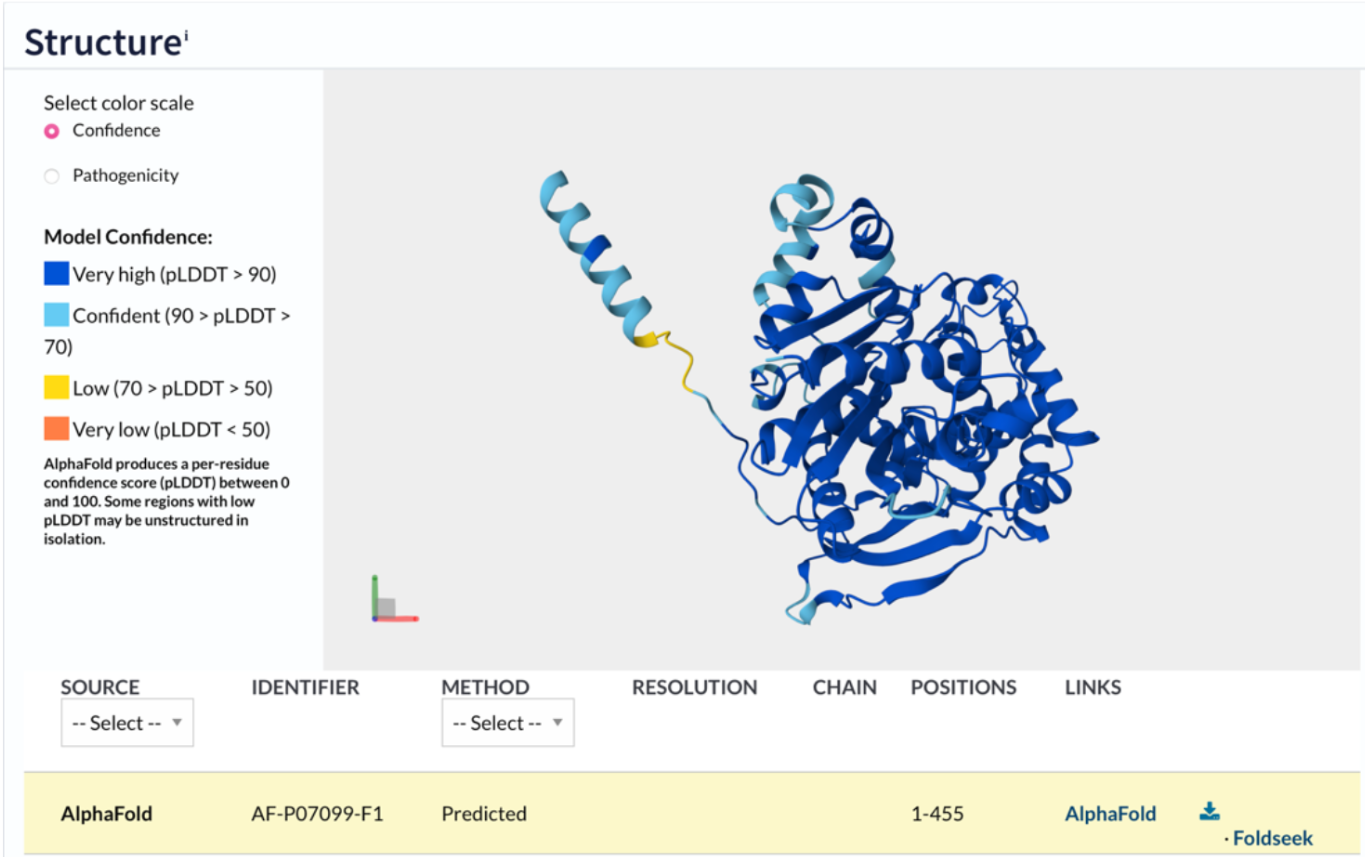
| Estructura principal | model experimental o AlphaFold segons cobertura |
| Plegament o família | α/β hidrolasa amb triada catalítica i butxaca per epòxids hidrofòbics |
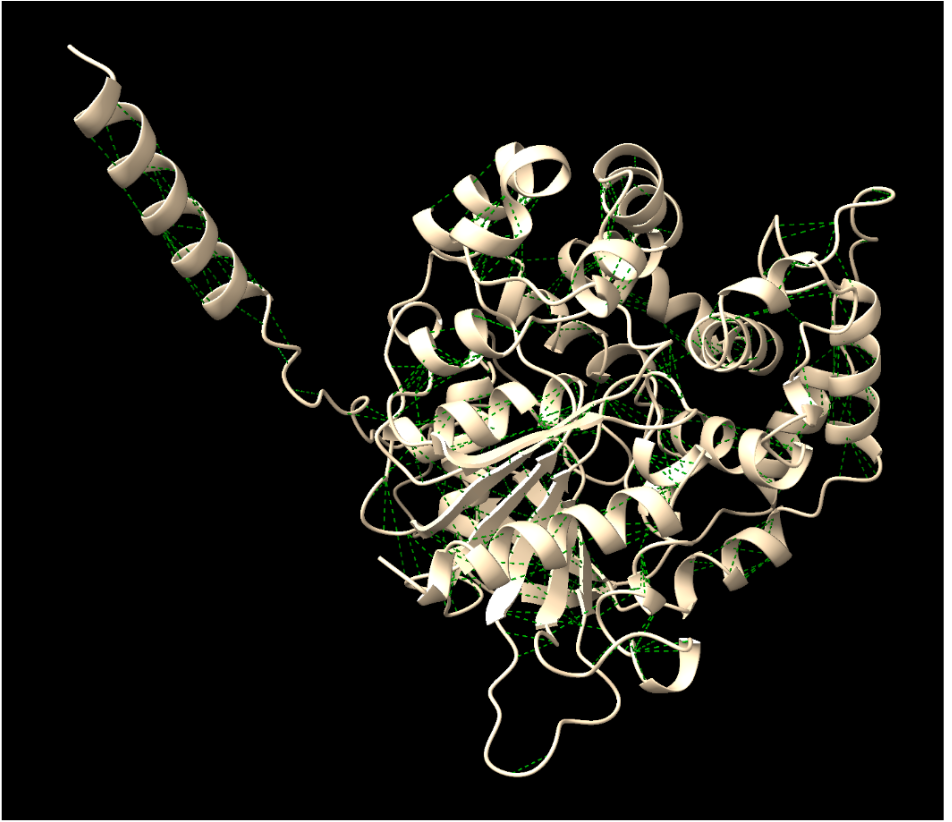
| Estructura secundària i lectura ChimeraX | α/β hidrolasa de membrana; cal separar nucli catalític, cavitat hidrofòbica i regions d’ancoratge o contacte amb membrana |
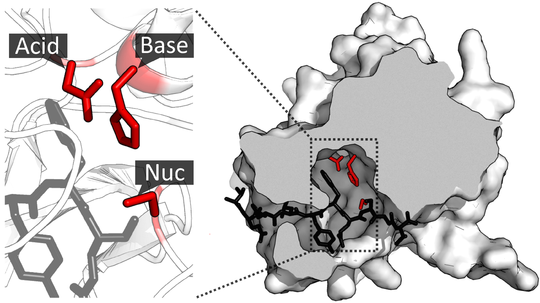
| Lligands, cofactors o lloc funcional | epòxid al centre actiu; el mecanisme forma un intermedi covalent hidroxialquil-enzim i després l’hidrolitza |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. L’epoxi hidrolasa microsomal 1 transforma epòxids reactius en diols, una reacció important en metabolisme de xenobiòtics.
Arquitectura molecular
EPHX1 és una hidrolasa associada al metabolisme de compostos lipòfils. La seva arquitectura combina un nucli catalític amb regions adequades per captar epòxids hidrofòbics.
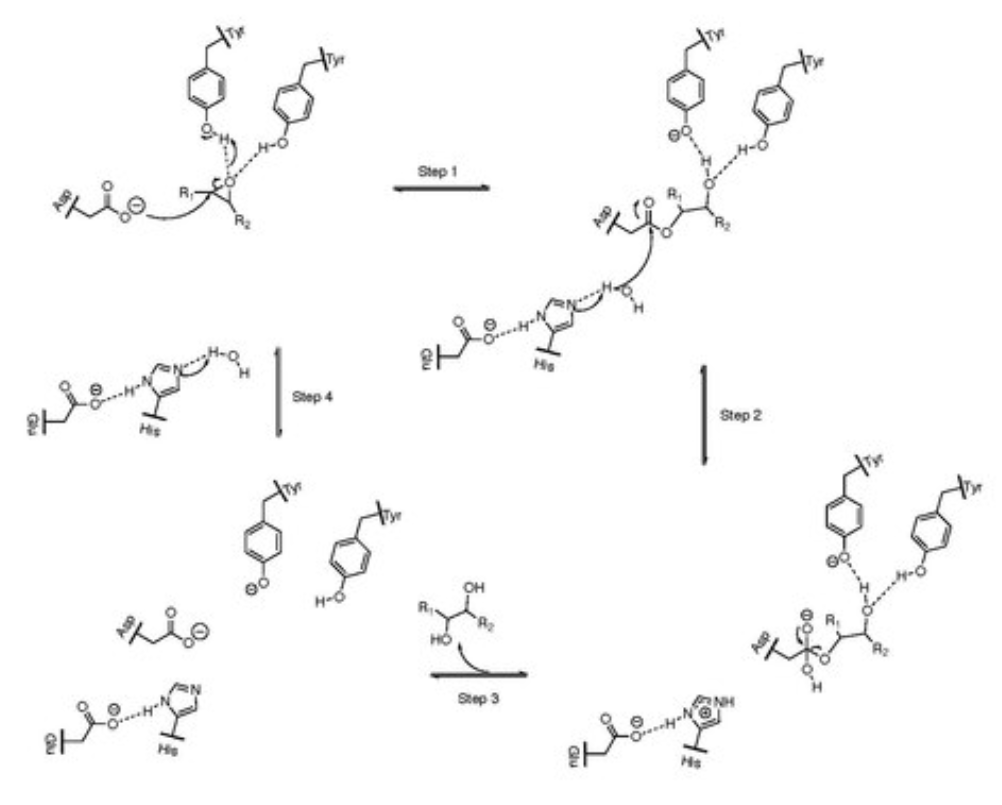
Lloc funcional i mecanisme
El mecanisme obre l’epòxid i produeix un diol. La xarxa catalítica activa aigua i estabilitza intermedis, reduint la reactivitat del substrat original.
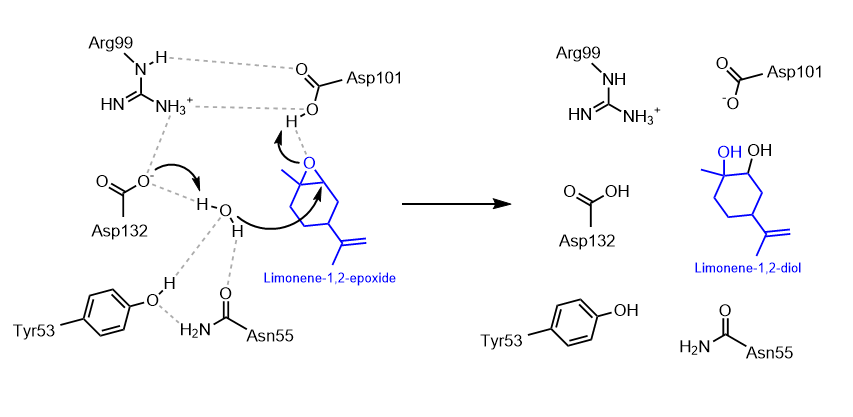
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Morisseau et al., 2005).
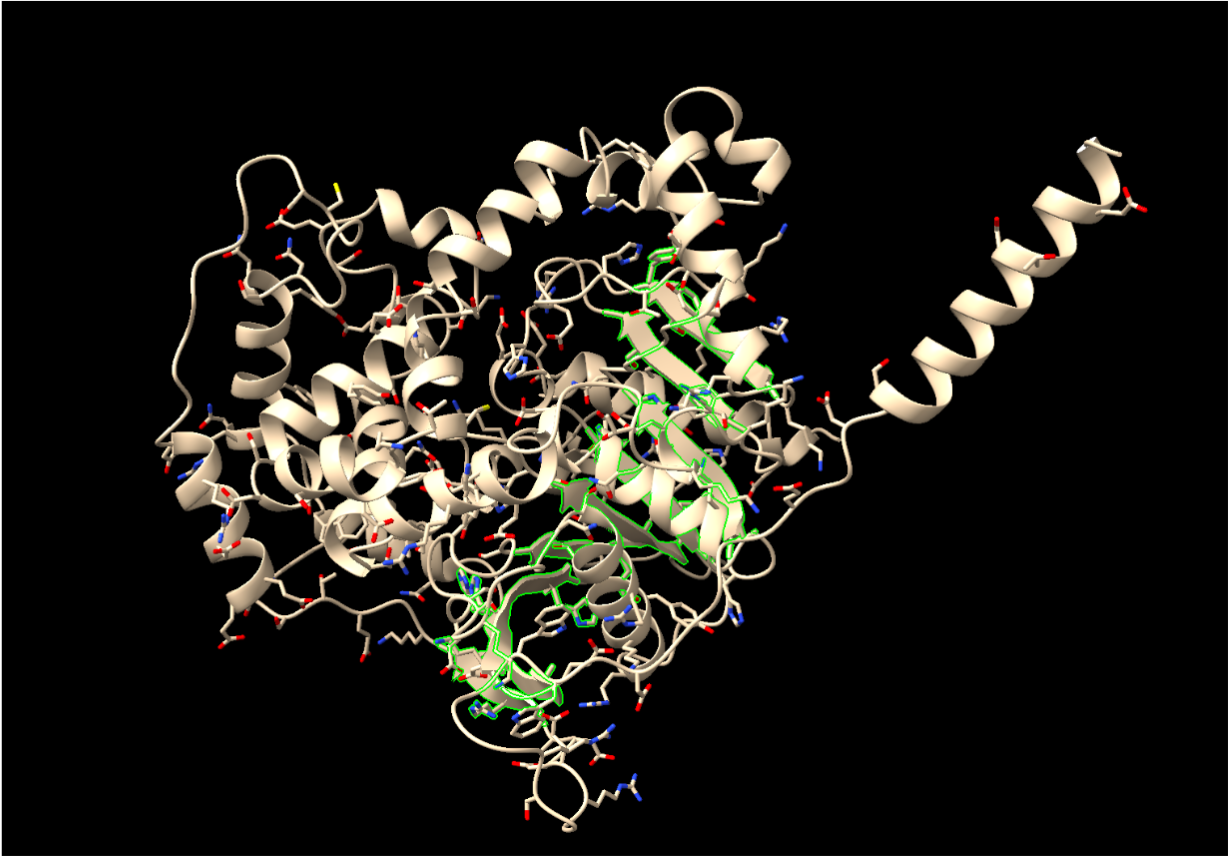
Modificacions i variants
En EPHX1 humana interessen variants funcionals i context de membrana; les variants s’han de mapar a la seqüència exacta. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.
Referències
- Morisseau, C.; Hammock, B. D. (2005). Epoxide Hydrolases: Mechanisms, Inhibitor Designs, and Biological Roles. Annual Review of Pharmacology and Toxicology. doi: 10.1146/annurev.pharmtox.45.120403.095920.