QIEP
Glicosiltransferasa
Grup I · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>8CHD | 2024-2025 | seqüència problema
MEATQRDGGAQSPTPHVVMLPSPGMGHLIPLLEFAKRLLFLHRFTVTFAIPSGDPPSKAQISILSSLPSGIDYVFLPPVN
FHDLPKDTKAGVFIVLAVARSLPSFRDLFKSMVANTNLVALVVDQFGTDAFDVAREFNVSPYIFFPCAAMTLSFLLRLPE
FDETVAGEYRELPEPIRLSGCAPIPGKDLAGPFHDRENDAYKLFLHNAKRYALADGIFLNSFPELEPGAIKALLEEESRK
PLVHPVGPLVQIDSSGSEEGAECLKWLEEQPHGSVLFVSFGSGGALSSDQINELALGLEMSGHRFIWVVRSPSDEAANAS
FFSVHSQNDPLSFLPEGFLEGTRGRSVVVPSWAPQAQILSHSSTGGFLSHCGWNSTLESVVYGVPLIAWPLYAEQKMNAI
LLTEDIKAALRPKINEESGLIEKEEIAEVVKELFEGEDGKRVRAKMEELKDAAVRVLGEDGSSSTLSEVVQKWKRKISG
Seqüència recuperada del lliurament original (practica1qep.md). Longitud: 479 aminoàcids. Cisteïnes: 147, 181, 263, 371.
Identificació i estructura de referència
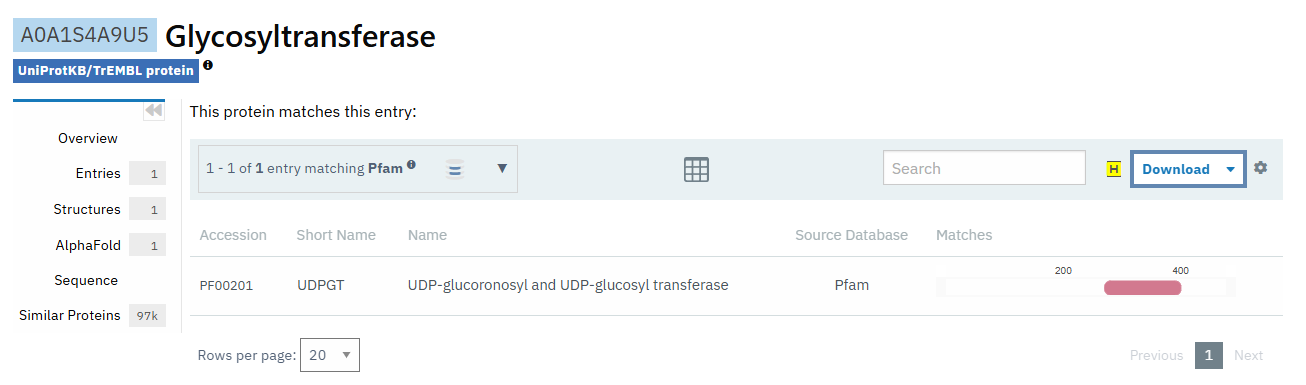
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a glicosiltransferasa. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | no fixat a la pàgina original; gen: glicosiltransferasa segons família |
| EC / BRENDA | segons substrat i família CAZy/GT |
| Estructura principal | 8CHD |
| Plegament o família | domini GT-A o GT-B segons la família; reconeixement de sucre nucleòtid i acceptor |
| Estructura secundària i lectura ChimeraX | domini de glicosiltransferasa amb cavitats per donador i acceptor; cal distingir l’arquitectura GT i els residus de coordinació del substrat |
| Lligands, cofactors o lloc funcional | donador glicosídic, acceptor i sovint metall divalent en GT-A; cal separar mecanisme inversor o retenidor |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. Les glicosiltransferases formen enllaços glicosídics transferint sucres activats cap a acceptors específics. El codi PDB: 8CHD permet situar el domini catalític i les cavitats de reconeixement del donador i de l’acceptor.
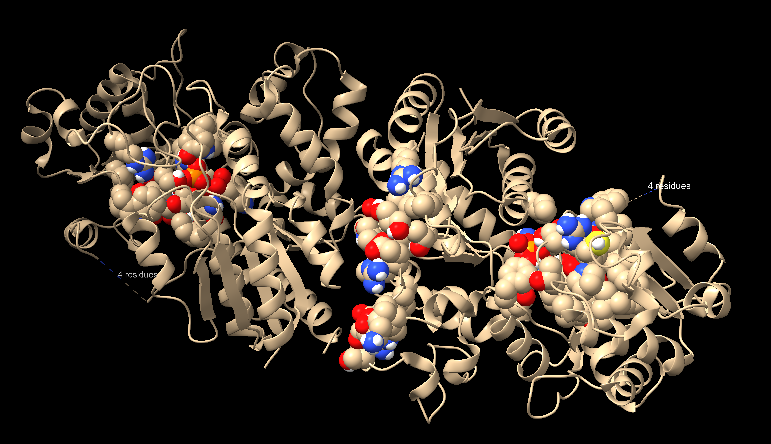
Arquitectura molecular
Les glicosiltransferases organitzen un donador nucleòtid-sucre i un acceptor en una escletxa catalítica. La geometria entre dominis explica especificitat i estereoquímica.
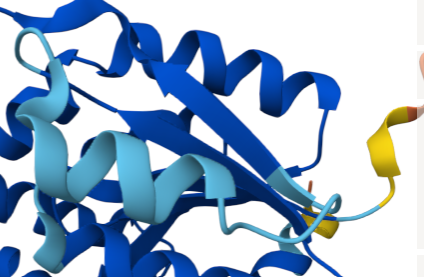
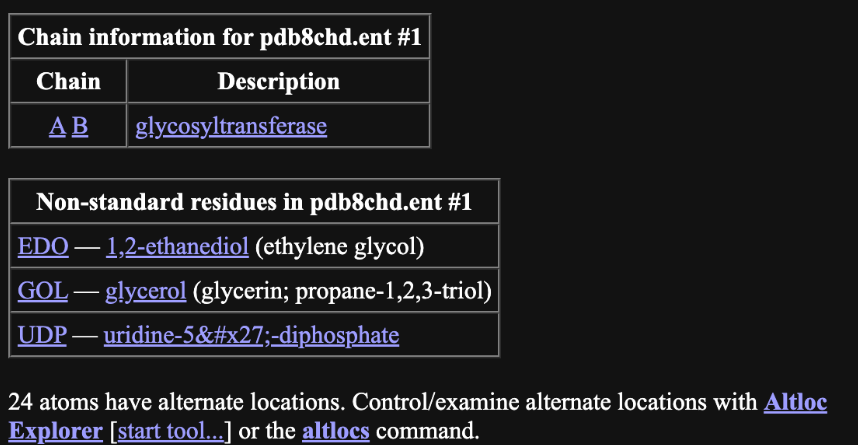
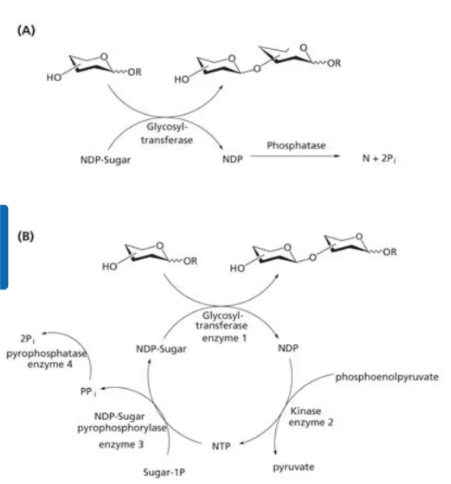
Lloc funcional i mecanisme
La reacció forma un nou enllaç glicosídic. La identitat del nucleòtid-sucre, el grup acceptor i els residus que estabilitzen l’estat de transició determinen el producte.
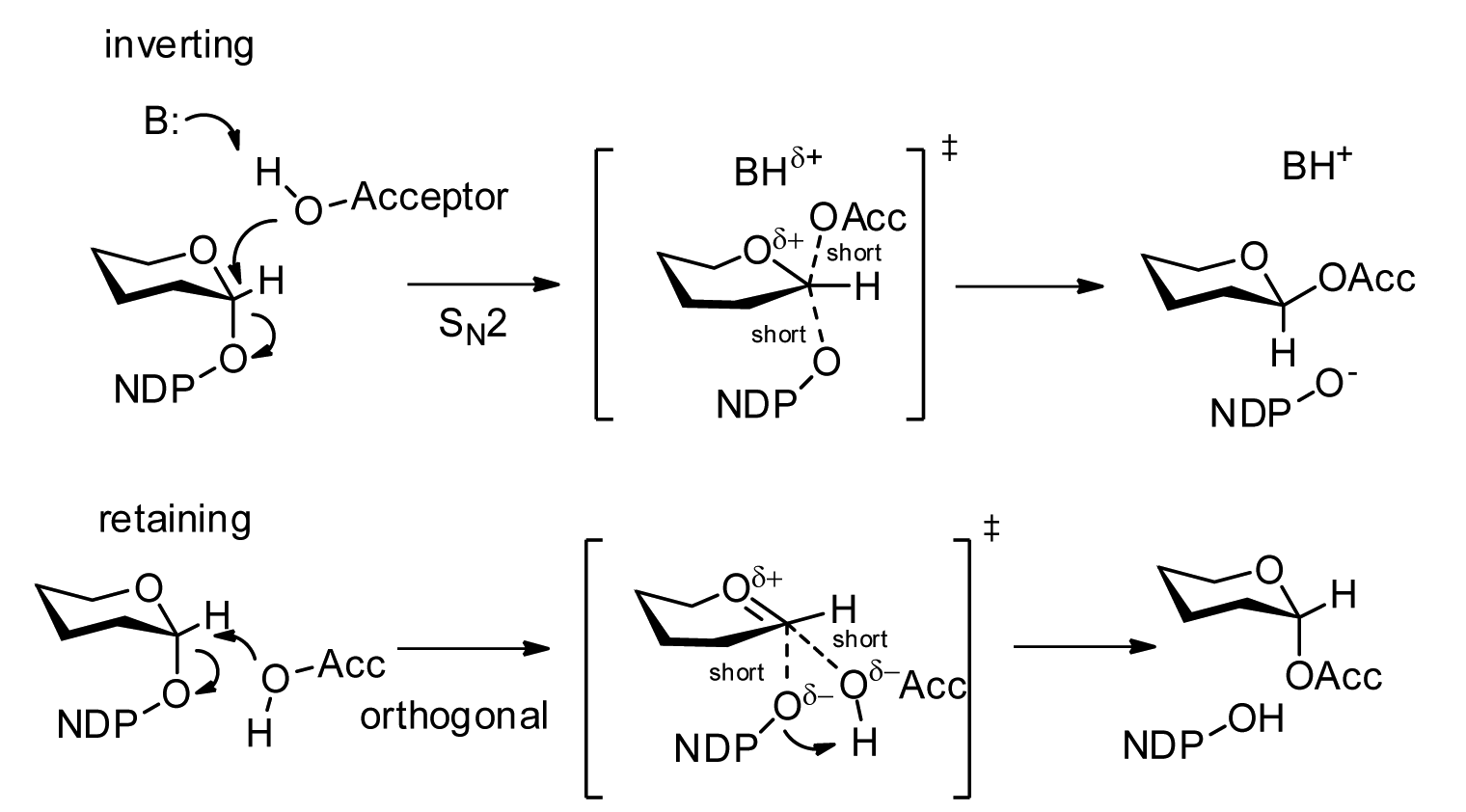
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Lairson et al., 2008).
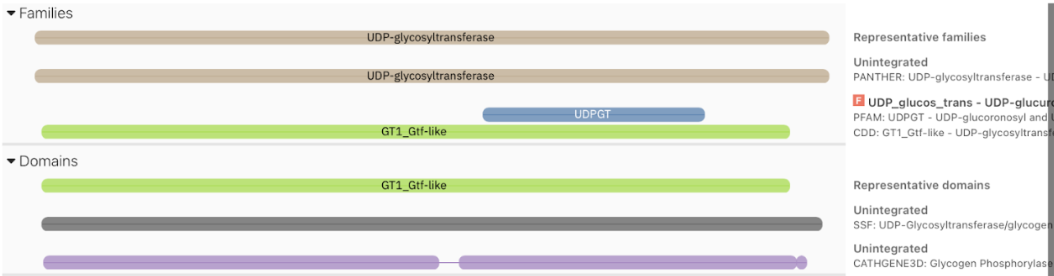
Modificacions i variants
Les modificacions posttraduccionals són secundàries respecte a la identitat de família GT i als residus que coordinen donador/acceptor. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.
Referències
- Lairson, L. L. et al. (2008). Glycosyltransferases: Structures, Functions, and Mechanisms. Annual Review of Biochemistry. doi: 10.1146/annurev.biochem.76.061005.092322.