Capítol 5 Química de Materials
(darrera actualització: 13 de maig de 2026)
Índex
5.1 Introducció
Un automòbil és un sistema químic i mecànic format per moltes famílies de materials, com acers i aliatges lleugers a l’estructura, polímers a l’interior i als sistemes elèctrics, elastòmers als pneumàtics i juntes, ceràmiques als sensors i als catalitzadors, vidres laminats a l’habitacle i materials electroquímics a bateries i cèl·lules de combustible. La tria no és només una qüestió de “resistència”. Cal equilibrar densitat, rigidesa, tenacitat, temperatura de servei, corrosió, procés de fabricació, cost, reparabilitat i impacte ambiental[4, 8].
La química permet connectar aquests criteris macroscòpics amb l’estructura microscòpica. L’enllaç metàl·lic explica la conductivitat i ductilitat dels aliatges; l’enllaç covalent i les forces intermoleculars expliquen ,
, elasticitat i degradació dels polímers; les xarxes iòniques/covalents expliquen la duresa i fragilitat de moltes ceràmiques; i la química superficial controla adhesió, catàlisi, corrosió i compatibilitat entre fases. El capítol segueix aquest fil. Primer tracta criteris de selecció, després polímers, compostos i
elastòmers, a continuació ceràmiques i aliatges, i finalment materials per a cèl·lules de combustible.
5.2 Criteris de selecció de materials
El disseny d’un component d’automoció parteix de la funció. Un para-xocs ha d’absorbir energia d’impacte i recuperar forma; un disc de fre ha de suportar temperatura i fricció; una llanta necessita baixa massa no suspesa i bona dissipació tèrmica; un dipòsit d’hidrogen ha de combinar baixa permeabilitat, resistència a fatiga i seguretat. Per tant, la pregunta correcta no és “quin material és millor?”, sinó “quin material dona la millor combinació de propietats per a una funció i un procés concrets?”[4].
Un criteri central en automoció és la propietat específica, és a dir, una propietat dividida per la densitat. Un acer pot ser molt resistent, però si un alumini, un magnesi o un compost de fibra de carboni ofereix una resistència suficient amb menys massa, el balanç pot afavorir el material lleuger. Aquesta reducció de massa impacta el consum, les emissions i, en peces com rodes o elements de suspensió, la resposta dinàmica del vehicle. Tanmateix, la lleugeresa no justifica qualsevol substitució. Cal comprovar també fatiga, unió amb altres materials, reciclatge, inflamabilitat, manteniment i cost total.
5.3 Plàstics i polímers
Els materials plàstics han guanyat pes en automoció perquè combinen baixa densitat, resistència a la corrosió, bon aïllament elèctric i una gran llibertat de disseny. A més, es poden transformar per injecció, extrusió o bufament en geometries que serien cares o difícils amb metall. Un vehicle pot contenir més d’una desena de famílies polimèriques, però tres d’elles —polipropilè, poliuretà i PVC— concentren una part majoritària del plàstic emprat[20]. La selecció, però, no és genèrica. Un connector elèctric, una escuma de seient, una lent de far i un dipòsit de fluid imposen requisits químics i mecànics diferents.
5.3.1 Propietats elàstiques i estructura dels polímers
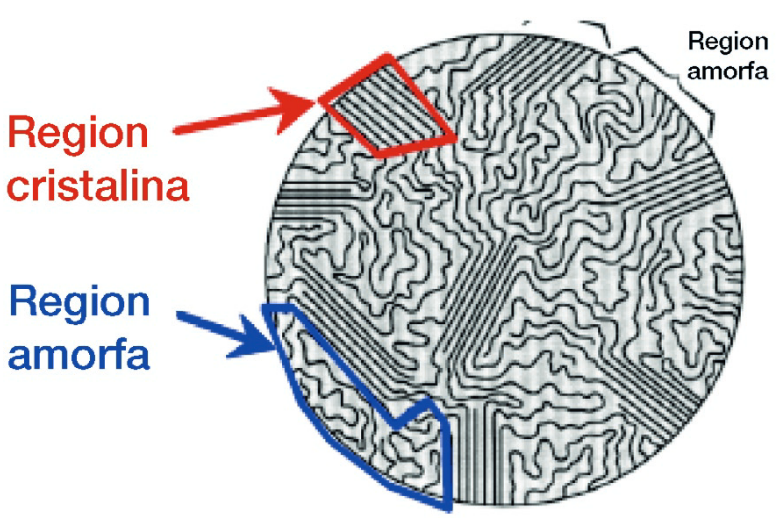
Poden ser molt rígids i resistents, com els policarbonats; tous i duradors, com alguns poliuretans; o elàstics, com els cautxús. També poden ser opacs o transparents. La transparència depèn de l’absorció electrònica del polímer i de la dispersió de la llum. Els dominis cristal·lins, additius o buits poden dispersar la llum i fer opac un material, mentre que molts polímers amorfs i homogenis són transparents[6, 8].
Abans de comparar les tres grans famílies de la Figura 5.2, convé aclarir alguns termes. Un polímer lineal no té per què ser una cadena recta, sinó una macromolècula sense ponts covalents permanents amb altres cadenes. Un polímer entrecreuat sí que conté aquests ponts, i per això no es pot dissoldre ni fondre de la mateixa manera que un termoplàstic. Quan un elastòmer s’infla en un dissolvent, el líquid penetra a la xarxa i separa parcialment les cadenes, però la xarxa covalent impedeix que el material es dissolgui completament.
Rigidesa, resistència i deformació
La rigidesa és l’oposició del material a deformar-se dins la zona elàstica. Es mesura amb el mòdul de Young , que correspon al pendent inicial d’una corba tensió-deformació. Com més gran és
, menys s’allarga o es doblega el material sota la mateixa tensió. Aquest mateix mòdul es farà servir més endavant per descriure fibres, matrius i direccions de càrrega en materials compostos.
La resistència mecànica indica la tensió que un material pot suportar abans de deformar-se permanentment o trencar-se. No és el mateix que la rigidesa. Un material pot ser molt rígid i alhora fràgil si només admet una deformació petita abans de la ruptura.
La deformació és l’allargament relatiu,
, i sovint s’expressa en percentatge. Una
de pocs punts percentuals és típica de materials rígids o fràgils, mentre que molts elastòmers poden arribar a deformacions de centenars per cent i recuperar la forma si no se supera el límit elàstic. A la figura,
significa que els dominis amorfs es troben per sota de la transició vítria i les cadenes tenen molt poca mobilitat segmentària[7, 8].
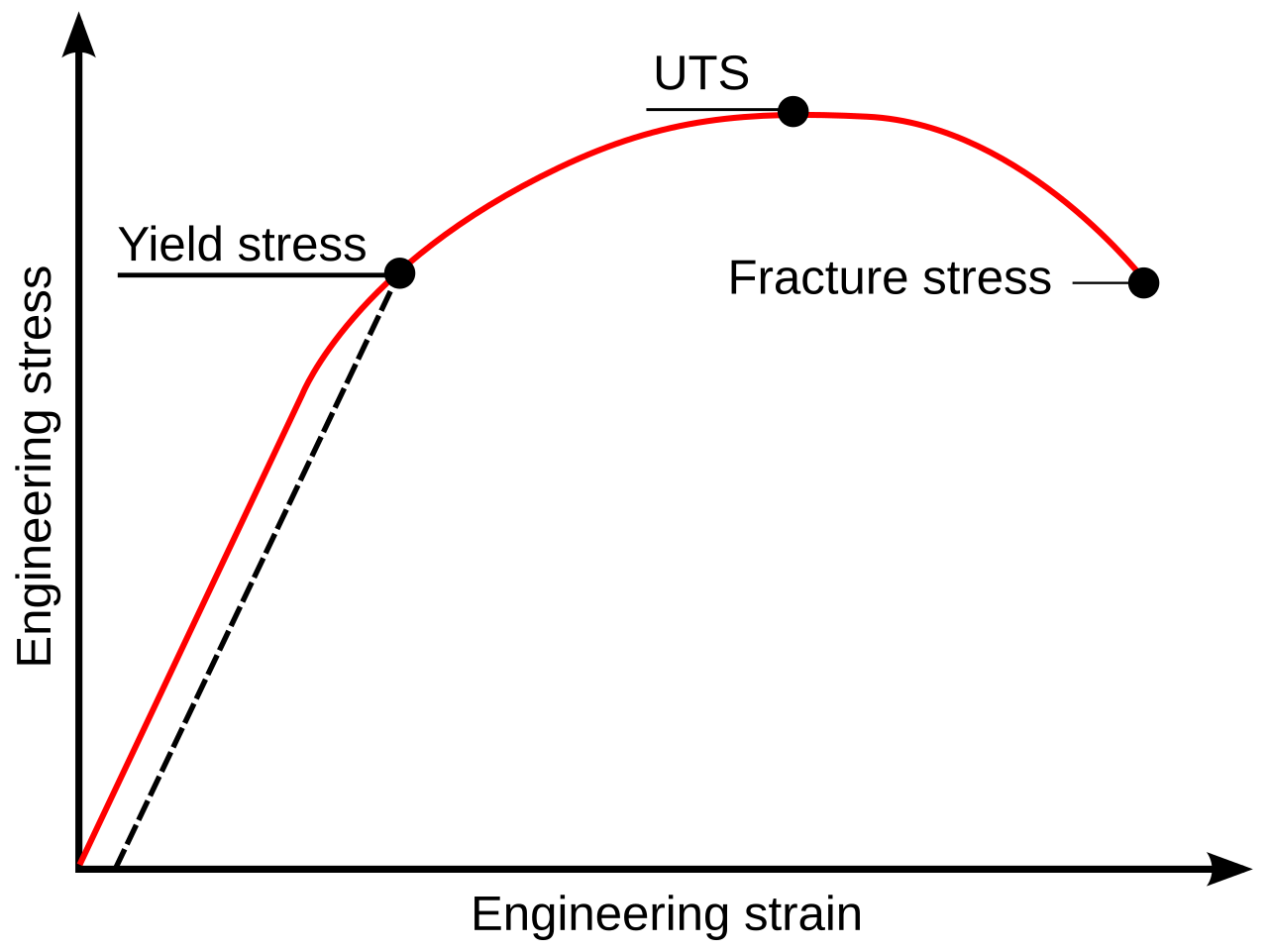
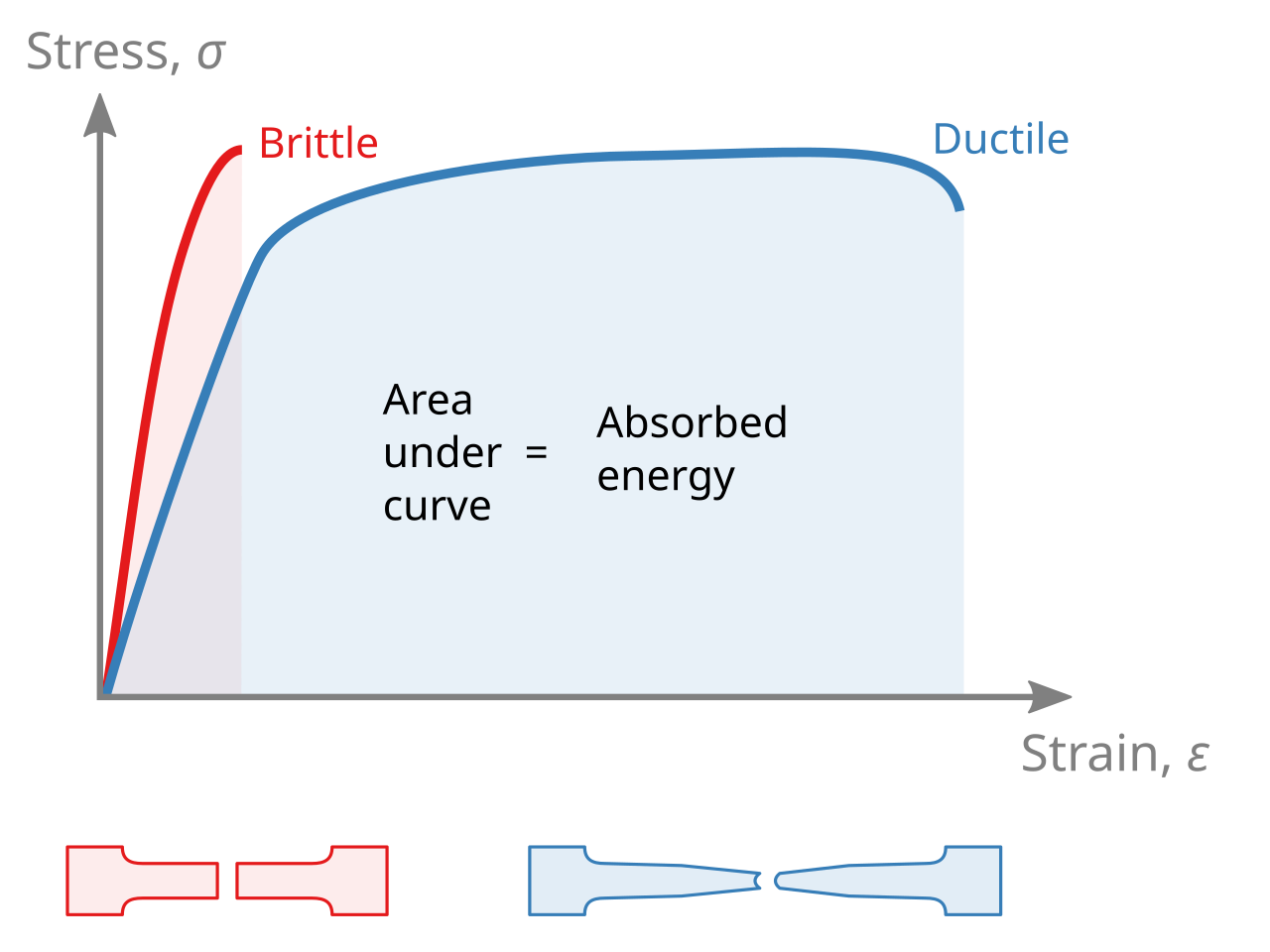
La Figura 5.1 situa aquests conceptes sobre corbes tensió–deformació. El pendent inicial correspon a la rigidesa, els màxims o punts característics de tensió informen sobre la resistència i l’allargament horitzontal abans de la ruptura indica la deformació admissible.
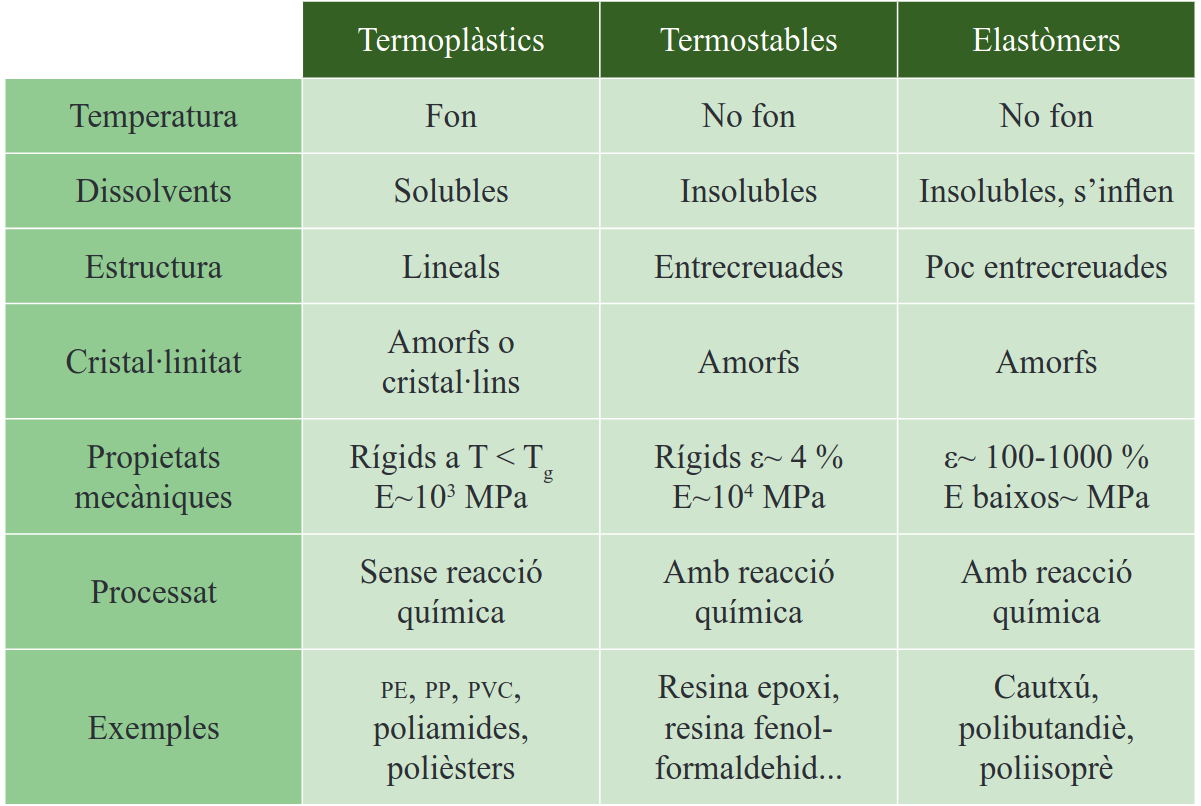
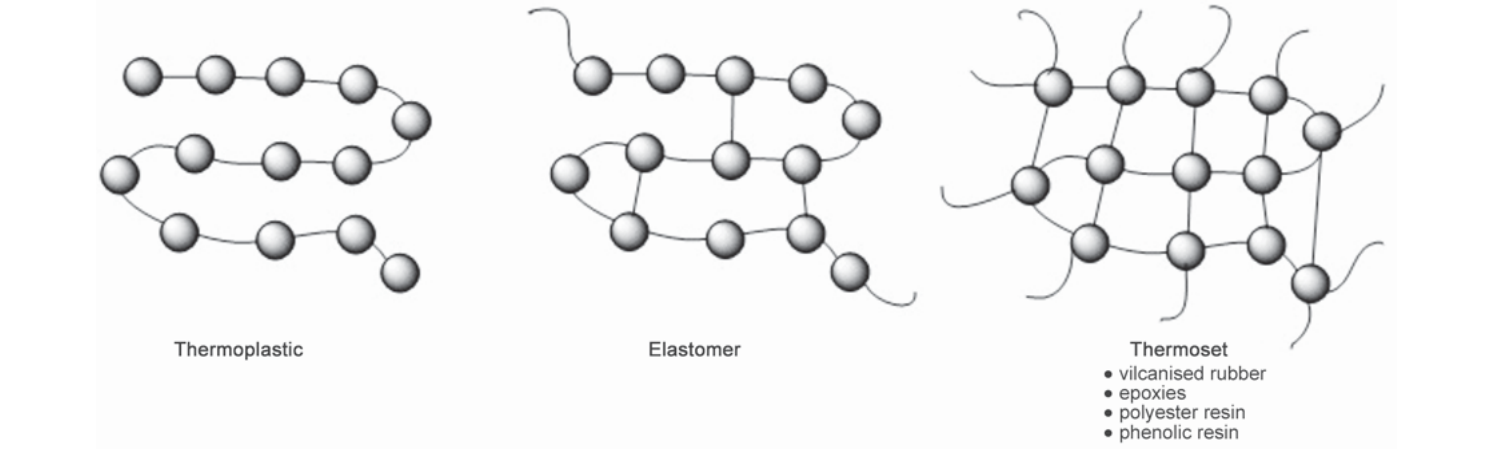
Les diferències principals entre termoplàstics, termoestables i elastòmers es resumeixen a la Figura 5.2.
Per llegir correctament la Figura 5.2, convé associar cada família amb el tipus d’enllaç entre cadenes i amb la resposta mecànica esperada.
-
• Termoplàstic. Està format per cadenes lineals o ramificades unides sobretot per forces intermoleculars, no per una xarxa covalent permanent. En escalfar-lo s’estova o fon i es pot tornar a conformar; per això és adequat per a injecció, extrusió i reciclatge mecànic. A la figura correspon a materials que poden tenir rigidesa i resistència moderades o altes, però que mantenen certa capacitat de deformació abans de trencar.
-
• Termoestable. Durant el curat forma una xarxa tridimensional d’enllaços covalents entre cadenes. Un cop curat, no fon de nou i es degrada químicament si s’escalfa massa. Aquesta xarxa explica que acostumi a ser rígid, dimensionalment estable i resistent a temperatura, però amb poca deformació admissible i comportament més fràgil que molts termoplàstics.
-
• Elastòmer. És una xarxa polimèrica amb pocs entrecreuaments, prou separats per permetre grans deformacions reversibles. Les cadenes es poden desenrotllar i reordenar quan s’estiren, però els entrecreuaments impedeixen que flueixin permanentment. A la figura es reconeix per un mòdul
molt baix i una deformació
molt alta, típica de cautxús, juntes i pneumàtics.
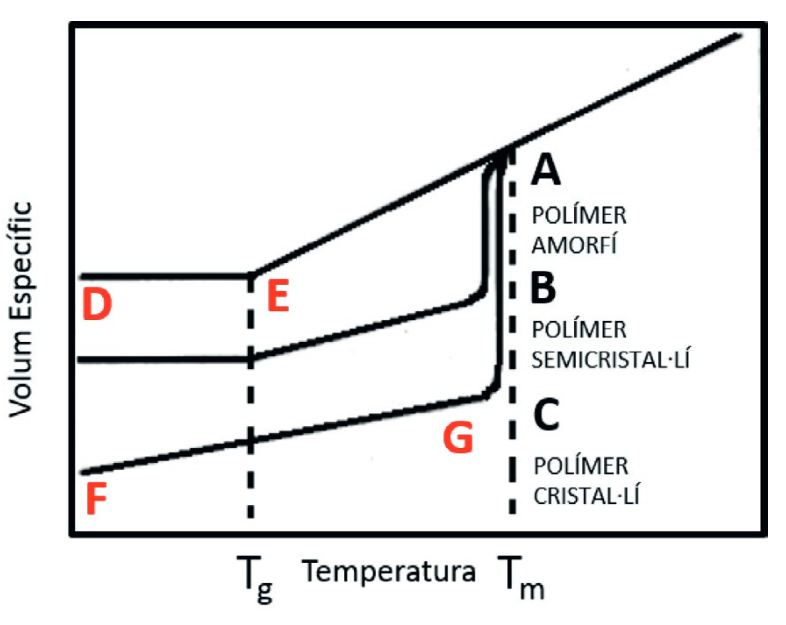
Entre els inconvenients dels polímers hi ha una resistència menor a altes temperatures que molts metalls, fluència sota càrrega sostinguda, sensibilitat a dissolvents concrets i degradació per radiació ultraviolada, oxidació o hidròlisi. El baix cost, la lleugeresa i la facilitat de processament solen compensar aquestes limitacions si es tria bé la formulació. Hi ha dos paràmetres especialment importants (Figura 5.4)[8].
-
• La temperatura de fusió (
) és la temperatura a la qual els dominis cristal·lins perden l’ordre. Només té sentit en polímers cristal·lins o semicristal·lins; un polímer completament amorf no presenta una fusió definida.
-
• La temperatura de transició vítria (
) és la temperatura per sota de la qual els dominis amorfs perden mobilitat segmentària i el material passa a comportar-se com un vidre rígid. Per sobre de
, les cadenes poden reordenar-se localment i el material és més flexible.
Interpretació de la transició vítria
La transició vítria és un canvi gradual propi dels materials amorfs, o de la part amorfa d’un polímer semicristal·lí. En escalfar, el material passa d’un estat dur, rígid i sovint fràgil a un estat més tou, viscós o gomós. En refredar, la mobilitat molecular es va alentint fins que l’estructura queda “congelada” en una configuració desordenada. Per això un vidre o un polímer amorf no és un cristall mal format, sinó un sòlid sense ordre de llarg abast que conserva part del desordre d’un líquid molt viscós.
no s’ha d’interpretar com una temperatura de fusió. A
es desfan dominis cristal·lins i apareix un canvi de fase amb un salt clar de propietats. A
, en canvi, no desapareix cap xarxa cristal·lina perquè la regió afectada ja és amorfa. El que canvia és el temps que necessiten els segments de cadena per reordenar-se. Per sota de
, aquests moviments són massa lents a l’escala de l’ús del material; per sobre de
, els segments poden explorar configuracions noves i el material admet deformacions més grans.
Per aquest motiu, és més aviat un interval que no pas un punt exacte. El valor mesurat depèn de la velocitat d’escalfament o refredament, de la història tèrmica, del pes molecular, dels additius i de la humitat. Experimentalment es detecta com un canvi de pendent en el volum específic o en l’expansió tèrmica, i també
com un canvi en la capacitat calorífica en calorimetria. La Figura 5.4 ho representa amb el canvi de pendent de la corba amorfa.
En la pràctica, cal comparar la temperatura de servei amb . Un PC o un PMMA treballen com a plàstics rígids i transparents quan estan per sota de
; un elastòmer de pneumàtic, en canvi, ha de treballar per sobre de
per mantenir flexibilitat i adaptar-se a la rugositat del paviment. Els entrecreuaments d’un cautxú vulcanitzat impedeixen que les cadenes flueixin com un líquid, però no eliminen la transició vítria. La seva funció és fixar una xarxa que pot ser gomosa per sobre de
i dura per sota d’aquest valor[7, 8].
També es poden classificar segons la seva arquitectura molecular[8].
-
• Grau de polimerització. Segons les condicions de síntesi es poden obtenir cadenes de longitud diferent i, per tant, pesos moleculars i propietats mecàniques diferents.
-
• Copolímers. Són polímers formats per més d’un tipus de monòmer. Segons l’ordre de repetició, es distingeixen diferents casos.
-
– Alternats, (-A-B-A-B-)
-
– Periòdics, (A-B-B-A-B-A-A-A-B)
-
– Estadístics, amb una probabilitat determinada de repetició
-
– Aleatoris, sense ordre de repetició
-
– Per blocs, (A-A-A-B-B-B-A-A)
Els copolímers són freqüents en els pneumàtics i altres components elàstics (veure Secció 5.5).
-
-
• Ramificació. Són cadenes laterals unides a una cadena principal. En el polietilè, per exemple, una ramificació elevada dificulta l’empaquetament de les cadenes i redueix la cristallinitat; per això el LDPE és més flexible que l’HDPE.
-
• Entrecreuament. Són ponts covalents entre cadenes. Un exemple clàssic és la vulcanització del cautxú amb sofre. El cautxú natural és el cis-poliisoprè; quan s’afegeix sofre en proporcions baixes es formen ponts entre cadenes que augmenten resistència, elasticitat útil i resistència al desgast. Amb percentatges molt elevats de sofre s’obté ebonita, un sòlid dur i rígid.
Un cop distingides les famílies principals de polímers, el pas següent és entendre com es formen les cadenes. La polimerització determina l’arquitectura molecular inicial i ajuda a explicar per què alguns materials es poden fondre i reprocessar, mentre que altres es curen fins a formar xarxes permanents o estructures elàstiques.
5.3.2 Polimerització
La polimerització és el procés químic pel qual els monòmers s’uneixen per formar macromolècules. Per a aquest curs és suficient distingir dos mecanismes generals, la polimerització per etapes i la polimerització en cadena. La diferència és important perquè condiciona el pes molecular, el tipus d’enllaç de la cadena i, per tant, la manera de reciclar, degradar o processar el material[1, 8].
Clau per identificar el mecanisme de polimerització
La primera pregunta és si el monòmer té un centre reactiu que creix sempre a l’extrem d’una cadena activa, sovint un doble enllaç . Si és així, el cas habitual és una polimerització en cadena, també anomenada polimerització per addició.
Si el que reaccionen són grups funcionals de molècules difuncionals o polifuncionals, com ,
,
, carbonats o isocianats, el cas habitual és una polimerització per etapes. Pot anar acompanyada de l’eliminació d’una molècula petita, com aigua o metanol, però no sempre. Per això convé reservar el terme condensació per als casos en què aquesta molècula petita s’allibera
realment.
La lectura pràctica és que les polimeritzacions en cadena generen cadenes llargues molt aviat, mentre que les polimeritzacions per etapes necessiten conversions molt altes per arribar a pesos moleculars elevats.
5.3.2.1 Polimerització per etapes
En la polimerització per etapes, qualsevol molècula amb grups funcionals reactius pot unir-se amb qualsevol altra, ja sigui monòmer amb monòmer, monòmer amb oligòmer o oligòmer amb oligòmer. El monòmer es consumeix aviat, però el pes molecular elevat només s’assoleix quan la conversió és molt alta. Moltes d’aquestes reaccions són de condensació. En formar-se l’enllaç del polímer s’allibera una molècula petita, sovint aigua o metanol. És el cas de polièsters i poliamides. Altres polimeritzacions per etapes, com alguns poliuretans, no alliberen necessàriament cap molècula petita; per això és més precís parlar de polimerització per etapes i no identificar-la sempre amb condensació.
Poliacetals i polièters No tots els polímers tècnics d’automoció encaixen còmodament en l’esquema simple “polièster, poliamida o polímer vinílic”. El polioximetilè (POM), també anomenat acetal o poliacetal, té una cadena principal amb unitats repetitives . Es pot obtenir a partir de formaldehid o de trioxà, i es classifica com a termoplàstic tècnic semicristal·lí. La presència regular d’enllaços C–O a l’esquelet afavoreix un empaquetament ordenat i una superfície de baixa fricció; per això és adequat per a engranatges petits, clips, guies i peces de precisió
on cal estabilitat dimensional i resistència al desgast[20, 8].
La Figura 5.5 compara estructures representatives de polímers de condensació.
La Figura 5.6 mostra exemples de polímers formats per polimerització per etapes.
Poliamides (Nylons) La primera fibra polimèrica totalment sintètica, el niló-6,6, va ser produïda l’any 1938 per la companyia DuPont. El químic principal de l’equip era Wallace H. Carothers, que va raonar que algunes propietats de la seda podien imitar-se construint una cadena polimèrica formada per enllaços amida repetits, tal com passa amb les proteïnes de la seda[1].
El niló-6,6 es crea a partir de la reacció entre l’ (àcid adípic o 1,6-hexandioic) i l’
(1,6-hexandiamina), que donen lloc a una sal que, un cop escalfada, forma múltiples enllaços amida mitjançant una substitució acil nucleòfila. El producte és una poliamida anomenada niló-6,6. Els números del nom fan referència al nombre de carbonis en cada monòmer. El
primer “6” indica els carbonis de la diamina, i el segon “6”, els del diàcid. Variant el nombre de carbonis en cada monòmer es poden obtenir molts tipus de nylons diferents.
Els nylons són entre les fibres sintètiques més utilitzades. S’empren en cordes, veles, catifes, roba, reforç de pneumàtics, raspalls i paracaigudes. També poden ser modelats en blocs per a equips elèctrics, engranatges, coixinets i vàlvules. La seva resistència deriva en part de la capacitat de formar enllaços d’hidrogen entre cadenes; la mateixa interacció que dona cohesió a moltes proteïnes.
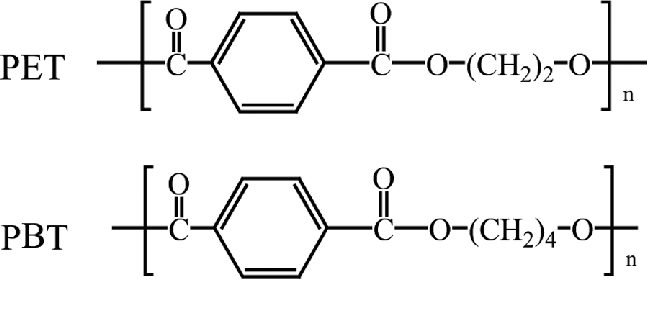
Polièsters Els enllaços èster també poden formar-se mitjançant substitucions acil nucleòfiles, com a mecanisme principal en els polímers per creixement per etapes. Un polièster es produeix típicament per la reacció entre un diàcid i un diol (Figura 5.6). El producte inicial conté un grup àcid lliure () a un extrem i un grup alcohol lliure (
) a l’altre. Mitjançant reaccions successives d’esterificació, es forma el polièster. El PET es genera amb la reacció entre l’àcid tereftàlic (
) i l’etilenglicol (
). De manera simplificada, es pot representar amb l’equació següent.
Les molècules de polièster són excel·lents per a la producció de fibres i films. Dues de les més comunes són el politereftalat d’etilè (PET) i el politereftalat de butilè (PBT). Tots dos són polímers semicristal·lins amb bona resistència química i mecànica, a més d’una estabilitat tèrmica adequada per a peces tècniques[1, 20]. En automoció, el PBT és especialment útil en connectors i carcasses perquè absorbeix poca humitat i manté millor la dimensió que altres polímers en ambients calents.
Aplicacions del politereftalat d’etilè (PET)-
• Envasos i tèxtils. El PET és àmpliament conegut per l’ús en la indústria de l’embalatge, especialment en ampolles de plàstic i recipients per aliments, per la seva resistència, transparència i durabilitat. També és el material principal en fibres sintètiques com el polièster, utilitzades en roba i tapisseria.
-
• Electrònica. Tot i que el PBT és més habitual en components de precisió, el PET també s’utilitza en aplicacions que requereixen transparència o alta resistència mecànica, com films protectors o carcasses. Es transforma en films com el Mylar. Quan es recobreix magnèticament, la cinta de Mylar s’utilitza en cassets d’àudio i vídeo.
-
• Indústria de l’automòbil. El PBT s’utilitza àmpliament en components automotrius com connectors, sensors i carcasses, gràcies a la seva excel·lent resistència a la calor, als productes químics i a l’estabilitat dimensional.
-
• Electrònica i maquinària industrial. En el sector electrònic, s’empra en connectors, interruptors i altres components de precisió per la seva baixa absorció d’humitat, alta aïllació elèctrica i cristal·lització ràpida. També es fa servir en la fabricació de peces mecàniques com engranatges i coixinets, on cal flexibilitat, resistència al desgast i tenacitat.
Policarbonats Més enllà dels derivats dels àcids carboxílics, qualsevol reacció entre espècies reactives en dues molècules diferents pot usar-se per a la polimerització per etapes. Una variant implica l’ús de monòmers amb grups carbonat.
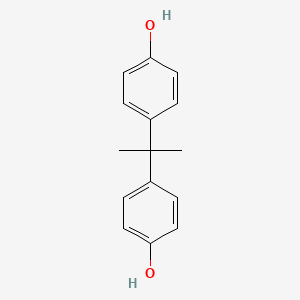
Els carbonats actuen com èsters dobles i poden reaccionar amb dos alcohols mitjançant una doble transesterificació per formar compostos amb grups carbonat. Aquestes molècules difuncionals poden reaccionar amb un diol per formar un polímer amb grups carbonat repetits, anomenat policarbonat. Un exemple és el Lexan, format per la reacció entre carbonat de difenil i bisfenol A, un diol. Els policarbonats són materials resistents, durs i, en alguns graus, òpticament transparents. Són fàcilment treballables, modelables i termoformables. Aquestes propietats els fan útils en aplicacions com discos compactes, DVDs i Blu-ray.
El bisfenol A (BPA), principalment usat per fabricar policarbonat, és un dels compostos químics més produïts al món. A causa de la seva presència en ampolles de plàstic i revestiments d’envasos alimentaris, hi ha preocupacions sobre la migració de BPA als aliments. Un estudi del CDC de 2003–2004 va trobar rastres de BPA en el 93% de les persones analitzades als EUA; aquest tipus de resultats va impulsar la substitució de policarbonats per materials lliures de BPA en algunes aplicacions alimentàries[6].
5.3.2.2 Polimerització en cadena o per addició
La polimerització en cadena s’inicia en un centre reactiu —sovint un radical, però també pot ser catiònic, aniònic o coordinatiu— que afegeix monòmers successivament a l’extrem actiu de la cadena. A diferència de moltes condensacions, no es perd cap molècula petita en cada pas. Les cadenes d’alt pes molecular apareixen molt aviat, encara que la conversió global del monòmer sigui baixa; això contrasta amb la polimerització per etapes, on cal una conversió gairebé completa per obtenir pesos moleculars elevats. Es coneixen també com a polimeritzacions per addició (Taula 5.4).
En molts polímers d’addició, els monòmers contenen un enllaç doble . El mecanisme radicalari general inclou els passos següents.
Iniciació per ruptura homolítica de l’enllaç doble.
Propagació
Terminació
on M és un monòmer genèric, I és l’iniciador, i els radicals lliures es representen amb punts. La iniciació inclou la formació de radicals i la seva reacció amb monòmers per generar radicals de monòmers. La propagació implica la reacció d’aquests radicals amb més monòmers. La terminació representa la pèrdua del radical actiu, bé per combinació de radicals o per transferència del radical a un altre monòmer.
Polímers habituals formats per aquest mètode i utilitzats en l’automoció inclouen polietilè, polipropilè, clorur de polivinil (PVC) i polimetilmetacrilat (PMMA). El panell dret de la Figura ?? mostra estructures químiques representatives d’aquest grup i d’altres polímers ja descrits.
5.3.3 Conformat dels polímers
Una vegada sintetitzat el polímer, el conformat dona la geometria final de la peça. El procés depèn sobretot de si el material és termoplàstic, termoestable o elastòmer. Els termoplàstics es poden escalfar, estovar o fondre i tornar a conformar; en polímers amorfs cal treballar per sobre de , mentre que en semicristal·lins sovint cal acostar-se o superar
. Els termoestables, en canvi, formen una xarxa covalent durant el curat i no es poden fondre de nou sense degradar-se[8].
La conformació dels polímers termoestables es duu a terme en dues etapes.
-
1. Es prepara un polímer lineal (de vegades denominat prepolímer) en fase líquida de baix punt de fusió i s’introdueix en un motlle d’una manera determinada.
-
2. S’endureix el polímer, un procés conegut com a curat, per escalfament, afegint-hi un catalitzador, o sota pressió. Durant el curat hi ha reaccions químiques i estructurals en què s’entrecreuen les cadenes polimèriques i augmenten molt les interaccions intermoleculars (entre cadenes) de naturalesa covalent. Després del curat, es treuen del motlle (encara calent) ja que aquests polímers són estables dimensionalment, no canvien molt de grandària amb la temperatura i, per descomptat, molt menys que els termoplàstics.
Les tècniques més comunes d’emmotllament i conformat són les següents.
-
• En la compressió, s’aplica pressió al polímer calent, en estat semipastós o parcialment fos, fins que adquireix la forma del motlle.
-
• En la injecció, el polímer granulat es fon fins a obtenir un fluid viscós i s’injecta en una cavitat. És molt utilitzada perquè permet cicles ràpids i peces complexes, com connectors, clips, carcasses i components d’interior.
-
• En l’extrusió, el polímer fos és empès de manera contínua, habitualment amb un cargol sense fi, a través d’una filera amb la secció desitjada. És adequada per fabricar perfils, tubs, làmines, films, recobriments de cables i preformes que després es poden tallar, refredar o transformar en una etapa posterior.
-
• En el bufament, primer es genera una preforma tubular o una preforma injectada; després es tanca dins un motlle i s’hi injecta aire a pressió perquè les parets adoptin la forma final. És adequada per a cossos buits, com dipòsits i recipients.
-
• En la colada, el material fluid es diposita en un motlle i, en solidificar o curar, adquireix la forma del recipient.
Per fabricar peces plàstiques d’automòbil, el polímer ja produït arriba com a grànuls durs o perles de resina. Sovint ja contenen agents colorants o additius.
5.4 Materials compostos
Els compostos són materials formats per dues o més fases amb funcions diferents. La matriu dona forma, protegeix i transfereix càrrega, mentre que el reforç aporta rigidesa, resistència o una propietat funcional. En automoció n’hi ha molts, com pastilles de fre, fibra de vidre en panells lleugers, fibres de carboni en peces estructurals, vidre laminat de seguretat i dipòsits d’hidrogen de tipus III i IV. La propietat clau és que el conjunt pot tenir una resistència específica superior a la de cada component per separat, sempre que la interfície entre fases sigui bona[21, 4].
Mòduls elàstics en un compòsit unidireccional
El mòdul de Young introduït a la Secció 5.3.1 també s’utilitza per descriure compòsits, però cal indicar de quin component o de quina direcció de càrrega es parla. En un compòsit reforçat amb fibres alineades, les propietats dels components no coincideixen necessàriament amb les propietats del material final[11].
-
•
és el mòdul de la fibra (fiber), que normalment és la fase més rígida.
-
•
és el mòdul de la matriu, per exemple una resina epoxi o un polímer.
-
•
és el mòdul longitudinal del compòsit, mesurat amb la càrrega parall·lela a les fibres.
-
•
és el mòdul transversal del compòsit, mesurat amb la càrrega perpendicular a les fibres.
Per tant, i
descriuen fases individuals, mentre que
i
descriuen el material compost final. Si
i
són les fraccions en volum de fibra i matriu, amb
si no hi ha porositat, el model longitudinal idealitzat assumeix la mateixa deformació en fibra i matriu i dona
Per a la direcció transversal, una estimació simple de límit inferior assumeix una situació de tensió comuna i s’escriu amb la regla inversa de mescles.
Aquesta segona expressió és útil per fer estimacions ràpides, però no substitueix models micromecànics més complets quan cal predir amb precisió el mòdul transversal. En qualsevol cas, reflecteix l’anisotropia del compòsit, ja que el material sol ser molt més rígid en direcció longitudinal que en direcció transversal quan les fibres són molt més rígides que la matriu.
En lloc de centrar-nos en els avantatges i desavantatges mecànics d’aquests compostos i les seves aplicacions, aquesta secció es focalitza en la química de fabricació dels materials. La fibra de vidre és un compost que conté fibres de vidre incrustades en una matriu polimèrica, habitualment un polímer que, per si sol, seria fràgil o es trencaria sense deformar-se sota estrès. Quan es forma una esquerda, aquesta es propaga fàcilment a través del polímer fràgil. No obstant això, si aquest polímer conté fibres resistents de vidre, és probable que l’esquerda xoqui contra una fibra i no es pugui propagar més. Així, les fibres ajuden a evitar un col·lapse catastròfic sota estrès moderat. Alhora, les fibres de vidre aporten resistència i una certa flexibilitat al polímer originalment fràgil. Tot i així, sota un estrès molt elevat, els panells de fibra de vidre es trenquen en petits fragments, dissipant millor l’energia d’un impacte, un avantatge important per a aplicacions de competició.
Com la majoria de vidres, les fibres de vidre emprades en aquests compostos són habitualment de sílice (SiO), tot i que sovint es barregen amb altres materials inorgànics per reduir la temperatura de treball i millorar la resistència química als àcids o als àlcalis. El tipus més comú de vidre és l’anomenat E-glass, patentat per Owens-Corning el 1943. Es tracta d’un vidre d’aluminoborosilicat format per una
mescla d’òxids de sílice, bor, calci, magnesi i alumini. Aquesta mescla fosa s’extrudeix a través de boquilles estretes per formar fibres. Aquestes fibres es poden teixir o tallar en segments curts; aquest darrer format és el més utilitzat en aplicacions automotrius.
La matriu polimèrica de la fibra de vidre pot estar composta de materials com polivinil, poliestirè, acrilats d’èster o metilmetacrilats, o resines d’acrilonitril. També s’empren polímers de condensació com policarbonats, polièsters i òxids de polifenilè. El polímer escollit ha de tenir una forta adhesió a les fibres de vidre, la qual cosa implica (a) formació d’interaccions intermoleculars amb els grups funcionals superficials d’òxid i hidròxid del vidre, i (b) omplir fàcilment els espais entre fibres, evitant la formació de buits que podrien debilitar el material compost.
Normalment, la matriu i les fibres es combinen amb solvents per formar una pasta viscosa que es pot aplicar amb pinzell o modelar i escalfar per eliminar el solvent i curar el polímer, produint un panell sòlid compost.
Els compostos de fibra de carboni representen una altra classe de materials amb aplicacions comercials en el sector automobilístic i un ús extensiu en vehicles de competició. També són compostos polimèrics reforçats amb fibres. En general, ofereixen avantatges similars als de les fibres de vidre, però amb diferències clau. La fibra de carboni té densitat més baixa i rigidesa específica més alta que moltes fibres de vidre, i pot interaccionar millor amb matrius orgàniques si la superfície ha estat oxidada o funcionalitzada de manera controlada. Tant les fibres de carboni com les de vidre tenen gran resistència a tracció; el repte químic és transferir aquesta càrrega des de la matriu fins a la fibra sense que la interfície falli.
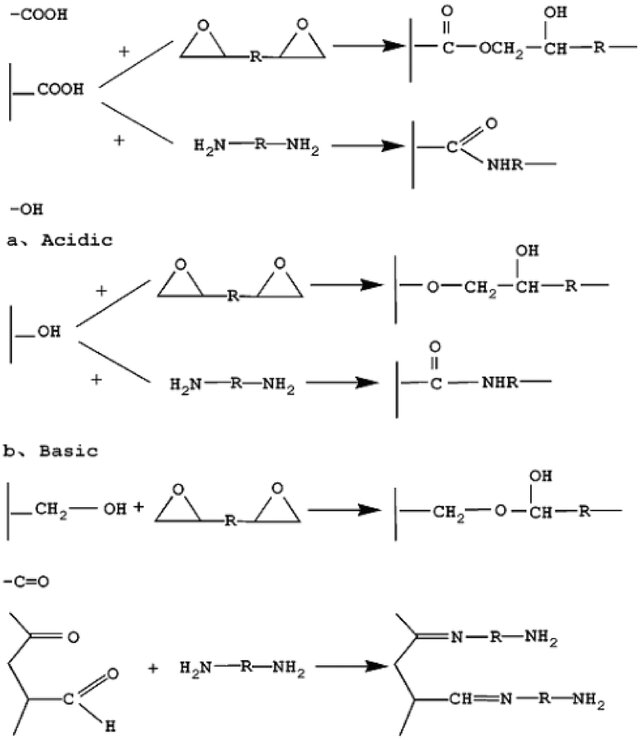
La majoria de fibres de carboni es fabriquen estirant poliacrilonitril o brea fosa de manera similar al procés industrial de les fibres de vidre. En la majoria d’estructures automobilístiques, les fibres es teixeixen en làmines que s’impregnen amb una matriu polimèrica, normalment una resina epoxi que conté el grup funcional epòxid. Aquestes resines, com les resines fenòliques i les novolacs, es curen mitjançant un agent enduridor que obre l’anell epòxid i permet la formació d’enllaços entre monòmers. Els agents curatius més comuns són amines o alcohols (Figura 5.8). Dissolent la resina en un solvent adequat es redueix la viscositat, facilitant la impregnació de les làmines de fibra. Aquestes es poden apilar, modelar i escalfar per completar el procés de curat.
Xassís monocasc Els primers vehicles tenien bastidors d’acer soldats que actuaven com a suport estructural. Amb el temps, la tecnologia ha evolucionat cap a dissenys més avançats i segurs gràcies a nous materials estructurals. El màxim exponent d’aquesta evolució és el xassís monocasc de fibra de carboni. En un monocasc, la pell exterior del vehicle forma part del suport estructural, eliminant la necessitat de penjar panells de carrosseria. Això redueix el pes i millora la seguretat. En cas de col·lisió, els panells exteriors absorbeixen i dissipen millor l’energia que els sistemes tradicionals amb panells units només per punts de contacte. Tot i que un monocasc d’acer seria massa pesat per a competició, un de fibra de carboni ofereix una resistència similar amb un pes molt inferior. Actualment s’utilitzen en cotxes de competició com el xassís DW12 d’IndyCar i en cotxes esportius d’alta gamma com el McLaren F1 o el Lamborghini Aventador.
Vidre laminat de seguretat El vidre de les finestres dels automòbils és també un material compost, conegut com a compost laminat. Cal combinar una elevada resistència a l’impacte amb rigidesa i una transparència pràcticament total. Tant el vidre com el policarbonat són materials adequats, però poden trencar-se de manera fràgil sota impactes forts, generant fragments perillosos. Enlaminant vidre o policarbonat amb un polímer flexible, durador i transparent, s’aconsegueix que el polímer absorbeixi part de l’energia i mantingui les làmines unides. Els polímers utilitzats són habitualment resina de polivinil butiral, uretans alifàtics o làmines de resina transparent curada. Químicament, contenen grups hidroxil i oxigen que formen interaccions fortes amb les funcionalitats del vidre o policarbonat i poden establir enllaços químics durant el procés d’unió.
Discs d’embragatge Els discs d’embragatge són compostos molt més complexos que els polimèrics reforçats amb fibra o els compostos laminats. Són similars a les pastilles de fre pel que fa a la funció. Han de generar fricció elevada quan cal, baixa fricció i resistència quan no s’utilitzen, i ajudar a circular un líquid refrigerant. En transmissions tancades, aquest líquid és el fluid de transmissió. Els discs solen tenir canals per facilitar la circulació del líquid. Si massa lubricant quedés atrapat entre els discs i els engranatges, l’embragatge lliscaria. Els materials de fricció estan formats per fibres orgàniques, càrregues inorgàniques, modificadors de fricció, polímers com cautxú làtex, i una resina polimèrica que actua com a aglutinant. La química esdevé crucial en el curat de la resina, quan el solvent s’evapora i es produeix la polimerització. En alguns casos també hi intervé química de galvanització.
5.5 Elastòmers i cautxú
Els cotxes utilitzen cautxú als pneumàtics, mànegues, a la superfície dels pedals, com a juntes per evitar l’entrada d’aigua al vehicle, a les fulles dels eixugaparabrises i en altres aplicacions. Alguns d’aquests cautxús són molt durs, com els que es poden trobar a la suspensió, mentre que d’altres són tous i fàcilment flexibles, com les juntes de les portes i les fulles dels eixugaparabrises. Alguns components tenen fibres trenades o altres materials estructurals intercalats entre capes de cautxú, per exemple, les cintes d’acer i fibra dels pneumàtics. L’adhesió del cautxú a altres materials així com les seves propietats físiques (elasticitat, resistència tèrmica, amortiment, abrasió, etc.) depenen en gran mesura de la formulació química[6].
Els cautxús naturals són làtex de poliisoprè produïts per alguns arbres i altres plantes. Un làtex és una suspensió estable de micropartícules de polímer (amb diàmetres de 100 nm a 100 µm), tot i que en anglès comú, làtex s’ha convertit en sinònim del terme general cautxú. Els làtex naturals sovint són líquids enganxosos i lletosos que varien de color entre blanc pur i marró clar. Com que provenen d’organismes biològics, contenen sucres, proteïnes i altres biomolècules vegetals comunes juntament amb poliisoprè en un dissolvent d’aigua. Quan es deshidrata el làtex, les micropartícules de cautxú coagulen i formen un sòlid feble i tou amb alta elasticitat i resistència a fractures fràgils.
Els làtexs sintètics també es produeixen industrialment, i en aquests materials el polímer orgànic és d’origen petroquímic o sintetitzat a partir de matèries primeres naturals. Els polímers de làtex sintètics comuns inclouen el cautxú estirè-butadè (SBR), polímers acrílics i acetat de polivinil. La indústria del cautxú combina polímers, agents de curat, farciments, plastificants, antioxidants i agents d’adhesió; per això un pneumàtic és més aviat una formulació química complexa que no pas un sol polímer.
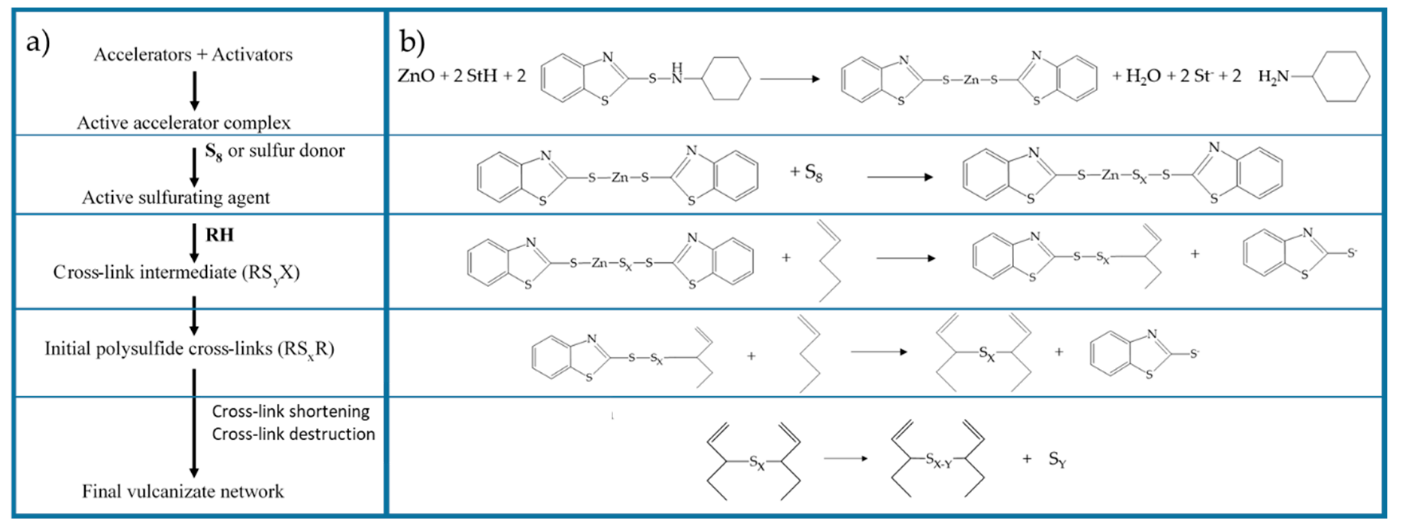
Molts cautxús naturals i sintètics contenen enllaços carboni-carboni insaturats (C=C), importants per la reactivitat i per les reaccions de curat. No tots els elastòmers depenen d’aquesta insaturació; els cautxús de silicona, per exemple, tenen una cadena principal . Des d’una perspectiva automotriu, la química més important del cautxú és la vulcanització (Figura 5.9). La vulcanització fa els cautxús més resistents a la deformació permanent i a la calor promovent la formació d’enllaços
químics entre cadenes, els anomenats enllaços creuats (cross-links)[18].
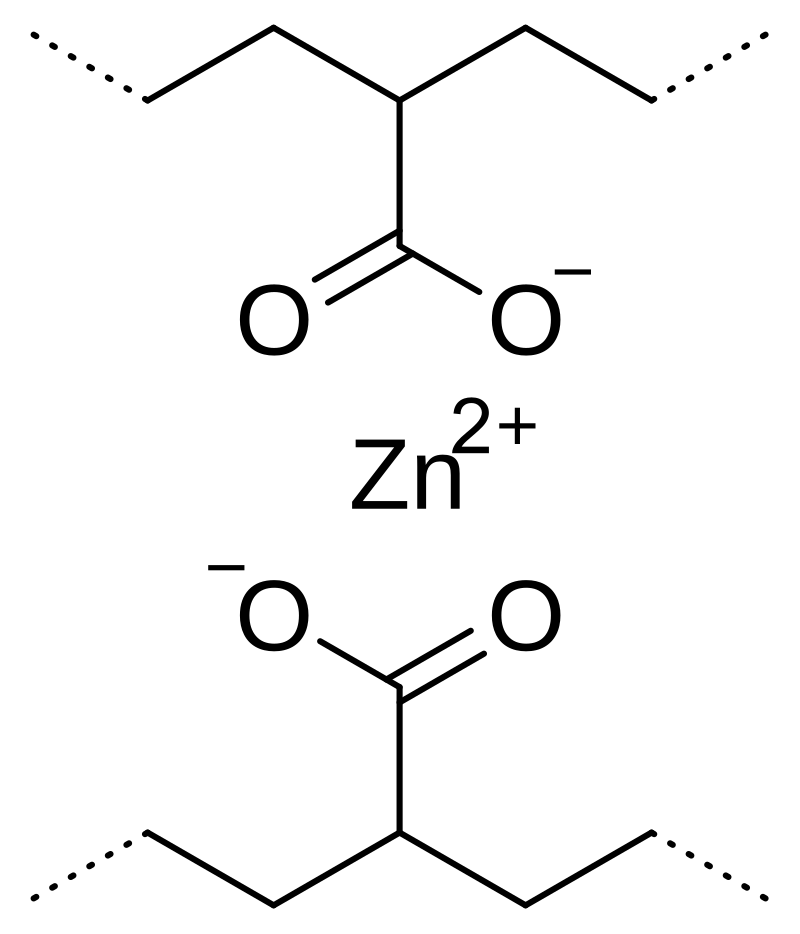
L’agent vulcanitzant clàssic per al cautxú natural és el sofre combinat amb calor elevada, tot i que també es poden utilitzar altres curatius químics que contenen sofre (com els sulfenàmids). La vulcanització amb sofre pur és molt lenta, i per això, els agents vulcanitzants es combinen amb acceleradors químics per augmentar la velocitat del procés fins a un ritme industrialment acceptable. Els acceleradors inclouen òxid de zinc i àcid esteàric, tot i que qualsevol substància que pugui obrir els anells S8 del sofre i trencar els enllaços de la cadena de sofre ajudarà a accelerar el procés. Aquests acceleradors redueixen l’energia d’activació per a la formació d’enllaços creuats oferint un mecanisme alternatiu per a l’obertura dels anells de sofre i la ruptura dels enllaços.
Els enllaços creuats en el procés clàssic de vulcanització amb sofre són cadenes d’àtoms de sofre que enllacen els polímers orgànics. Tot i que existeixen moltes teories sobre el mecanisme químic detallat de la vulcanització amb sofre, sembla clar que la presència d’hidrogen al·lícic és crítica. Un hidrogen al·lícic és aquell unit a un carboni adjacent a un C=C. L’eliminació d’aquest hidrogen, que és el més fàcil d’extreure en un alquè no conjugat, forma un radical polimèric que pot reaccionar amb cadenes de sofre per formar enllaços creuats.
La resistència i la resistència tèrmica del cautxú vulcanitzat depenen del nombre d’àtoms de sofre implicats en l’enllaç creuat. Les cadenes curtes d’enllaç creuat proporcionen millor resistència a la calor gràcies a l’energia d’enllaç més alta, mentre que les cadenes llargues ofereixen més resiliència i flexibilitat perquè permeten major llibertat de moviment de les cadenes polimèriques sota tensió. Existeixen alternatives al sofre com a agents curatius, com els peròxids, òxids metàl·lics i uretans.
Els farciments reforçadors també són modificadors molt importants del cautxú per a automoció i exerceixen una forta influència sobre el seu rendiment. El més utilitzat tradicionalment ha estat el negre de carboni, que també dóna el color negre al cautxú vulcanitzat. Com a sòlid orgànic, la funcionalitat química
de la superfície del negre de carboni facilita la interacció química amb els polímers orgànics del cautxú. Tant els enllaços com
entre el farciment i el polímer proporcionen reforç estructural, mentre que la duresa de les partícules de carboni afavoreix la resistència a l’abrasió i la gestió tèrmica. Així, els negres de carboni petits amb alta àrea superficial que poden formar molts enllaços químics amb el polímer proporcionen els
màxims beneficis.
L’altre farciment més utilitzat en la indústria del cautxú és la sílice. Les partícules de sílice són més dures que el negre de carboni i poden proporcionar més rigidesa i menor resistència al rodament, millorant així l’eficiència del combustible en els pneumàtics “verds” rics en sílice. Els grups funcionals de la
superfície de la sílice són principalment grups hidroxil que no interaccionen fàcilment amb la fase polimèrica, ja que participen més fàcilment en enllaços d’hidrogen o forces intermoleculars de tipus dípol-dípol i ió-dípol. Per això, les superfícies de la sílice sovint es funcionalitzen amb compostos organosilans
més compatibles químicament amb el polímer. Malgrat aquesta funcionalització, les partícules de sílice que es desgasten a la superfície del cautxú poden reexposar els grups hidroxil, cosa que pot millorar la tracció en mullat d’un pneumàtic, així com l’alteració de la , que és l’energia dissipada durant l’estirament en comparació amb l’energia alliberada durant la relaxació.
Tant la sílice precipitada com la sílice fumada s’utilitzen en la indústria del cautxú. No obstant això, la sílice funcionalitzada és actualment molt més cara que el negre de carboni, i aquesta diferència de cost és el principal motiu pel qual el negre de carboni continua sent el farciment de reforç principal en aplicacions automotrius.
5.5.1 Pneumàtics per a cada estació
En climes freds és habitual trobar pneumàtics d’estiu, d’hivern i tot temps. Els d’estiu funcionen bé en condicions càlides, tant en sec com en mullat. Els d’hivern ofereixen màxima tracció amb neu i gel, mentre que els tot temps ofereixen un rendiment raonable tot l’any. Les diferències són tant d’enginyeria (profunditat de canals, arestes angulars, ranures petites) com químiques. Es fan servir diversos elastòmers com cis-1,4-poli butadiè, cis-1,4-poliisoprè, poli(isobutilè-co-isoprè), poli(estirè-co-butadiè), etc. La seva combinació permet ajustar la fricció i resistència al desgast segons la temperatura.
La duresa de la goma depèn de la seva temperatura de transició vítria, . Per sota de
, l’elastòmer s’endureix i perd capacitat d’adaptar-se a la rugositat del paviment; per tant, un pneumàtic d’hivern necessita una formulació amb
prou baixa per continuar sent flexible en fred. Polibutadiè cis-1,4 (
) i poliisoprè natural (
) ajuden en aquest sentit. En canvi, una formulació d’estiu pot prioritzar estabilitat a temperatura elevada i resistència al desgast. El compromís és inevitable. Més flexibilitat en fred sol implicar més desgast i pitjor rendiment quan la temperatura puja.
Pneumàtics verds Actualment, els anuncis de pneumàtics destaquen l’eficiència del combustible i la tecnologia “verda”, però què fa que un pneumàtic sigui “verd”? Hi ha dues estratègies. Una és millorar l’eficiència del combustible reduint la resistència al rodament, cosa que es pot aconseguir substituint part
del negre de carboni per sílice funcionalitzada. Una fracció significativa del combustible consumit per un vehicle es perd superant aquesta resistència, de manera que petites millores en histèresi i poden tenir un efecte acumulat important[6].
L’altra estratègia és produir els blocs de construcció del cautxú a partir de fonts renovables. Actualment, el cautxú per a pneumàtics prové d’espècies vegetals concretes o de combustibles fòssils. També s’han desenvolupat rutes biotecnològiques per obtenir isoprè a partir de sucres; aquest isoprè pot servir per fabricar poliisoprè sintètic.
Cautxús de silicona Una altra classe comuna de cautxú sintètic són els basats en silicona i els segellants d’alta temperatura. Els polímers de cautxú de silicona tenen una estructura principal d’enllaços silici-oxigen (), i grups funcionals orgànics laterals (metil, fenil, etc.). Aquests grups orgànics determinen les propietats físiques i químiques. Ajuden a fer els polímers més resistents a la humitat i solubles en dissolvents orgànics.
Abans del curat, solen ser líquids o gels enganxosos. Els processos de curat inclouen vulcanització o agents de curat com els peròxids. Són ideals per aplicacions d’alta temperatura i es fan servir en mànegues de radiador, juntes, casquets elèctrics, etc.
Envelliment del cautxú Amb el temps, el cautxú es degrada per desgast físic o processos químics.
-
• L’ozó oxida els enllaços C=C, trencant les cadenes polimèriques.
-
• L’oxigen atmosfèric forma enllaços creuats amb oxigen, endurint el material.
-
• La vulcanització continua lentament al llarg del temps.
-
• La llum pot provocar radicals lliures o fotòlisi de l’estructura.
Per prevenir-ho, s’afegeixen antioxidants com amines, compostos fenòlics i organofosfits.
5.6 Materials ceràmics i vidres
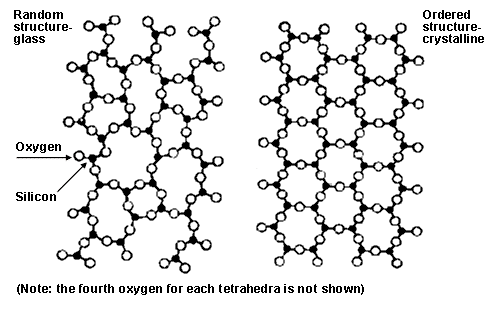
S’anomena material ceràmic tot material d’enginyeria inorgànic i no metàl·lic. Moltes ceràmiques són cristal·lines, amb ions o àtoms ordenats periòdicament; els vidres, en canvi, són sòlids amorfs amb ordre local però sense ordre de llarg abast. Per això un vidre de sílice i una ceràmica de sílice poden tenir
composició química semblant, però una organització microscòpica diferent. En el vidre, els tetraedres formen una xarxa desordenada que queda congelada en refredar el líquid. En una ceràmica cristal·lina, aquests mateixos motius estructurals es repeteixen de manera regular en l’espai. Les vitroceràmiques ocupen una situació intermèdia: es preparen a partir d’un vidre i després es tracten
tèrmicament perquè cristall·litzi una part important del material.
Aquesta diferència estructural no impedeix que vidres i ceràmiques comparteixin propietats generals, com alta duresa, estabilitat química i tèrmica, baixa conductivitat elèctrica en molts casos i fragilitat elevada. La fragilitat s’explica perquè els enllaços iònics/covalents són direccionals o fortament electrostàtics i no permeten la mobilitat de dislocacions que dona ductilitat als metalls[8, 7].
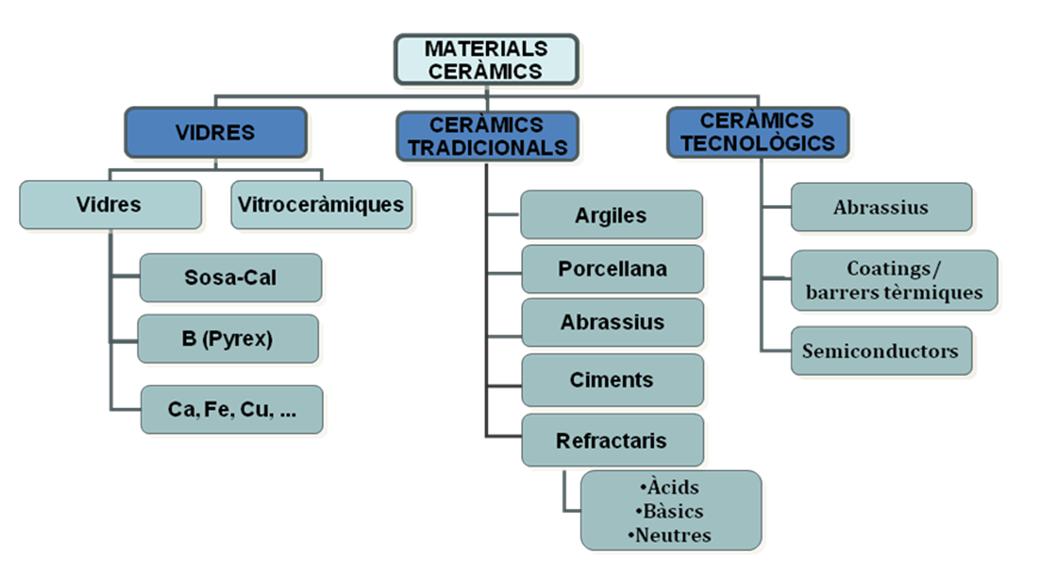
La Figura 5.11 ordena els principals grups de ceràmiques i vidres que es fan servir en enginyeria.
En automoció no s’utilitzen ceràmiques només perquè “resisteixen la temperatura”. També s’aprofiten propietats funcionals com la conductivitat iònica, l’activitat catalítica, la baixa expansió tèrmica, la resistència al desgast o la transparència. Alguns exemples importants són els següents.
-
• El vidre laminat de seguretat combina làmines de vidre amb una capa polimèrica transparent. El vidre aporta rigidesa i resistència a ratllades; el polímer manté fragments units i dissipa energia en impacte.
-
• Les bugies i els aïllants utilitzen alúmina i altres ceràmiques que aïllen elèctricament i resisteixen temperatura, vibració i atac químic dins el motor.
-
• En els catalitzadors de tres vies, el suport ceràmic, sovint de cordierita amb estructura de bresca, proporciona gran superfície i baixa pèrdua de càrrega; a sobre hi ha una capa porosa (washcoat) d’òxids com
,
i
que dispersa metalls catalítics com Pt, Pd o Rh.
-
• Moltes sondes lambda es basen en zircona estabilitzada amb ítria, que pot conduir ions
a alta temperatura i permet mesurar la diferència d’activitat d’oxigen entre escapament i aire de referència.
-
• Els frens ceràmics amb discos de carboni-ceràmica o carbur de silici reforçat amb carboni mantenen propietats mecàniques a temperatura elevada i redueixen massa, però són cars i més difícils de fabricar que els discos de ferro colat.
La conseqüència per al disseny és clara. Les ceràmiques són excel·lents quan el component treballa en compressió, fricció, aïllament o alta temperatura, però cal evitar concentracions de tensió i impactes que obrin esquerdes. Per això sovint es fan servir en forma de recobriment, suport porós, aïllant o peça protegida dins un conjunt més gran.
5.7 Aliatges
5.7.1 Enllaç, cristalls i propietats
El comportament físic i químic dels metalls prové de l’enllaç metàl·lic. Els electrons interns romanen associats als nuclis, però una part dels electrons de valència queda deslocalitzada pel sòlid, formant un “gas d’electrons”. La conseqüència és que l’enllaç no és fortament direccional i els plans atòmics poden lliscar sota esforç sense trencar completament la cohesió del sòlid. Això explica propietats que són essencials en automoció.
-
• Alta conductivitat elèctrica i tèrmica
-
• Alta mal·leabilitat i ductilitat
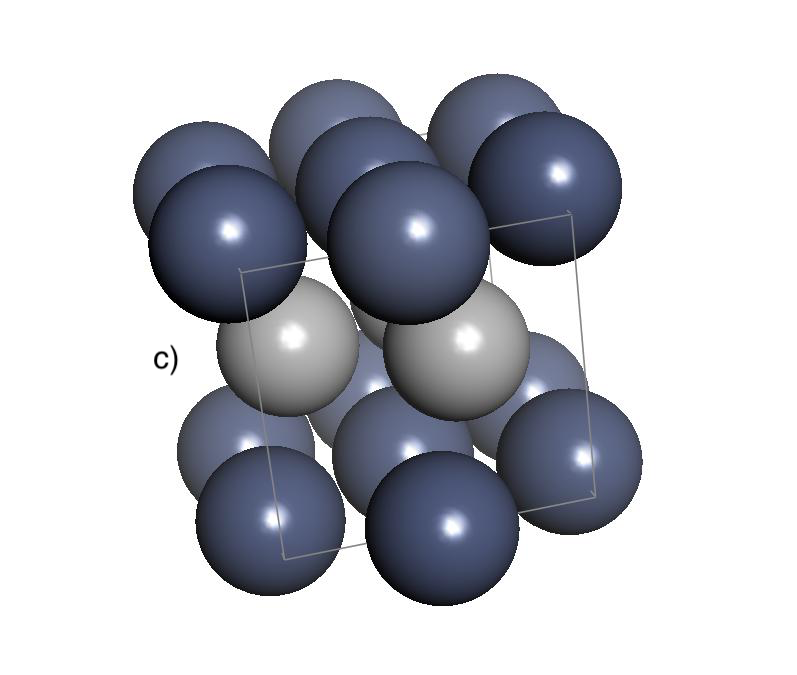
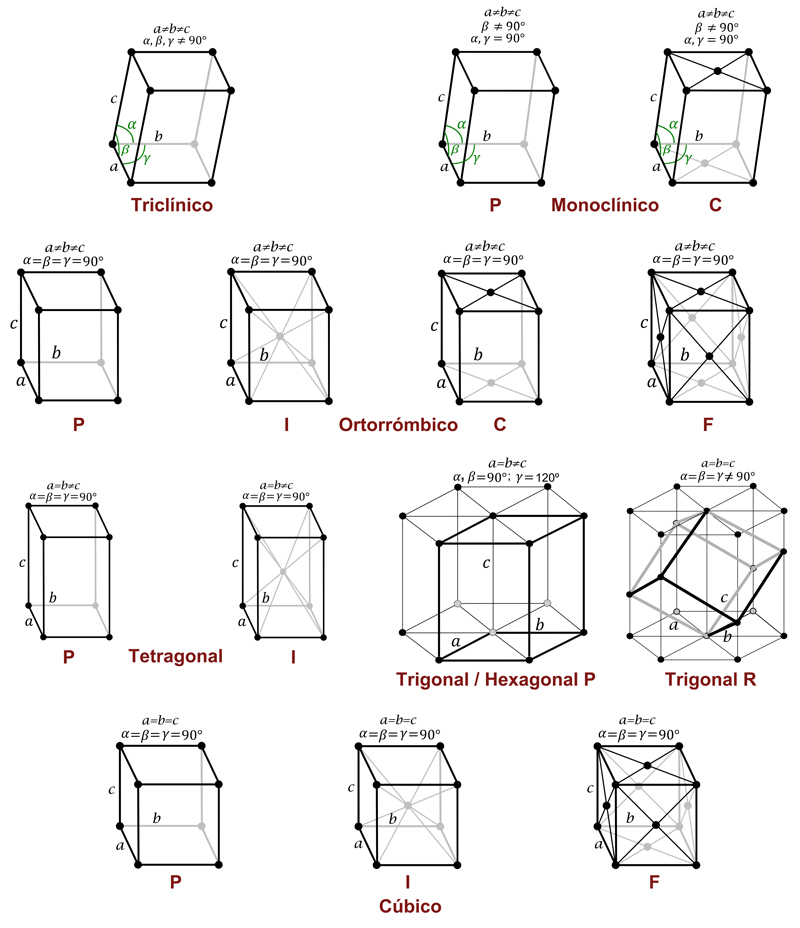
Pràcticament tots els metalls són sòlids a temperatura ambient i presenten lluentor metàl·lica. Una característica típica és que la conductivitat elèctrica disminueix quan augmenta la temperatura, perquè la vibració de la xarxa dispersa més els electrons. Estructuralment, la majoria de metalls i aliatges són sòlids cristal·lins, amb una cel·la unitat que es repeteix periòdicament en les tres dimensions. En tres dimensions hi ha set sistemes cristal·lins i catorze xarxes de Bravais (Figura 5.13), però la majoria de metalls d’interès cristal·litzen en tres estructures compactes o gairebé compactes, BCC, FCC i HCP[8, 7].
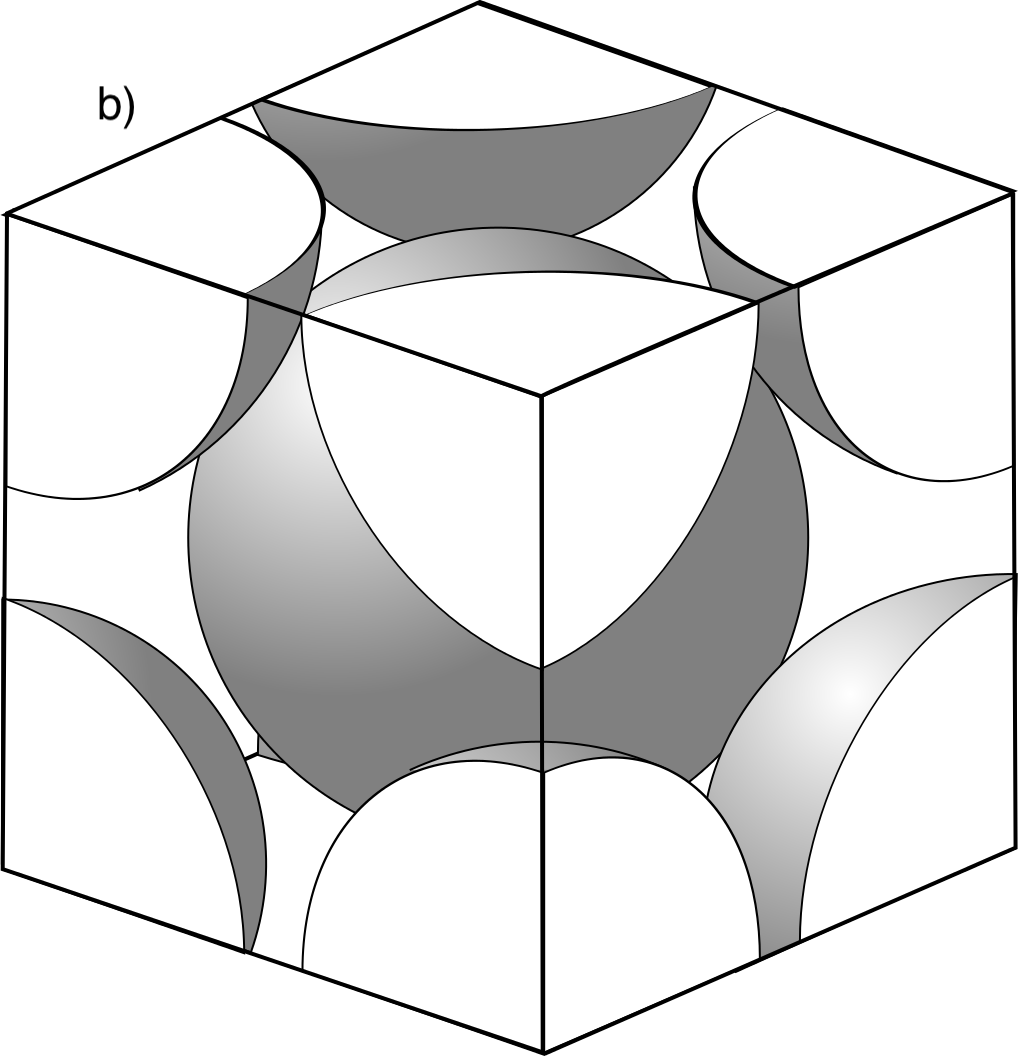
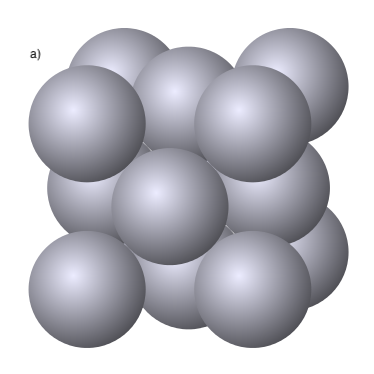
Les sigles BCC, FCC i HCP descriuen la manera com els àtoms metàl·lics ocupen l’espai en una xarxa periòdica (Figura 5.12). No són noms de materials, sinó patrons geomètrics d’ordenació. En una primera aproximació podem imaginar els àtoms metàl·lics com esferes iguals que es toquen.
-
• BCC (body-centered cubic, cúbica centrada en el cos) té àtoms als vèrtexs del cub i un àtom al centre. Els àtoms es toquen al llarg de la diagonal del cos. La cel·la conté 2 àtoms efectius, que corresponen a
dels vèrtexs més 1 àtom central. No és una estructura compacta màxima perquè cada àtom té 8 veïns pròxims i el factor d’empaquetament és 0,68.
-
• FCC (face-centered cubic, cúbica centrada a les cares) té àtoms als vèrtexs i al centre de cada cara del cub. Els àtoms es toquen al llarg de la diagonal de la cara. La cel·la conté 4 àtoms efectius,
. És una estructura compacta, amb 12 veïns pròxims i factor d’empaquetament 0,74.
-
• HCP (hexagonal close-packed, hexagonal compacta) també és una estructura compacta, amb 12 veïns pròxims i factor d’empaquetament 0,74. La diferència amb FCC no és la compacitat, sinó l’ordre d’apilament de les capes compactes. En HCP segueixen una seqüència ABAB, mentre que en FCC segueixen una seqüència ABCABC.
El factor d’empaquetament és la fracció del volum de la cel·la unitat que queda ocupada pels àtoms, si els aproximem com esferes rígides.
Un valor de 0,74 vol dir que el 74 % del volum està ocupat per esferes atòmiques i el 26 % restant correspon a buits intersticials. Aquest és el màxim empaquetament possible per a esferes iguals en tres dimensions, i per això FCC i HCP s’anomenen estructures compactes. BCC, amb 0,68, deixa més volum buit i no és compacta màxima, tot i que continua sent una estructura metàl·lica molt eficient. Aquesta idea d’empaquetament també apareix en sòlids iònics, on sovint es pot entendre l’estructura com un empaquetament d’anions amb cations ocupant els forats; vegeu la Secció ??.
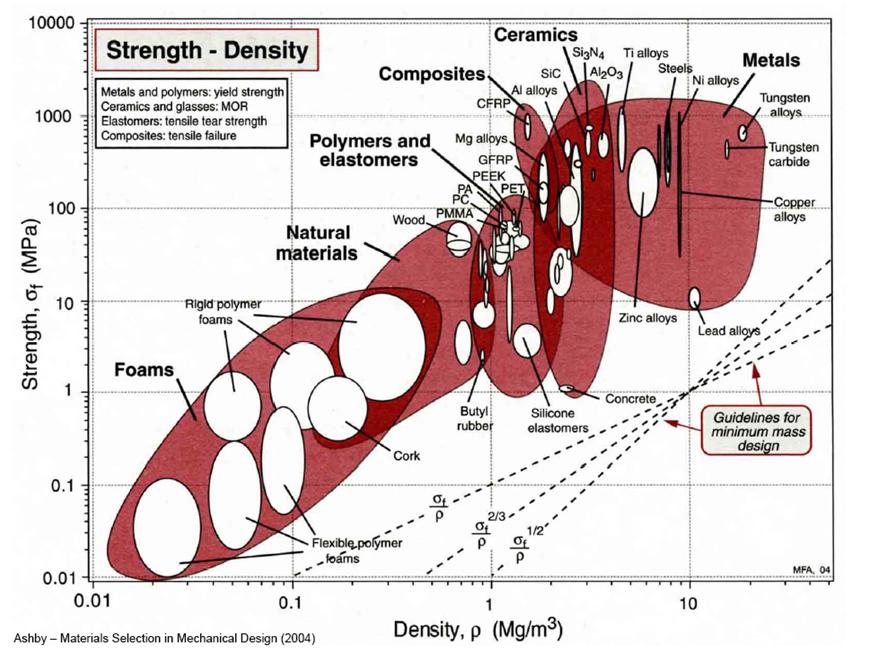
La Figura 5.14 mostra com es poden comparar resistència i densitat quan es tria un material per a una aplicació concreta.
A la Figura 5.13, les lletres majúscules indiquen el tipus de xarxa que presenta cada sistema cristal·lí.
-
• El tipus P correspon a la cel·la unitat primitiva, en la qual els àtoms estan situats als vèrtexs del poliedre.
-
• El tipus I correspon a la cel·la unitat centrada al cos, en la qual els àtoms estan situats als vèrtexs del poliedre i al seu interior.
-
• El tipus F correspon a la cel·la unitat centrada a les cares, en què els àtoms estan situats als vèrtexs del poliedre i en el centre de cada cara del políedre.
-
• El tipus C correspon a la cel·la unitat centrada a les tapes, en la qual els àtoms estan situats als vèrtexs del poliedre i a les cares perpendiculars a l’eix c.
En la Taula 5.5 es mostren exemples d’estructures cristal·lines de metalls purs.
|
Estructura |
Índex de coordinació |
Factor d’empaquetament |
Exemples |
|
Estructura |
Índex de coordinació |
Factor d’empaquetament |
Exemples |
|
BCC |
8 |
0,68 |
|
|
FCC |
12 |
0,74 |
|
|
HCP |
12 |
0,74 |
|
Les característiques de cada tipus de xarxa (compacitat, nombre de sistemes de lliscament i espais intersticials) condicionen les propietats dels metalls que les presenten, però no les determinen totes soles. La mida de gra, els soluts, els precipitats, els tractaments tèrmics i els defectes són igualment decisius. En general, molts metalls FCC són molt dúctils perquè tenen sistemes de lliscament actius a temperatura ambient; els HCP solen tenir menys ductilitat; i els BCC poden mostrar bona resistència però una ductilitat més sensible a la temperatura.
En un aliatge, la ubicació dels àtoms de solut depèn principalment del seu radi atòmic i de la mida dels espais intersticials en la xarxa cristal·lina del metall. Per exemple, els àtoms de carboni són prou petits per encaixar en els espais intersticials entre els àtoms de ferro a la xarxa cristal·lina del ferro (radi atòmic del C = 70 pm enfront dels 126 pm del Fe). En canvi, en l’aliatge Cu/Zn que anomenem llautó, els àtoms de zinc substitueixen directament els de coure a la xarxa cristal·lina perquè tenen radis atòmics similars (128 pm pel Cu contra 133 pm pel Zn).
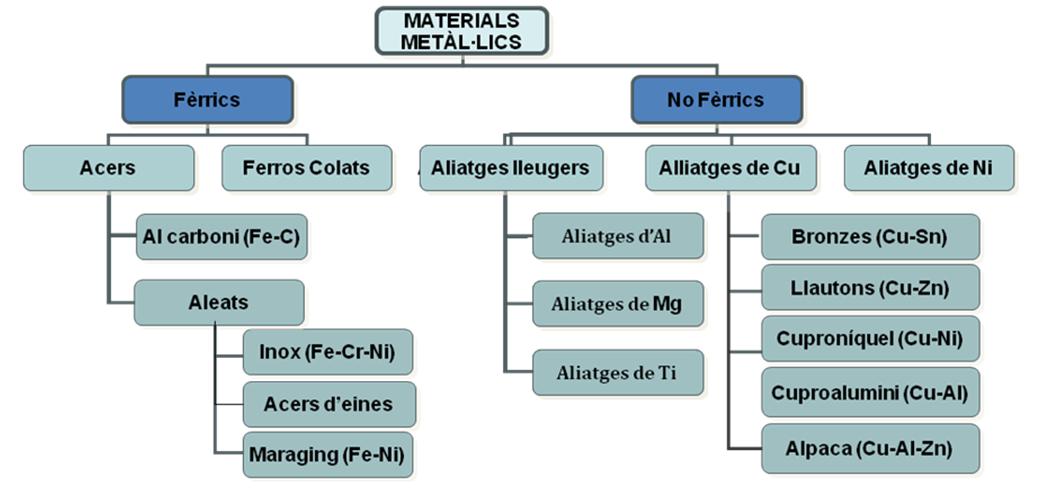
La Figura 5.15 resumeix una classificació general dels aliatges metàl·lics.
El principal avantatge de formar aliatges és que presenten propietats químiques i/o mecàniques diferents dels elements purs, generalment de manera positiva. Per exemple, afegir carboni al ferro dona lloc a una substància metàl·lica que anomenem acer, amb molta més resistència i duresa que el ferro sol. Es podria pensar que introduir un element que tendeix a formar enllaços covalents, com el C, canviarà la naturalesa de l’enllaç a l’aliatge; però, el ferro i altres aliatges continuen sent dominats per enllaços metàl·lics fins i tot en presència de soluts no metàl·lics.
5.7.2 Metal·lúrgia
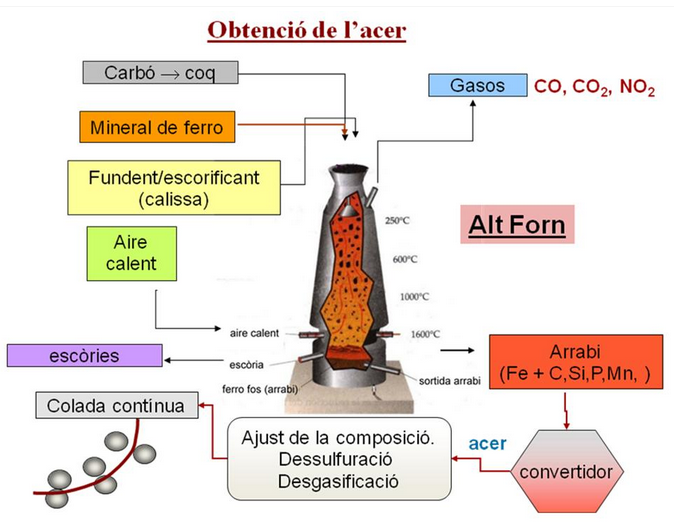
La metal·lúrgia del ferro ha anat evolucionant al llarg de la història de la humanitat, a causa de l’exigència de més consum i, per tant, d’una major productivitat, així com per la necessitat de millorar-ne les propietats. Un dels mètodes més utilitzats per a la producció de ferro és l’alt forn, el funcionament del qual es mostra en la Figura 5.16.
El ferro, amb una abundància relativa del 5%, és el primer metall de transició i el quart element més abundant de l’escorça terrestre. L’àrea de Sagunt ha estat un referent en la indústria metal·lúrgica de l’acer a Espanya, tot i que actualment ja no està en funcionament.
Si s’empren pirites o calcopirites com a matèries primeres, en primer lloc cal fer-hi un procés de torrada per formar el corresponent òxid de ferro. En realitat, les reaccions químiques que es produeixen en l’alt forn són senzilles. Es tracta de reaccions de reducció a alta temperatura. No obstant això, establir les condicions idònies d’operativitat del forn resulta complicat.
Una manera d’abaratir costos i simplificar l’operació és la utilització de fundents, com el carbonat de calci, que permet reduir la temperatura de treball, que ve donada per la temperatura de fusió del ferro (1 538 °C).
Com a agent reductor s’empra el monòxid de carboni, que es genera in situ mitjançant l’oxidació del carboni present en el coc.
És crucial mantenir completament controlada l’atmosfera de l’alt forn, ja que si hi ha massa oxigen, el monòxid es transforma en diòxid, fet que fa perdre poder reductor al forn i, per tant, eficiència en el procés.
En definitiva, dins de l’alt forn es produeix un equilibri químic entre totes les reaccions, un fet en què és de vital importància el seu control. Cal destacar també que l’oxidació del coc, és a dir, la seua combustió, té una doble funció. Actua tant de combustible com de reductor.
Agafem l’exemple de reducció de la magnetita, que, segons siga total o parcial, donarà lloc a les reaccions següents.
A més d’aquests processos principals, la fabricació de l’acer implica altres reaccions químiques rellevants, com la descomposició de la calcària i la carburació, que queden fora de l’abast d’aquest tema.
El ferro obtingut d’aquesta manera, encara amb impureses, s’anomena ferro colat i es drena per la part inferior del forn en un procés anomenat sagnat. Les impureses (cendres, etc.) es denominen escòria i, com que són menys denses que el ferro, es retiren per la superfície. Posteriorment, al ferro colat se’l sotmet a processos de dessulfuració, desoxidació, afinament, i addició dels aliatges necessaris per tal d’obtenir el material amb les propietats requerides.
Tant en la metal·lúrgia del ferro com en la d’altres aliatges és important distingir entre temperatura de fusió, interval de solidificació i microestructura final. Un metall pur fon i solidifica a una temperatura definida; un aliatge, en canvi, sovint solidifica en un interval de temperatures perquè la composició del líquid i del sòlid no és la mateixa. La velocitat de refredament, la composició i la presència de fases secundàries controlen la mida de gra, la segregació i la fragilitat del material resultant[7].
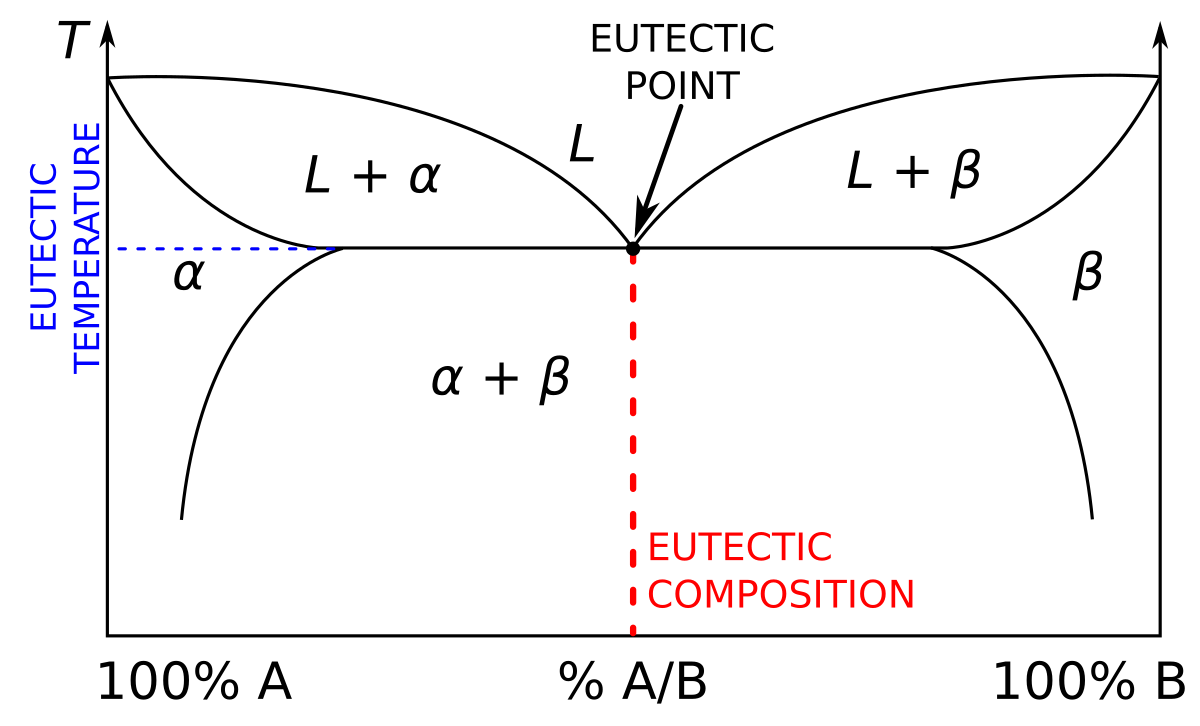
Per exemple, la Figura 5.17 mostra el diagrama de refredament d’un aliatge Pb-Sn a una composició del 15% d’estany en pes. Les aturades o canvis de pendent de la corba indiquen transformacions de fase. Part de la calor extreta no baixa la temperatura, sinó que es dedica a solidificar o transformar fases.
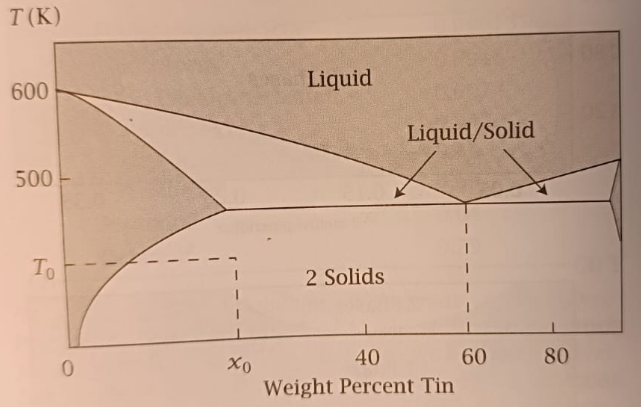
La majoria dels aliatges es preparen mitjançant la fusió de les proporcions adequades dels elements desitjats, i la composició és un factor crític. En un diagrama de fases binari, les línies de líquidus i sòlidus indiquen quines fases són estables a cada temperatura. En moltes composicions, en refredar, apareix primer una fase sòlida i després una segona fase. La composició eutèctica és un cas especial. El líquid solidifica a una temperatura mínima en una mescla íntima de dues fases sòlides. Això és útil en soldadures i aliatges colables perquè redueix la temperatura de fusió i dona una solidificació més definida, però no implica necessàriament una solució sòlida homogènia[7].
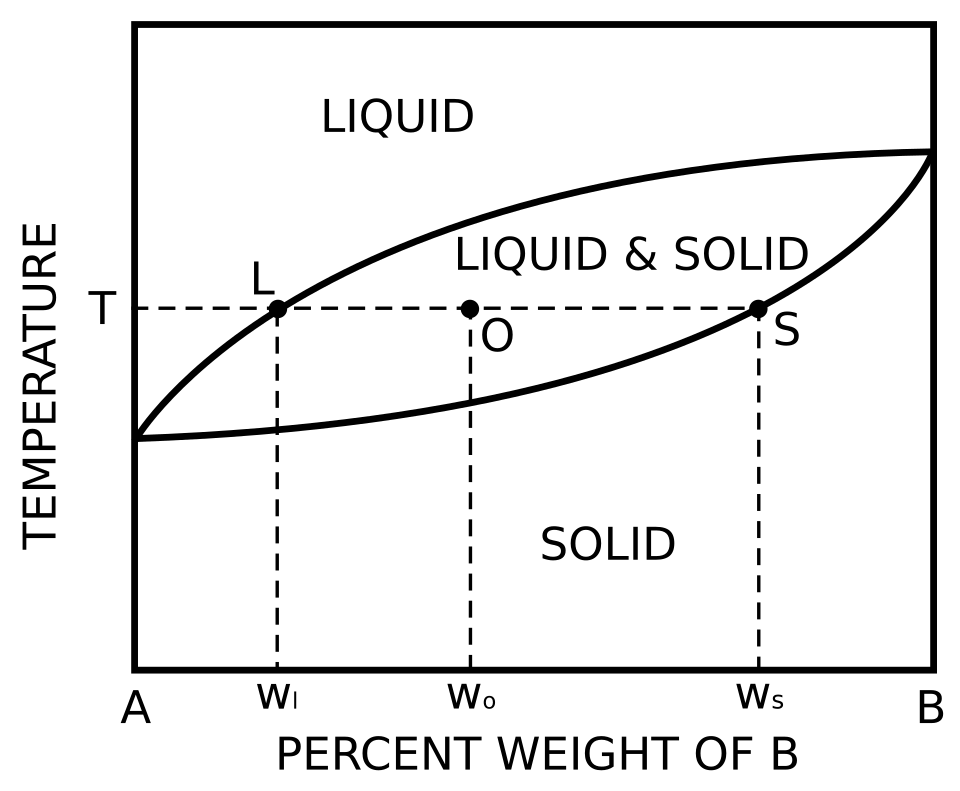
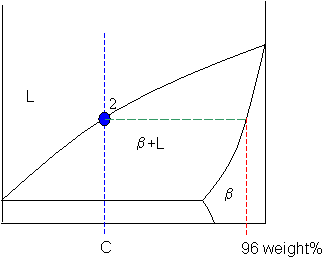
Quan una composició global es troba dins una regió bifàsica, el diagrama no només diu quines fases hi ha, sinó també quanta quantitat de cada fase s’espera. La regla de la palanca s’aplica dibuixant una isoterma, o línia d’equilibri horitzontal, a la temperatura considerada. Els dos punts on aquesta línia talla els límits de
la regió bifàsica donen la composició de cada fase en equilibri, com ara
per al sòlid
i
per al líquid. La composició global
queda entre aquests dos extrems, però no coincideix necessàriament amb la composició de cap de les fases.
El nom de la regla ve de la idea d’una palanca equilibrada, on la quantitat d’una fase és proporcional al segment oposat de la línia d’equilibri. Si , les fraccions màssiques de les dues fases són les següents[7, 24, 14].
El denominador és la longitud total de la isoterma dins la regió bifàsica, i cada numerador és la distància des de fins a l’extrem contrari. Per això, si
s’acosta a
, la fracció de fase
tendeix a 1 i la de líquid tendeix a 0; si
s’acosta a
, passa el contrari. La regla també es pot aplicar a dues fases sòlides, com
, substituint
per la composició de l’altra fase. És una eina útil per connectar un diagrama de fases amb propietats reals, perquè una fracció més alta d’una fase dura pot augmentar la resistència al desgast però reduir la ductilitat, mentre que una fracció més alta de fase dúctil pot millorar la tenacitat però reduir la
duresa.
5.7.2.1 Ús pas a pas de la regla de la palanca
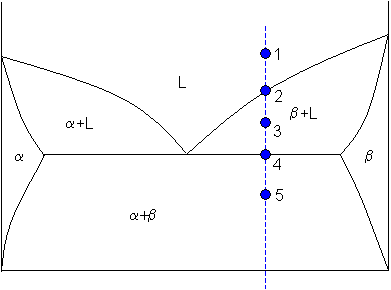
La regla de la palanca només s’aplica quan el punt de treball cau dins una regió de dues fases. En una regió monofàsica no cal calcular cap repartiment, perquè tota la mostra és aquella fase i la seva composició és la composició global. En una regió bifàsica, en canvi, la regla ens permet respondre les qüestions següents.
-
1. quina és la composició de cada fase i
-
2. quina és la quantitat de cada fase.
La composició global de l’aliatge actua com el punt de suport d’una balança; les composicions de les dues fases són els extrems de la barra. La fase situada a un extrem és més abundant com més llarg és el braç oposat[14].
El procediment operatiu és el següent.
-
1. Situar el punt de l’aliatge. Es fixa la composició global
a l’eix horitzontal i la temperatura de treball a l’eix vertical. Si el punt és dins
,
,
, etc., no s’aplica la regla de la palanca.
-
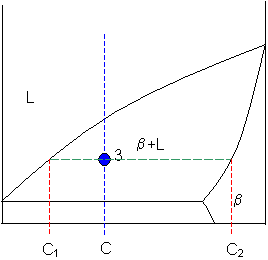
2. Dibuixar la isoterma. Es traça una línia horitzontal a la temperatura considerada fins que talla les fronteres de la regió bifàsica. Aquesta línia és la línia d’equilibri, o tie-line.
-
3. Llegir les composicions dels extrems. L’extrem esquerre dona la composició d’una fase i l’extrem dret la de l’altra. En una regió
, per exemple, podem anomenar-les
i
. Aquestes composicions són propietats de les fases en equilibri a aquella temperatura, no de tota la mostra. En general, si els extrems són
i
, amb
, la fracció de la fase de composició
és
, i la de la fase de composició
és
.
-
4. Calcular cada fracció amb el braç oposat. La fracció d’una fase es calcula amb la distància des de
fins a l’extrem de l’altra fase, dividida per la longitud total de la isoterma. Aquesta és la idea de la palanca, ja que cada fase es calcula amb el segment oposat.
-
5. Comprovar el resultat. Les fraccions han de sumar 1, o 100%. A més, si
és més a prop d’un extrem, la fase d’aquell extrem ha de ser la majoritària.
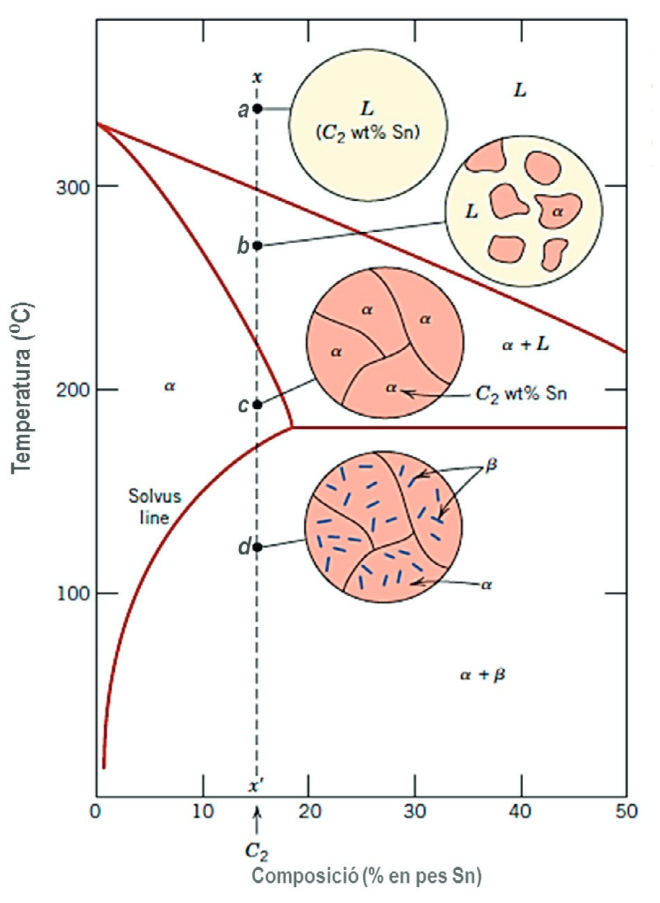
Com a exemple numèric, considerem un aliatge binari amb composició global
en massa de B. A temperatura alta, si el punt cau dins la regió
, l’aliatge és completament líquid i la composició del líquid és simplement
. Quan el refredament arriba a la línia de líquidus, comença a formar-se el primer sòlid
. En l’exemple de DoITPoMS, aquest primer sòlid apareix amb una composició aproximada de
B; és una dada del diagrama, no una fracció de fase.
Un cop el punt ja és dins la regió , la regla de la palanca permet calcular quina part és líquid i quina part és sòlid
. A una certa temperatura, la isoterma talla el límit del líquid a
B i el límit del sòlid
a
B. Les fraccions són
Per tant, l’aliatge conté aproximadament un en massa de sòlid
i un
en massa de líquid. La diferència entre
i
és només arrodoniment. Amb el mateix diagrama, si es refreda fins a una temperatura més baixa dins la mateixa zona
, els extrems de la isoterma poden passar, per exemple, a
B i
B. Aleshores,
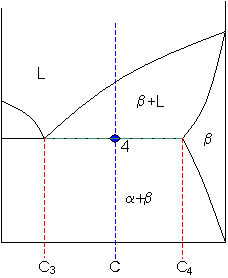
El sentit físic del càlcul és que, en refredar, augmenta la fracció de sòlid i disminueix la de líquid. Si aquesta temperatura correspon a l’eutèctic, el líquid que queda no solidifica com una sola fase, sinó com un microconstituent eutèctic
. Per tant, en aquest punt es pot dir que hi ha un
de
primari i un
de líquid que, en completar la reacció eutèctica, es transformarà en un
de microconstituent eutèctic. Cal mantenir separades les fases
,
i
dels microconstituents que s’observen després de solidificar.
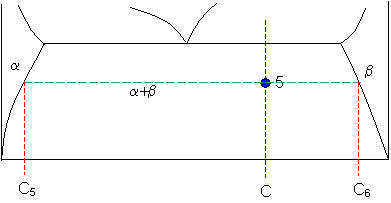
Si finalment el material queda dins una regió , la mateixa regla es fa servir amb les dues fases sòlides. Per exemple, amb
B i
B,
En aquest últim cas el resultat no parla de líquid i sòlid, sinó del repartiment final entre dues fases sòlides, amb aproximadament un de fase
i un
de fase
. La lectura correcta d’un exercici ha d’incloure sempre les fases presents, la composició de cada fase i la fracció de cada fase. Quan hi ha una reacció eutèctica, també pot caldre distingir entre fraccions de fase finals i fraccions de microconstituents. Escriure només
o només el percentatge d’una fase deixa incompleta la informació que proporciona el diagrama.
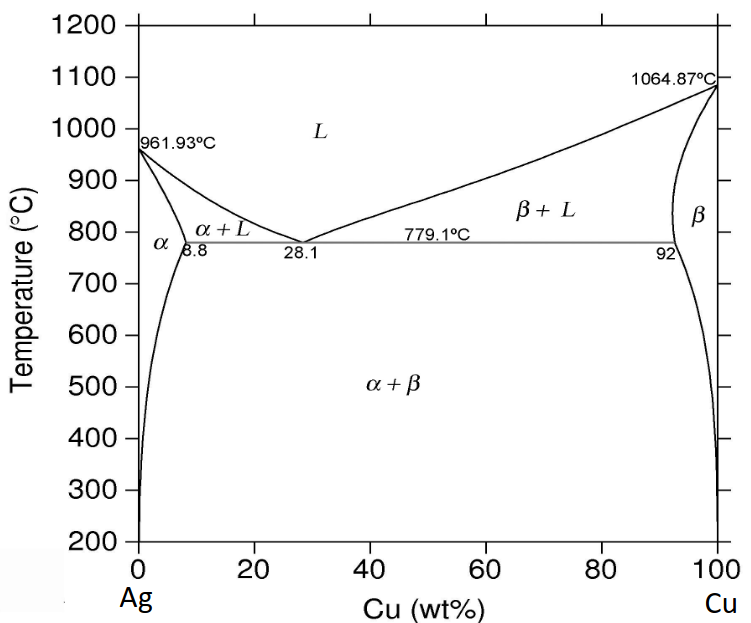
La Figura 5.20 mostra de manera esquemàtica la composició eutèctica i la temperatura mínima de fusió d’un sistema binari.
5.7.3 Aliatges fèrrics
Els aliatges fèrrics tenen el ferro com a element majoritari. Són els més abundants en automoció perquè combinen cost relativament baix, bona resistència, soldabilitat i una gran varietat de tractaments tèrmics. L’avantatge de l’acer respecte al ferro pur sorgeix perquè els àtoms de carboni intersticials dificulten
el moviment de dislocacions, que és el mecanisme microscòpic principal de deformació plàstica. Afegir crom millora la resistència a la corrosió perquè es forma una capa passiva rica en òxid de crom; per això anomenem acers inoxidables els aliatges amb prou crom per mantenir aquesta passivació[7, 8].
Els inconvenients principals dels aliatges fèrrics són la densitat elevada i la susceptibilitat a corrosió si no hi ha recobriment, passivació o protecció electroquímica. Per això l’automoció moderna combina acers avançats d’alta resistència amb alumini, magnesi, polímers i composites en funció de la zona del vehicle.
Acer L’acer és un aliatge de ferro i carboni, amb un contingut de carboni que oscil·la entre el 0,02% i el 2,1% en pes, amb concentracions variables d’altres elements. La designació AISI/SAE dels acers consta de quatre xifres, on les dues primeres indiquen el contingut en elements d’aliatge (per als acers al carboni són 1 i 0) i les dues últimes, la concentració de carboni (percentatge en carboni multiplicat per 100).
S’identifiquen segons el contingut en carboni o bé en funció de la seva aplicació.
-
• Els acers de baix carboni amb menys del 0,25 % C són relativament tous i poc resistents, amb extraordinària ductilitat i tenacitat, ideals per a carrosseries d’automoció, bigues, etc. L’addició d’elements d’aliatge proporciona característiques mecàniques molt diverses, millorant notablement les respostes dels acers que només tenen carboni com a element d’aliatge. Cal destacar el grup dels HSLA (High Strength Low Alloy), que és un grup d’acers molt més resistents mecànicament i a la corrosió que els acers al carboni d’aquest mateix grup. Les microestructures més habituals són ferrítiques i/o ferritoperlítiques.
-
• Els acers de mig carboni amb entre 0,25 i 0,6 % C poden ser tractats tèrmicament a fi de modificar la seva microestructura per guanyar duresa i resistència, en detriment de la ductilitat i la tenacitat. Són especialment indicats per a la fabricació de rails de trens, engranatges i cigonyals.
-
• Els acers d’alt carboni amb entre 0,6 i 1,4 % C són més durs i resistents que els altres acers al carboni però menys dúctils. Són molt resistents al desgast i s’utilitzen habitualment com a eines de tall i matrius de conformat de materials. Presenten microestructures de perlita (eutectoide Fe-C).
-
• Els acers inoxidables recullen un conjunt d’acers molt resistents a la corrosió per l’alta concentració de crom (més d’un 12 %), que afavoreix la generació d’una capa d’òxid de crom superficial que evita progressius atacs del medi. Es classifiquen segons la microestructura, i així es troben inoxidables martensítics, inoxidables ferrítics (fase alfa BCC) o inoxidables austenítics (fase gamma FCC). Els martensítics i ferrítics tenen comportament magnètic.
Ferro colat El ferro colat és un aliatge de ferro amb un contingut de carboni superior al 2,1% en pes; la majoria de ferros colats comercials contenen aproximadament entre un 3 i un 4,5% de carboni. La seva microestructura és més complexa que la dels acers i depèn del contingut en carboni, silici, velocitat de refredament i tractaments posteriors. Els ferros colats es classifiquen segons la microestructura; entre els més habituals hi ha ferros colats grisos, blancs, nodulars i mal·leables.
-
• El ferro colat blanc, amb continguts en C entre 2 i 3,5 %, presenta continguts importants de cementita (carbur de ferro, Fe3C), que confereixen una gran duresa i fragilitat. És ideal per a aplicacions en què el material hagi de suportar tensions elevades sense deformar-se. Amb un tractament tèrmic, es pot convertir en ferro colat maleable, ja que la cementita es disgrega en grafit (nòduls ramificats) dins una matriu de ferrita o perlita.
-
• El ferro colat gris, amb continguts de C entre 2,5 i 4 %, i entre 1,0 i 3,0 % de Si, presenta làmines de grafit dins una matriu de ferrita alfa o de perlita. Són fràgils i poc resistents a tracció, però són resistents i dúctils sota esforços de compressió. Són molt econòmics i poden ser tractats tèrmicament per tal de modificar la seva microestructura i guanyar una mica de ductilitat (ferro dúctil o esferoïdal, amb el grafit en forma d’esferoids, en comptes de làmines).
5.7.4 Aliatges no fèrrics
Els aliatges no fèrrics no tenen el ferro com a component majoritari. En automoció s’utilitzen quan la reducció de massa, la resistència a corrosió, la conductivitat o el comportament a alta temperatura compensen un cost superior.
La classificació d’aliatges no fèrrics es fa en base a l’element majoritari, tot i que cada gran grup pot contenir diversos subgrups.
-
• Els aliatges de coure parteixen d’un coure pur que és molt tou i dúctil i difícil de treballar. La seva resistència mecànica i a la corrosió millora per aliatge.
-
– En el llautó, el zinc actua de solut.
-
– El bronze és coure amb estany, alumini, silici i níquel. És més resistent que el llautó.
-
-
• Els aliatges d’alumini destaquen per baixa densitat, bona resistència específica i resistència a corrosió per passivació. Són habituals en llantes, blocs de motor, peces de bastidor i panells.
-
• Els aliatges de titani combinen resistència específica elevada i bona resistència a corrosió, però són cars i difícils de processar. S’usen sobretot en aplicacions d’alt valor o competició.
-
• Els aliatges de magnesi tenen densitat molt baixa, però menor ductilitat i més sensibilitat a corrosió; requereixen disseny i protecció superficial acurats.
-
• Els superaliatges, basats en níquel, cobalt o ferro, mantenen resistència i estabilitat a temperatura molt alta. Són típics de turbines i zones extremes, més que de components massius d’un turisme convencional.
Els materials metàl·lics, per la seva combinació de propietats mecàniques, elèctriques, tèrmiques i industrials, són insubstituïbles per a gran quantitat d’elements elaborats dins els sectors següents.
-
• En el sector aeronàutic, una de les parts de l’avió que resulta més desafiant respecte la millora de mescles de metalls és l’anomenada turbina a gas o turboreactor.
-
• En el sector automoció, l’acer és un dels materials més abundants en estructura i carrosseria; l’alumini s’utilitza en elements de bastidor, blocs de motor, llantes i panells; platí, paladi i rodi intervenen en catalitzadors; el coure apareix al cablejat i als contactes; el zinc protegeix xapes d’acer per galvanització.
-
• En el sector elèctric, les aplicacions més destacades dels materials metàl·lics són les de transformadors, connectors elèctrics, fils superconductors, suports de contactes elèctrics i parts d’interruptors, entre d’altres.
-
• En el sector electrònic, els materials que s’utilitzen han de suportar estructuralment els components, proporcionar protecció contra els efectes mediambientals i dissipar els excessos de calor generats pels components electrònics. Els materials utilitzats han de mostrar alta rigidesa, alta conductivitat tèrmica, un coeficient d’expansió tèrmica baix i una densitat molt baixa.
-
• En el sector químic, els materials metàl·lics tenen aplicacions molt diverses. Es podria destacar l’ús del magnesi, per la seva lleugeresa; el zinc per la seva utilitat com a protecció catòdica d’altres metalls; els acers inoxidables com a contenidors i recipients, etc.
5.7.5 Ús dels aliatges en automoció
Les propietats especials dels aliatges, especialment la resistència a la corrosió, fan que siguin materials molt utilitzats en l’automòbil.
Les rodes d’aliatge i de magnesi (mag) són extremadament populars entre els entusiastes de l’automòbil i són sovint opcions escollides en vehicles comercials. Sens dubte, les rodes personalitzades o de recanvi són una manera eficaç i relativament econòmica de personalitzar estèticament un cotxe, però què són exactament les rodes d’aliatge, quina relació tenen amb la química i quins avantatges reals ofereixen?
L’acer i l’acer inoxidable s’utilitzen per a panells de carrosseria, components estructurals, sistemes d’escapament, discs de fre, alguns tipus de rodes, etc. L’ús d’aliatges no fèrrics (no basats en Fe) en rodes d’automòbil prové de l’esforç per fer els cotxes més lleugers i reduir el que es coneix com a massa no suspesa. La massa no suspesa és el pes del vehicle que no és suportat pel sistema de suspensió, i reduir-la pot millorar la maniobrabilitat del vehicle, l’eficiència del combustible i fins i tot una mica l’acceleració.
Un altre benefici de les rodes d’aliatges d’alumini, magnesi i similars és que aquests metalls tenen una conductivitat tèrmica elevada, cosa que ajuda a dissipar la calor generada per fricció dels frens i dels pneumàtics. Fer rodes amb aliatges de baixa densitat i bona resistència específica aconsegueix alhora reducció de massa i dissipació tèrmica, i va ser l’enfocament original per a fabricar rodes d’alt rendiment.
Tanmateix, l’alumini i el magnesi purs no són tan resistents com l’acer i estan subjectes a diverses reaccions de corrosió que poden malmetre l’aspecte o la funció de les rodes. La resistència i la resistència a la corrosió de les rodes d’alumini o magnesi es poden millorar aplicant recobriments metàl·lics o polimèrics a la superfície o fabricant rodes amb aliatges d’aquests metalls.
Els aliatges són més desitjables perquè, si el recobriment superficial es danya en una roda de Al o Mg pur, l’aigua i els ions poden penetrar sota el recobriment i corroir la roda des de dins.
Les rodes d’aliatge basades en magnesi solen contenir entre un 2% i un 12% d’alumini, juntament amb quantitats menors de zinc, zirconi i/o altres metalls exòtics. La millora mecànica de l’aliatge prové principalment del solut d’alumini, mentre que els altres soluts aporten resistència a la corrosió.
Els aliatges a base d’alumini sovint contenen entre un 2% i un 4% de Mg, juntament amb Be, Mn i Zn com a antioxidants, i quantitats variables de Si. Les formulacions específiques dels aliatges varien segons el mètode de fabricació de la roda (si les rodes són colades, forjades, mecanitzades, etc.).
5.8 Materials per a cèl·lules de combustible
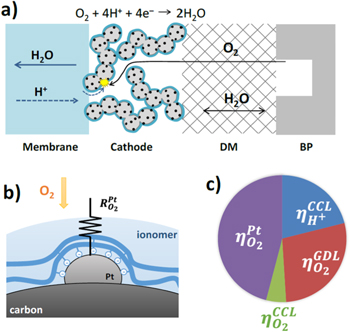
Les cèl·lules de combustible ja apareixen al capítol d’electroquímica com a dispositius redox. Aquí l’objectiu és diferent. Es tracta d’entendre quins materials fan possible el dispositiu i quines limitacions imposen. Una PEMFC d’automoció necessita una membrana que condueixi protons però bloquegi gasos i electrons, catalitzadors actius i durables, plaques i capes poroses que distribueixin gasos, i dipòsits lleugers capaços d’emmagatzemar hidrogen a alta pressió[16, 12].
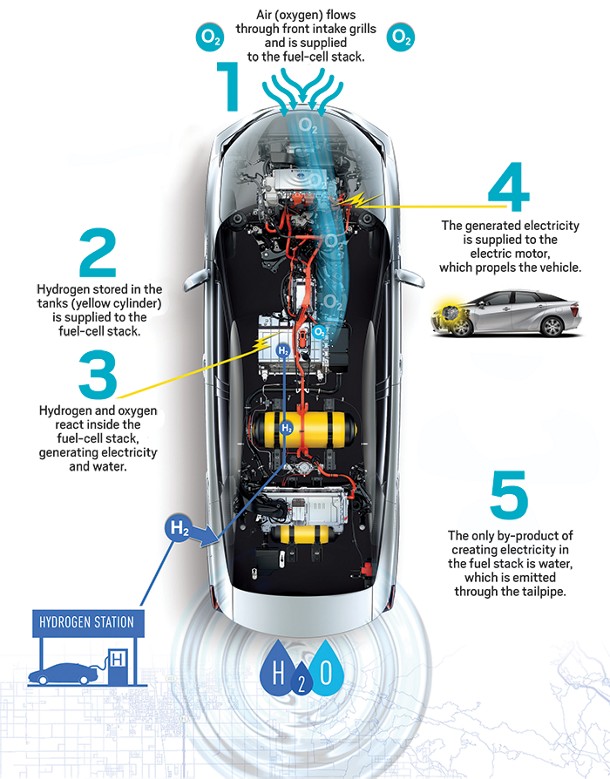
Una alternativa als motors de combustió és generar electricitat a bord a partir d’hidrogen i oxigen. Si l’hidrogen s’ha produït amb electricitat baixa en carboni, la cadena pot reduir molt les emissions locals i globals; si prové de gas natural sense captura de carboni, el balanç ambiental és pitjor. Per això convé separar el dispositiu electroquímic de la font de l’hidrogen. La Figura 5.21 mostra un vehicle comercial de pila d’hidrogen, el Toyota Mirai.
La recerca en materials se centra en quatre colls d’ampolla. Cal reduir o substituir platí, millorar membranes que no s’assequin ni es degradin, dissenyar capes poroses que transportin gas i aigua sense grans pèrdues, i fabricar dipòsits de tipus III o IV amb prou seguretat i baixa massa.
Una cèl·lula de combustible és una alternativa a les bateries per generar corrent elèctric. En una bateria, els reactius redox estan emmagatzemats dins el dispositiu; en una cèl·lula de combustible, el combustible i l’oxidant s’alimenten contínuament des de l’exterior. Per tant, no és un dipòsit tancat d’energia
química, sinó un convertidor que transforma energia química en energia elèctrica mentre rep combustible, per exemple hidrogen gasós , i oxidant, habitualment
.
El concepte de cel·la de combustible s’origina al segle XIX, però no ha estat fins al final del XX que diverses proves pilot han demostrat que les cèl·lules de combustible poden ser una alternativa viable als motors de combustió interna. Van ser reconegudes com a dispositius fiables quan la NASA (Administració Nacional de l’Aeronàutica i de l’Espai dels EUA) va utilitzar aquests generadors d’energia durant les dècades de 1960 i 1970 en les missions Gemini i Apollo, així com en altres programes espacials[15].
Totes les cèl·lules de combustible contenen un electròlit, un combustible, catalitzadors a l’ànode i al càtode, i els elèctrodes/connexions. Hi ha una gran varietat d’electròlits disponibles, incloent líquids com la (utilitzada al programa espacial), ceràmiques sòlides i membranes d’electròlit polimèric.
5.8.1 Cèl·lules de combustible d’hidrogen
La cèl·lula de combustible més rellevant per a automoció lleugera és la d’hidrogen/oxigen amb membrana d’intercanvi protònic. En medi àcid, la reacció global produeix aigua i corrent.
El potencial reversible de la reacció és 1,23 V en condicions estàndard, però una cèl·lula real treballa a una tensió inferior per pèrdues d’activació, resistència òhmica i transport de massa. L’únic producte local és aigua; la contribució real a depèn de com s’hagi produït l’hidrogen.
S’han explorat altres combustibles, com el metanol i altres alcohols i hidrocarburs; tanmateix, aquestes reaccions generen diòxid de carboni com a subproducte i, per tant, són menys desitjables.
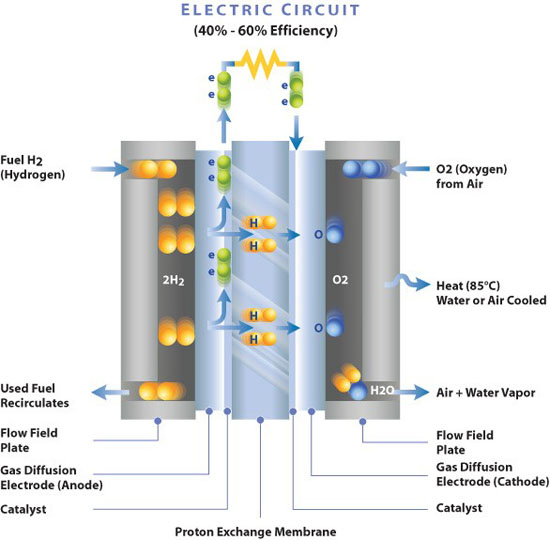
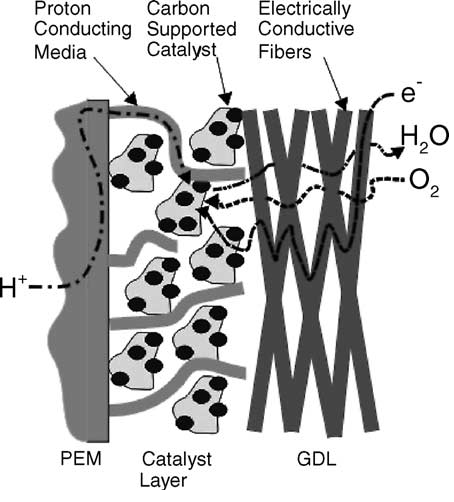
Una PEMFC (polymer electrolyte membrane fuel cell) utilitza una membrana ionomèrica semipermeable que permet el pas de protons (), però actua com a aïllant elèctric i barrera per a electrons, oxigen i hidrogen. El conjunt membrana-elèctrodes (MEA) situa la membrana entre ànode i càtode. A l’ànode, el catalitzador oxida
a protons i electrons. Els electrons circulen pel circuit extern i fan treball elèctric; els protons travessen la membrana; al càtode, oxigen, protons i electrons formen aigua.
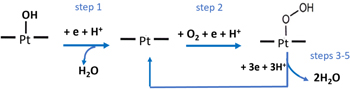
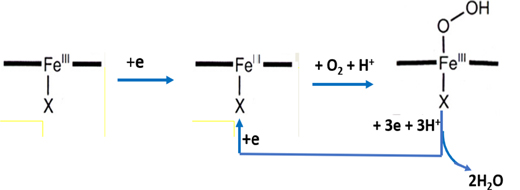
El procés electroquímic a l’ànode és ràpid i requereix poca quantitat de platí, però al càtode és més lent, necessita més platí i ofereix més oportunitats per reduir-ne l’ús o substituir-lo per altres materials.
El platí és ideal com a catalitzador perquè facilita les reaccions d’hidrogen i oxigen a una velocitat òptima, és estable en l’entorn químic de la cèl·lula i suporta altes densitats de corrent elèctric, mantenint l’eficiència a llarg termini.
Membranes polimèriques Les cèl·lules de combustible amb PEM són les de més projecció per a vehicles, ja que es poden fabricar de manera compacta i lleugera i funcionen a temperatures relativament baixes (50 °C a 100 °C).
La pel·lícula de gruix micromètric té dues funcions.
-
1. És un electròlit sòlid que condueix ions d’hidrogen des de l’ànode fins al càtode. Això s’aconsegueix mitjançant membranes ionòmeres. Consisteixen en un esquelet polimèric robust amb grups àcids fixos, com
, que faciliten el transport protònic quan la membrana és prou hidratada.
-
2. És un separador de gasos que evita la barreja directa i incontrolada d’hidrogen i oxigen. Aquesta barreja malgasta combustible, fa que la cèl·lula de combustible funcioni de manera ineficient i genera subproductes que poden degradar els components de la cèl·lula de combustible.
La Figura 5.22 presenta l’esquema d’una cèl·lula PEMFC i un exemple d’ionòmer relacionat amb el transport iònic.
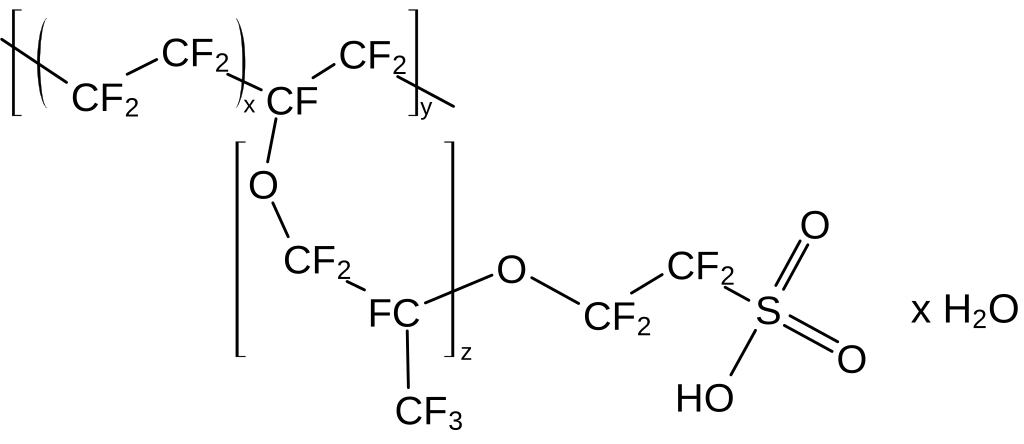
La membrana PEM més popular fins ara és la Nafion, produïda per DuPont. El Nafion o àcid perfluorosulfònic (PFSA, Figura 5.23) és un copolímer fluorinat amb grups àcid sulfònic. Utilitza aquests grups per facilitar el transport de protons mitjançant el mecanisme de ”salt”entre grups àcids a través de la matriu polimèrica.
L’ús de fluor a l’esquelet evita intercanvis de protons no desitjats amb el polímer. En principi, qualsevol membrana ionòmera amb funcionalitats àcid sulfònic o fosfòric podria ser una bona PEM, sempre que l’estructura sigui estable a la temperatura de funcionament i les taxes d’intercanvi protònic siguin suficientment ràpides.
Catalitzadors Pel que fa als catalitzadors, moltes cèl·lules de combustible requereixen metalls del grup del platí, abreujats PGM, com Ru, Rh, Pd, Os, Ir i Pt, níquel o altres metalls de transició per accelerar l’oxidació del combustible a l’ànode i la reducció d’oxigen al càtode. La reacció de reducció d’oxigen és especialment lenta; per això el càtode és un dels punts més importants de recerca en materials[16].
Problemes mediambientals dels metalls del grup del platí
Anteriorment es considerava que els metalls del grup del platí (PGMs) tenien molt pocs efectes negatius en comparació amb les seves propietats distintives i la seva capacitat per reduir les emissions nocives dels gasos d’escapament dels vehicles. Tot i això, cada vegada hi ha més proves que mostren que l’acumulació d’aquests metalls pot suposar un risc ambiental i per a la salut. Encara que el platí metàl·lic es considera inactiu i no al·lergènic, pot dissoldre’s en la pols de carretera, entrar a l’aigua i al sòl, i acumular-se en animals a través de la cadena alimentària. Això pot afectar tant la biodiversitat com la salut humana.
L’ús mèdic del platí, com en el fàrmac cisplatina per tractar tumors, també comporta efectes secundaris greus com nàusees, pèrdua d’audició i dany renal, així com riscos per al personal mèdic que el manipula (veure l’estructura de la seva interacció amb el DNA aquí). A més, els processos d’extracció i refinament del platí poden provocar contaminació ambiental, com s’ha vist a Zimbàbue. Els compostos halogenats de platí poden causar reaccions al·lèrgiques greus, especialment en treballadors de la indústria química.
Emmagatzematge de l’ L’hidrogen es pot emmagatzemar de diverses maneres, incloent-hi gas a alta pressió, líquid criogènic o en forma d’hidrurs metàl·lics. Els mètodes d’emmagatzematge d’hidrogen més comuns són els següents.
-
• En forma de gas a alta pressió, l’hidrogen es pot emmagatzemar en dipòsits d’acer o compostos. Els dipòsits d’acer són pesats i voluminosos, mentre que els dipòsits de compostos són més lleugers i compactes.
-
• En forma de líquid criogènic, l’hidrogen es pot emmagatzemar a temperatures criogèniques (menys de −253 °C). Els dipòsits criogènics són cars i pesats, però l’hidrogen líquid té una densitat energètica molt alta.
-
• En forma d’hidrurs metàl·lics, l’hidrogen queda incorporat en compostos químics que contenen hidrogen i metalls. Els hidrurs metàl·lics són segurs i eficients per emmagatzemar hidrogen, però la seva capacitat d’emmagatzematge és limitada.
Els vehicles de pila d’hidrogen utilitzen sobretot hidrogen gasós comprimit. En turismes, el valor habitual de disseny és de fins a 700 bar (70 MPa), mentre que en alguns vehicles pesants es fan servir sistemes de 350 bar. Aquestes pressions obliguen a pensar el dipòsit com un component
multicapa. Inclou una barrera interior contra la fuita d’, una estructura resistent que suporta la pressió, elements metàl·lics de connexió i vàlvules, i una protecció exterior contra impacte, abrasió, foc i envelliment ambiental.
La classificació dels dipòsits d’hidrogen es basa en quina part del recipient suporta la càrrega mecànica i quin material fa de barrera al gas (Taula 5.6). Els dipòsits de tipus I i II són majoritàriament metàl·lics i, per tant, robustos però massa pesants per a un vehicle lleuger. Els tipus III i IV són dipòsits compostos. Les fibres, normalment de carboni en una matriu epoxi, suporten la major part de l’esforç circumferencial; el folre interior evita la fuita de gas i dona forma al recipient. El tipus V elimina el folre i promet menor massa, però és molt exigent perquè el material compost ha de ser alhora estructura i barrera contra una molècula tan petita com l’hidrogen[12].
Com llegir els tipus de dipòsits d’hidrogen
Tipus I. És un recipient metàl·lic sense reforç compost. És simple i relativament econòmic, però té una massa elevada perquè tot l’esforç de pressió el suporta l’acer o l’alumini.
Tipus II. És un recipient metàl·lic reforçat parcialment amb fibres només a la zona cilíndrica. Redueix una part de la massa, però el metall continua tenint un paper estructural important.
Tipus III. Té un folre metàl·lic, sovint d’alumini, completament embolicat amb fibra de carboni/epoxi. El metall és una bona barrera contra l’hidrogen i ajuda a dissipar calor, però afegeix massa i pot patir problemes de fatiga, corrosió o compatibilitat amb l’hidrogen.
Tipus IV. Té un folre polimèric, per exemple HDPE, PA o un altre termoplàstic barrera, completament embolicat amb fibra de carboni/epoxi. És la solució més habitual en automoció lleugera perquè redueix massa. El polímer segella i el compost resisteix. Els reptes són la permeació d’, la fluència del polímer, els cicles de pressurització, la unió amb les boques metàl·liques de connexió i la protecció contra impacte i foc.
Tipus V. És un dipòsit compost sense folre. Pot ser el més lleuger, però encara és difícil garantir simultàniament baixa permeabilitat, tolerància al dany, fabricació repetible i certificació de seguretat per a ús massiu.
En conseqüència, el dipòsit d’hidrogen és un bon exemple de selecció integrada de materials. S’hi combinen polímers per a segellat i baixa permeabilitat, fibres de carboni per a resistència específica, resines termoestables per transferir càrrega entre fibres, metalls per a connexions i vàlvules, i recobriments externs per a protecció. Només els dipòsits de tipus III i IV s’utilitzen de manera habitual en vehicles de pila d’hidrogen; el tipus IV tendeix a ser preferit quan la massa és el criteri dominant, mentre que el tipus III pot ser atractiu quan es prioritzen barrera, robustesa i gestió tèrmica.
|
Taula 5.6: Classificació i aplicacions de diferents dipòsits d’hidrogenFont: [12]. |
|||
|
Tipus |
Materials |
Pressió màxima (bar) |
Aplicacions |
|
Tipus |
Materials |
Pressió màxima (bar) |
Aplicacions |
| Continua a la pàgina següent | |||
|
I |
Acers o alumini |
|
Aplicacions submarines |
|
II |
Revestiment de |
|
Piles de combustible estacionàries i tecnologies d’hidrogen (FCH) |
|
III |
Revestiment d’ |
|
Vehicles |
|
IV |
Sobreembolicat amb fibra de carboni i revestiment de polímer |
Autobusos, 350 bar; fins a 700 bar |
Vehicles |
|
V |
Material compost sense folre metàl·lic ni de polímer |
1 000 bar |
Aplicacions aeroespacials |
Avantatges i inconvenients Una càrrega de combustible d’hidrogen pot proporcionar autonomies de l’ordre de centenars de quilòmetres i es pot repostar en pocs minuts. Aquest és l’avantatge pràctic més visible respecte a molts vehicles elèctrics amb bateria. En canvi, el rendiment energètic de tota la cadena sol ser menys favorable si es considera producció d’hidrogen, compressió, transport i conversió electroquímica. Per això les cèl·lules de combustible són especialment interessants quan la massa de bateria, el temps de parada o l’ús intensiu del vehicle són limitants.
Els inconvenients principals són el cost de la cèl·lula i del dipòsit, la dependència de catalitzadors cars, la infraestructura de repostatge limitada, la producció d’hidrogen baix en carboni i la gestió de seguretat d’un gas lleuger i inflamable a pressions altes.
|
Taula 5.7: Polítiques i finançament anunciats en alguns països per a l’hidrogen verd i els FCEV. Taula orientativa amb dades publicades el 2022; els objectius poden haver canviat. Adaptat de CME Group. |
||
|
País |
Objectius de desplegament per al 2030 |
Inversió pública (M€) |
|
País |
Objectius de desplegament per al 2030 |
Inversió pública (M€) |
| Continua a la pàgina següent | ||
|
Austràlia |
N/A |
900 M€ |
|
Canadà |
19 M€ | |
|
Califòrnia |
200 estacions de recàrrega (HRS) per al 2025 |
20 M€ |
|
Xina |
1.000.000 FCEV, 1.000 HRS per al 2030, 2.000 HRS per al 2035 |
0 M€ |
|
Unió Europea |
40 GW d’electròlisi |
4 300 M€ |
|
França |
6,5 GW d’electròlisi, 20.000–50.000 LV, 800–2.000 HD, 400–1.000 HRS |
8 200 M€ |
|
Alemanya |
5 GW d’electròlisi |
10 300 M€ |
|
Japó |
800.000 FCEV, 1.200 autobusos, 10.000 carretons elevadors, 900 HRS |
6 500 M€ |
|
Corea del Sud |
Producció anual de 6,2 milions de FCEV, 1.200 HRS, 80.000 taxis, 40.000 autobusos, 30.000 camions, 15 GW FC estacionari |
2 200 M€ |
|
Països Baixos |
30.000 FCEV, 3.000 HV |
80 M€ |
|
Espanya |
4 GW d’electròlisi, 5.000–7.500 FCEV (LV+HV), 100–200 autobusos, 100–150 HRS |
1 800 M€ |
Per ser útils en aplicacions automobilístiques, les cèl·lules de combustible han de ser compactes, produir una potència elevada i funcionar a baixa temperatura. Molts d’aquests requisits són contradictoris. Per exemple, alta potència i eficiència requereixen operar a temperatures altes, però els cotxes han de funcionar a temperatures de fins a −30 °C (arrencada hivernal), i poden necessitar un escalfament previ.
La humitat de la membrana sovint és crítica, especialment en el cas del Nafion, que limita la temperatura operativa per evitar l’assecament. També preocupa l’eficiència del catalitzador, l’enverinament i el cost. La reacció de reducció d’oxigen continua sent prou exigent perquè moltes PEMFC utilitzin metalls preciosos, en especial platí; reduir-ne la càrrega sense perdre durabilitat és una línia central de recerca[16].
La Figura 5.24 recull processos i limitacions de transport al càtode d’una PEMFC, especialment al voltant del catalitzador.
Els objectius del Departament d’Energia dels EUA publicats el 2012 per a una cèl·lula de combustible de vehicle incloïen una eficiència del 60% o superior al 25% de potència neta, una autonomia mínima de 250 milles i una durabilitat de 2 000 hores. Aquests valors serveixen com a exemple de com els requisits de materials s’expressen finalment en prestacions de vehicle.
La tecnologia ha avançat prou perquè, a més de Toyota, altres fabricants com Hyundai hagin comercialitzat vehicles de pila d’hidrogen com el Nexo. Tanmateix, continuen existint problemes de cost de producció de l’hidrogen, emmagatzematge i seguretat, infraestructura de repostatge, durabilitat i cost dels materials de la cèl·lula.
5.9 Exercicis
5.9.1 Compendi d’exercicis
Exercici 1. Productes de polimerització per condensació
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Quin serà l’estructura del polímer que sorgeix dels següents reactius? Adaptat de [1].
| Reactiu 1 | Reactiu 2 |
Exercici 2. Selecció de materials en automoció
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Per a cadascun dels components següents, proposa una família de materials adequada i justifica-la amb dues propietats rellevants. Indica també una limitació que caldria comprovar abans de validar el disseny.
|
Component |
Funció dominant |
Condició crítica |
|
Para-xocs |
Absorbir energia d’impacte |
Baixa massa i fabricació en sèrie |
|
Disc de fre |
Dissipar energia per fricció |
Temperatura elevada |
|
Parabrisa |
Transparència i seguretat |
Impacte i fragments |
|
Connector sota capó |
Aïllament elèctric |
Temperatura i humitat |
|
Dipòsit d’ |
Emmagatzematge a pressió |
Fatiga i permeabilitat |
Exercici 3. Vulcanització i pneumàtics
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Una empresa compara dues formulacions simplificades de cautxú per a pneumàtics:
| Formulació | Farciment dominant | Grau d’entrecreuament | |
| A | −55 °C | sílice funcionalitzada | mitjà |
| B | −15 °C | negre de carboni | alt |
-
1. Quina formulació triaries per a un pneumàtic d’hivern? Justifica-ho.
-
2. Quina pot tenir més resistència a la deformació permanent a temperatura moderada?
-
3. Quin paper fa el sofre en la vulcanització?
-
4. Per què reduir la resistència al rodament pot reduir el consum del vehicle?
Exercici 4. Sonda lambda i tensió de Nernst
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
La sonda lambda és un sensor d’oxigen situat a l’escapament. En un motor de gasolina permet estimar si la combustió treballa amb mescla rica o pobra i envia aquesta informació a la unitat de control perquè corregeixi la injecció. Una sonda lambda de banda estreta típica conté una ceràmica de zircona
estabilitzada amb ítria, conductora d’ions a alta temperatura, amb elèctrodes porosos de platí i una referència d’aire. La diferència de pressió parcial d’oxigen entre l’aire i els gasos d’escapament genera una tensió de Nernst[17, 5].
Per a gasolina, pren com a relació estequiomètrica aire/combustible , expressada en kg d’aire per kg de combustible. Considera dues mesures:
| Cas | ||
| A | 13.8 | 1,0 · 10−16 bar |
| B | 15.4 | 1,0 · 10−3 bar |
-
1. Calcula
per als dos casos i indica quin és ric i quin és pobre.
-
2. A 800 °C, amb
, calcula la tensió ideal:
Usa
,
i
en kelvin.
-
3. Una sonda de banda estreta sol donar tensió alta amb mescla rica i baixa amb mescla pobra. Són coherents els resultats amb aquesta regla?
-
4. Per què cal que el material ceràmic treballi calent?
Exercici 5. Composites i dipòsits d’hidrogen
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Els vehicles de pila de combustible poden utilitzar dipòsits de tipus IV: un liner polimèric envoltat per fibres de carboni en una matriu polimèrica. Respon:
-
1. Identifica la funció del liner, de la fibra, de la matriu i de la interfície fibra-matriu.
-
2. Per què la fibra de carboni és atractiva en aquest component?
-
3. Quin problema podria aparèixer si la interfície fibra-matriu és feble?
-
4. Compara breument un dipòsit de tipus III i un de tipus IV.
Basat en els criteris de materials compostos i d’emmagatzematge d’hidrogen del capítol 5[21, 12].
Exercici 6. Ceràmiques, vidres i funció química
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Relaciona cada component amb el motiu químic o estructural pel qual s’utilitza una ceràmica o un vidre:
| Component | Opcions de funció |
| Bugia | Aïllament elèctric i resistència tèrmica |
| Sonda lambda | Conductivitat iònica d’ |
| Catalitzador de tres vies | Suport porós i estable per dispersar Pt/Pd/Rh |
| Parabrisa laminat | Transparència i retenció de fragments |
| Disc carboni-ceràmica | Resistència a desgast i temperatura amb baixa massa |
El catalitzador de tres vies és el més corrent en vehicles de turisme i rep aquest nom perquè actua sobre tres famílies de gasos: CO, hidrocarburs residuals i NOx.
Escull tres dels cinc casos i explica per què una ceràmica o un vidre és millor que un metall o un polímer convencional en aquella funció. Indica també el risc mecànic principal de les ceràmiques.
Exercici 7. Diagrama de fases de l’aliatge estany-plom [13]
La figura mostra el diagrama de fases de l’aliatge estany-plom emprat en soldadures.
-
1. Quina composició triaries si vols la soldadura amb la temperatura de fusió més baixa?
-
2. Per a una composició global
dins la regió de dos sòlids, com determinaries gràficament les composicions i les proporcions de les dues fases sòlides?
5.9.2 Exercicis d’autoavaluació
Exercici 8. Densitat d’un metall FCC
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
El coure cristal·litza en una xarxa cúbica centrada a les cares (FCC). La longitud de l’aresta de la cel·la unitària és , la massa molar del coure és
i
.
-
1. Quants àtoms de Cu hi ha en una cel·la unitària FCC?
-
2. Calcula la densitat del coure a partir d’aquest model cristal·lí.
-
3. Compara el resultat amb
.
-
4. Quin tipus d’informació microscòpica no queda recollida en aquest càlcul?
Exercici 9. Grau de polimerització i cristallinitat
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Un polipropilè per a una peça interior d’automoció té una massa molecular mitjana en nombre . La unitat repetitiva del PP és
, de massa molar
.
-
1. Calcula el grau de polimerització mitjà en nombre,
.
-
2. Quants mols de cadenes polimèriques hi ha en
d’aquest PP?
-
3. Quants mols d’unitats repetitives conté aquesta mateixa massa?
-
4. Si la fracció cristal·lina és
, estima la densitat del material. Considera que
és la densitat que tindria la part cristal·lina del PP i que
és la densitat que tindria la part amorfa. En aquesta notació, el subíndex
vol dir cristal·lí i el subíndex
vol dir amorf. Usa la regla de les fraccions de volum específic:
Exercici 10. Regla de mescles en un composite
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Una làmina unidireccional de fibra de carboni i resina epoxi es prepara amb de fibra i
de matriu. Les dades són:
Els subíndexs i
indiquen fibra i matriu, respectivament.
-
1. Calcula la fracció volumètrica de fibra,
.
-
2. Calcula la densitat del composite.
-
3. Estima el mòdul longitudinal
, és a dir, el mòdul del composite quan la càrrega va en la direcció de les fibres, amb la regla de mescles directa.
-
4. Estima el mòdul transversal
, és a dir, el mòdul del composite quan la càrrega va perpendicular a les fibres, amb la regla inversa de mescles com a aproximació simple:
Exercici 11. Tensió en un dipòsit d’hidrogen
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Un dipòsit cilíndric d’hidrogen comprimit treballa a , que podem aproximar com
. El radi intern és
. Per a una estimació preliminar, usa el model de paret prima:
on és la tensió circumferencial,
és la tensió longitudinal i
és el gruix de paret.
-
1. Si la tensió admissible de disseny del composite és
, calcula el gruix mínim imposat per
.
-
2. Amb aquest gruix, quina és
?
-
3. Si es tria
, quina és
?
-
4. Per què aquest càlcul no és suficient per validar un dipòsit real?
Exercici 12. Temperatura de transició vítria i temperatura de fusió
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
La taula dona valors orientatius de i
per a tres polímers que poden aparèixer en components d’automoció. Els valors exactes depenen de la formulació, però són suficients per raonar el comportament mecànic.
| Polímer | Estructura dominant | ||
| PP (polipropilè) | semicristal·lí | −10 °C | 165 °C |
| PET (poli(tereftalat d’etilè)) | semicristal·lí | 70 °C | 255 °C |
| PC (policarbonat) | amorf | 145 °C | – |
-
1. Quin d’aquests polímers esperaríem que fos més rígid a 25 °C? Justifica-ho.
-
2. Quin podria deformar-se de manera més evident en un interior de vehicle exposat al sol a 80 °C?
-
3. Per què el policarbonat no té una
definida en aquesta taula?
-
4. Si cal fabricar una lent transparent de far, quin criteri afegiries a
i
?
Exercici 13. Polimerització per addició i per etapes
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Classifica les polimeritzacions següents com a polimerització en cadena/addició o polimerització per etapes. Escriu també quin enllaç o grup funcional domina la unitat repetitiva del polímer.
-
1.
-
2.
-
3. Àcid adípic,
, amb 1,6-hexandiamina,
.
-
4. Àcid tereftàlic,
, amb etilenglicol,
.
Adaptat de la discussió de polímers d’addició i de condensació de LibreTexts[2, 1].
Exercici 14. Xarxes metàl·liques i propietats
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
La taula resumeix tres estructures metàl·liques habituals.
| Estructura | Àtoms per cel·la | Coordinació | Factor d’empaquetament |
| BCC | 2 | 8 | 0,68 |
| FCC | 4 | 12 | 0,74 |
| HCP | 6 | 12 | 0,74 |
-
1. Quines estructures són compactes?
-
2. Per què molts metalls FCC són dúctils a temperatura ambient?
-
3. El carboni en l’acer és un solut substitucional o intersticial? Justifica-ho.
-
4. Per què la xarxa cristal·lina no és suficient per predir tota la resistència d’un aliatge?
Adaptat del capítol 5 i de la discussió de xarxes FCC/HCP a LibreTexts[9, 7].
Exercici 15. Regla de la palanca en un aliatge eutèctic
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Considera un aliatge binari amb composició global
B. A una certa temperatura dins la regió
, la línia d’equilibri talla les fronteres de fase a:
-
1. Calcula les fraccions màssiques de fase
i líquid
.
-
2. En refredar fins a la composició eutèctica
B, quin microconstituent apareix a la reacció eutèctica?
-
3. Explica la diferència entre fracció de fase i fracció de microconstituent.
Adaptat dels problemes de diagrames de fase i regla de la palanca de LibreTexts[10, 7].
Exercici 16. Materials d’una PEMFC d’automoció
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Una cèl·lula de combustible PEMFC treballa a 0,68 V sota càrrega. Un mòdul de vehicle connecta 360 cèl·lules en sèrie.
-
1. Quin voltatge aproximat proporciona el mòdul?
-
2. Escriu les semireaccions d’ànode i càtode en medi àcid.
-
3. Quina funció fa la membrana polimèrica?
-
4. Per què el càtode acostuma a ser més crític que l’ànode pel que fa al catalitzador?
Basat en la descripció de les PEMFC de LibreTexts i del capítol 5[3, 16].
Exercici 17. Diagrama de fases Al-Ni
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Respon les següents preguntes respecte al diagrama de fases Al-Ni:
a) Determina les reaccions invariants que tenen lloc durant el refredament a les temperatures 640 °C, 700 °C, 854 °C, i 1 133 °C, indicant l’equació de la reacció, la composició de cada fase en la reacció i el seu nom.
b) Quins compostos intermetàl·lics apareixen en el diagrama? Explica si representen una fusió congruent o incongruent.
c) Indica les fases presents, la fracció en massa i la composició de cada fase, i la fracció en massa de cada microconstituent per a un aliatge amb 21% de Ni a una temperatura de 600 °C.
5.9.3 Exercicis d’examens anteriors
Exercici 18. Aliatge Cu-Ag (Parcial 3, 2024-2025)
Mostra la resolució
Resolució disponible a Exercise.pdf i als materials d autoavaluacio daquest tema.
Utilitzant el diagrama de fases Ag-Cu,
-
1. Com interpretes les diferents fases que es mostren al diagrama?(1 punt)
-
2. a) Mostra sobre el diagrama i b) estima la quantitat, la composició química i les fraccions en massa de les fases i microconstituents presents a:(a) 1 punt + b) 1 punt addicional)
-
(a)
-
(b)
-
(c)
per a aliatges de composició 70% Cu.
-
Bibliografia
-
[1] 21.9: Polyamides and Polyesters - Step-Growth Polymers. en. Ag. de 2015. uRl: https://chem.libretexts.org/Bookshelves/Organic_Chemistry/Organic_Chemistry_(Morsch_et_al.)/21%3A_Carboxylic_Acid_Derivatives-_Nucleophilic_Acyl_Substitution_Reactions/21.09%3A_Polyamides_and_Polyesters_-_Step-Growth_Polymers (cons. 04-05-2025).
-
[2] 27.8: Polymers and Polymerization Reactions. en. Jul. de 2023. uRl: https://chem.libretexts.org/Bookshelves/General_Chemistry/Map%3A_General_Chemistry_(Petrucci_et_al.)/27%3A_Reactions_of_Organic_Compounds/27.08%3A_Polymers_and_Polymerization_Reactions (cons. 28-04-2026).
-
[3] 31.15: Proton Exchange Membrane Fuel Cells (PEMFCs). en. Ag. de 2023. uRl: https://eng.libretexts.org/Bookshelves/Materials_Science/TLP_Library_I/31%3A_Fuel_Cells/31.a15%3A_Proton_Exchange_Membran_Fuel_Cells_(PEMFCs) (cons. 28-04-2026).
-
[4] M. F. Ashby. Materials selection in mechanical design. 3rd ed. Amsterdam ; Boston: Butterworth-Heinemann, 2005. isbn: 978-0-7506-6168-3.
-
[5] Bosch Motorsport. Lambda sensors: Basic information. Accessed: 2026-04-29. 2011. uRl: https://www.bosch-motorsport.com/content/downloads/Raceparts/Resources/pdf/Basic%20Information_69090699_Lambda_Sensor_LSU_4.9.pdf.
-
[6] Geoffrey M. Bowers i Ruth A. Bowers. Understanding Chemistry through Cars. en. CRC Press, nov. de 2014. isbn: 978-1-4665-7184-6. 10.1201/b17581.
-
[7] William D. (Jr) Callister i David G. Rethwisch. Ciencia e ingeniería de los materiales. spa. 2ª ed., correspondiente a la 9ª ed. original ; reimpr. OCLC: 1225074616. Barcelona: Reverté, 2020. isbn: 978-84-291-7251-5.
-
[8] Juan Bautista Carda Castelló et al. Ciència dels materials: metalls, ceràmiques i polímers. ca. 1a ed. Universitat Jaume I, 2022. isbn: 978-84-18432-91-0. 10.6035/sapientia181.
-
[9] Chapter 1: Atomistic Structure of Materials. en. 2025. uRl: https://eng.libretexts.org/Courses/California_State_Polytechnic_University_Humboldt/Mechanical_Behavior_of_Material/Chapter_1%3A_Atomistic_Structure_of_Materials (cons. 28-04-2026).
-
[10] Chapter 4: Phase Diagrams. en. 2023. uRl: https://eng.libretexts.org/Courses/California_State_Polytechnic_University_Humboldt/Mechanics_and_Science_of_Materials/Chapter_4%3A_Phase_Diagrams (cons. 28-04-2026).
-
[11] Krishan K. Chawla. Composite Materials: Science and Engineering. 3a ed. New York, NY: Springer, 2012. isbn: 978-0-387-74365-3. 10.1007/978-0-387-74365-3.
-
[12] Qian Cheng et al. “Review of common hydrogen storage tanks and current manufacturing methods for aluminium alloy tank liners”. A: International Journal of Lightweight Materials and Manufacture 7.2 (març de 2024), pàg. 269 - 284. issn: 2588-8404. 10.1016/j.ijlmm.2023.08.002.
-
[13] Ken A. Dill i Sarina Bromberg. Molecular Driving Forces: Statistical Thermodynamics in Chemistry and Biology. New York: Garland Science, 2003. isbn: 0-8153-2051-5.
-
[14] DoITPoMS, University of Cambridge. The Lever Rule. Department of Materials Science and Metallurgy, University of Cambridge. CC BY-NC-SA 4.0. uRl: https://www.doitpoms.ac.uk/tlplib/phase-diagrams/lever.php (cons. 08-05-2026).
-
[15] Fuel-cell cars finally drive off the lot. en. uRl: https://cen.acs.org/articles/95/i38/Fuel-cell-cars-finally-drive.html (cons. 04-03-2025).
-
[16] Shimshon Gottesfeld. “Editors’ Choice—Review—Polymer Electrolyte Fuel Cell Science and Technology: Highlighting a General Mechanistic Pattern and a General Rate Expression for Electrocatalytic Processes”. en. A: Journal of The Electrochemical Society 169.12 (gen. de 2023). Publisher: IOP Publishing, pàg. 124518. issn: 1945-7111. 10.1149/1945-7111/acada3.
-
[17] Sleight Halley et al. “A review of zirconia oxygen, NOx, and mixed potential gas sensors – History and current trends”. A: Sensors and Actuators B: Chemical 419 (2022), pàg. 132602. issn: 0925-4005. 10.1016/j.snb.2022.132602.
-
[18] Silvia Mostoni et al. “Zinc-Based Curing Activators: New Trends for Reducing Zinc Content in Rubber Vulcanization Process”. A: Catalysts 9 (ag. de 2019), pàg. 664. 10.3390/catal9080664.
-
[19] Nicoguaro. Stress strain comparison brittle ductile.svg. Wikimedia Commons, CC BY 4.0. 2020. uRl: https://commons.wikimedia.org/wiki/File:Stress_strain_comparison_brittle_ductile.svg (cons. 08-05-2026).
-
[20] Akshat Patil, Arun Patel i Rajesh Purohit. “An overview of Polymeric Materials for Automotive Applications”. en. A: Materials Today: Proceedings 4.2 (2017), pàg. 3807 - 3815. issn: 22147853. 10.1016/j.matpr.2017.02.278.
-
[21] Xin Qian et al. “Effect of carbon fiber surface chemistry on the interfacial properties of carbon fibers/epoxy resin composites”. A: Journal of Reinforced Plastics and Composites 32 (març de 2013), pàg. 393 - 401. 10.1177/0731684412468369.
-
[22] Sigmund. Stress-strain curve.svg. Wikimedia Commons, public domain. 2007. uRl: https://commons.wikimedia.org/wiki/File:Stress-strain_curve.svg (cons. 08-05-2026).
-
[23] A. Vashchuk et al. “Application of ionic liquids in thermosetting polymers: Epoxy and cyanate ester resins”. A: eXPRESS Polymer Letters 12.10 (2018). Figure reproduced under CC BY-NC-ND 4.0, pàg. 898 - 917. 10.3144/expresspolymlett.2018.77.
-
[24] Wikipedia contributors. Lever rule. 2023. uRl: https://en.wikipedia.org/wiki/Lever_rule (cons. 06-05-2026).
-
[25] Wizard191. Lever rule.svg. Wikimedia Commons, CC BY-SA 3.0 Unported. 2010. uRl: https://commons.wikimedia.org/wiki/File:Lever_rule.svg (cons. 06-05-2026).