QIEP
Glutatió S-transferasa GstA
Grup B · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>sp|P0A9D2|GSTA_ECOLI Glutathione S-transferase GstA OS=Escherichia coli (strain K12) OX=83333 GN=gstA PE=1 SV=1 | 2024-2025 | seqüència problema
MKLFYKPGACSLASHITLRESGKDFTLVSVDLMKKRLENGDDYFAVNPKGQVPALLLDDGTLLTEGVAIMQYLADSVPDR
QLLAPVNSISRYKTIEWLNYIATELHKGFTPLFRPDTPEEYKPTVRAQLEKKLQYVNEALKDEHWICGQRFTIADAYLFT
VLRWAYAVKLNLEGLEHIAAFMQRMAERPEVQDALSAEGLK
Seqüència recuperada de UniProt P0A9D2. Longitud: 201 aminoàcids. Cisteïnes: 10, 147.
Identificació i estructura de referència
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a glutatió S-transferasa GstA. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | P0A9D2; gen: gstA |
| EC / BRENDA | 2.5.1.18 |
| Estructura principal | 1A0F |
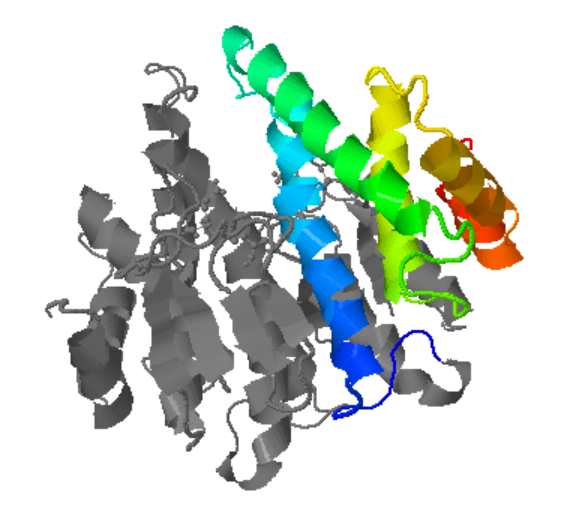
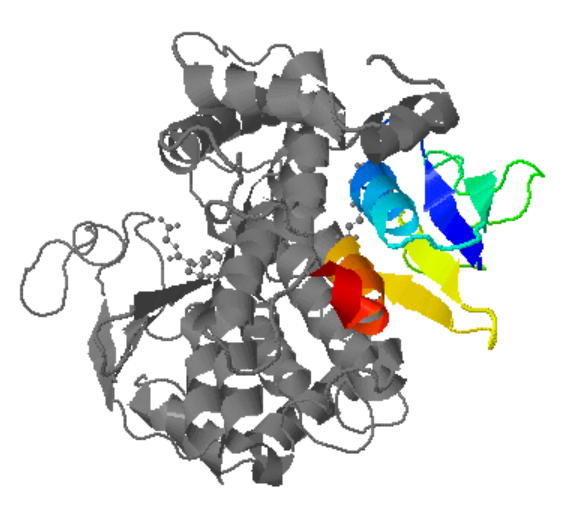
| Plegament o família | domini N-terminal d’unió al glutatió i domini C-terminal hidrofòbic; dímer funcional en moltes GST |
| Estructura secundària i lectura ChimeraX | domini N-terminal tipus tioredoxina amb el lloc G i domini C-terminal helicoidal; cal distingir la interfície dimèrica i la cavitat hidrofòbica del substrat |
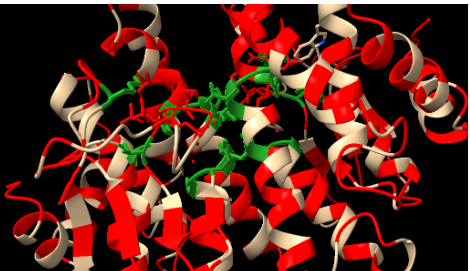
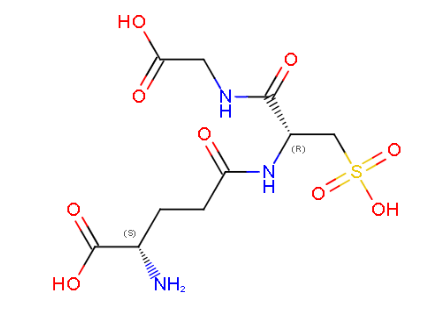
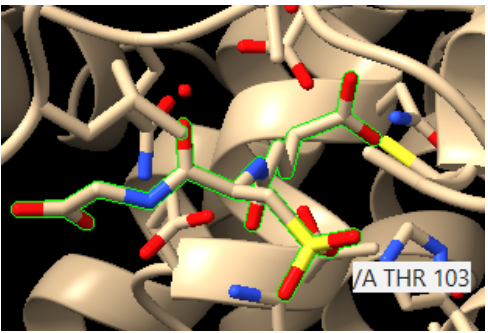
| Lligands, cofactors o lloc funcional | glutatió al lloc G; la química depèn de l’activació del tiol com a tiolat i de l’orientació del substrat electrofílic al lloc H |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. Les glutatió S-transferases catalitzen la conjugació del glutatió amb compostos electrofílics i participen en detoxificació cel·lular.
Arquitectura molecular
Les GST tenen un domini N-terminal que uneix glutatió i un domini C-terminal que configura el lloc hidrofòbic per al substrat electrofílic. Aquesta arquitectura separa clarament reconeixement de GSH i especificitat del segon substrat.
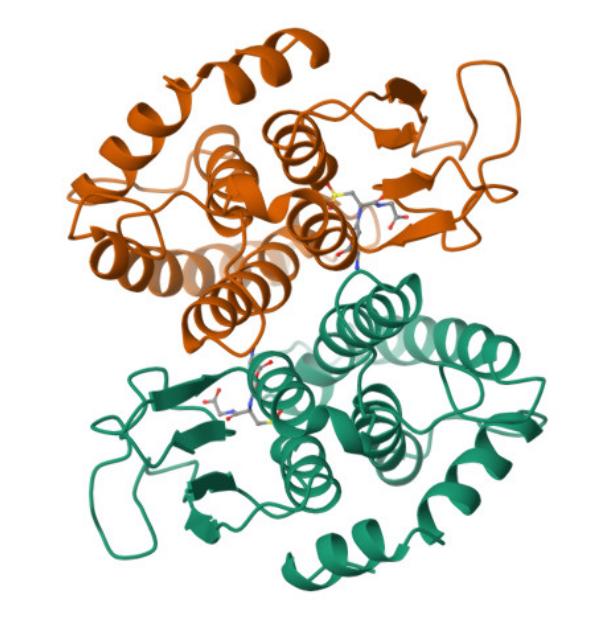
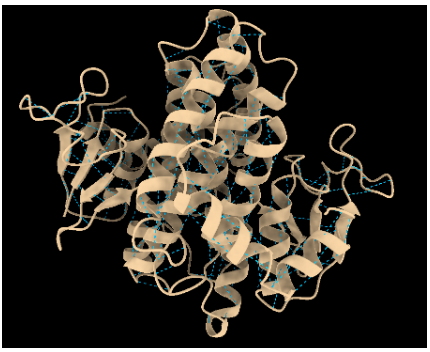
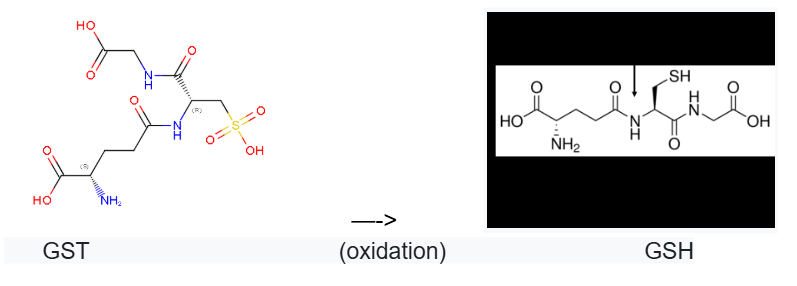
Lloc funcional i mecanisme
El mecanisme afavoreix la forma tiolat del glutatió i l’orienta per atacar el compost electrofílic. El producte és un conjugat més soluble, relacionat amb detoxificació i resposta a xenobiòtics.

La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Armstrong et al., 1997).
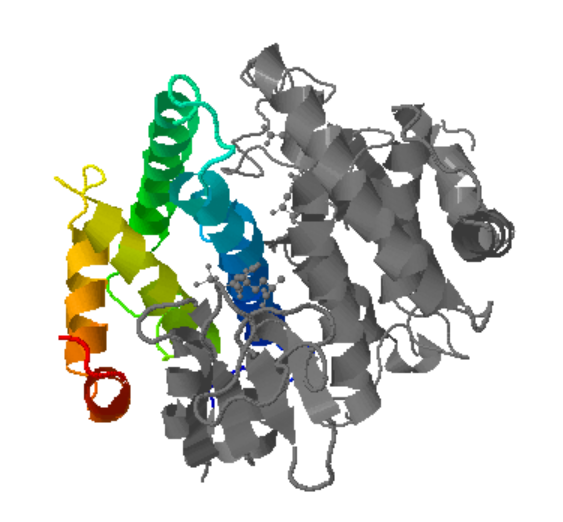
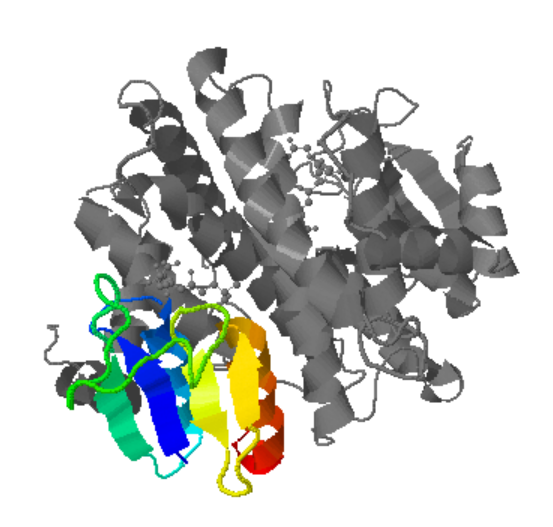
Modificacions i variants
En bacteris no s’ha d’assumir una regulació per modificacions posttraduccionals eucariotes; les variants rellevants són canvis en residus d’unió al glutatió o a la cavitat hidrofòbica. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.
Referències
- Armstrong, R. N. (1997). Structure, Catalytic Mechanism, and Evolution of the Glutathione Transferases. Chemical Research in Toxicology. doi: 10.1021/tx960072x.