QIEP
Cutinasa
Grup C · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>7YM9_1|Chains A, B|Poly(ethylene terephthalate) hydrolase|Cryptosporangium aurantiacum (134849) | 2024-2025 | seqüència problema
MAADNPYQRGPDPTNASIEAATGPFAVGTQPIVGASGFGGGQIYYPTDTSQTYGAVVIVPGFISVWAQLNWLGPRLASQG
FVVIGIETSVITDLPDPRGDQALAALDWATTRSPVASRIDRTRLAAAGWSMGGGGLRRAALQRPSLKAIVGMAPWNGERN
WSAVTVPTLFFGGSSDAVAspNDHAKPFYNSITRAEKDYIELRNADHFFPTSANTTMAKYFISWLKRWVDNDTRYTQFLC
PGPSTGLFAPVSASMNTCPFLEHHHHHH
Seqüència recuperada de RCSB PDB 7YM9. Longitud: 268 aminoàcids. Cisteïnes: 240, 258.
Identificació i estructura de referència
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a cutinasa. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | no fixat a la pàgina original; gen: cutinase/cut1 segons organisme |
| EC / BRENDA | 3.1.1.74 |
| Estructura principal | 7YM9/7YME segons comparació estructural |
| Plegament o família | plegament α/β hidrolasa amb triada catalítica Ser-His-Asp/Glu accessible al solvent |
| Estructura secundària i lectura ChimeraX | plegament α/β hidrolasa; cal marcar la triada Ser-His-Asp/Glu, els llaços d’accés i els ponts d’hidrogen que estabilitzen el nucli |
| Lligands, cofactors o lloc funcional | centre catalític de serina; el substrat és un èster de cutina o un èster lipídic model |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. La cutinasa hidrolitza enllaços èster en substrats com la cutina i és un model útil d’hidrolasa amb centre actiu accessible.
Arquitectura molecular
La cutinasa adopta un plegament d’hidrolasa α/β amb una serina catalítica accessible. La superfície oberta del centre actiu explica l’activitat sobre èsters de polímers com la cutina.
Lloc funcional i mecanisme
El mecanisme implica atac nucleofílic de la serina, intermedi acil-enzim i hidròlisi per aigua. La tríada catalítica i el forat oxianió estabilitzen els estats de transició.
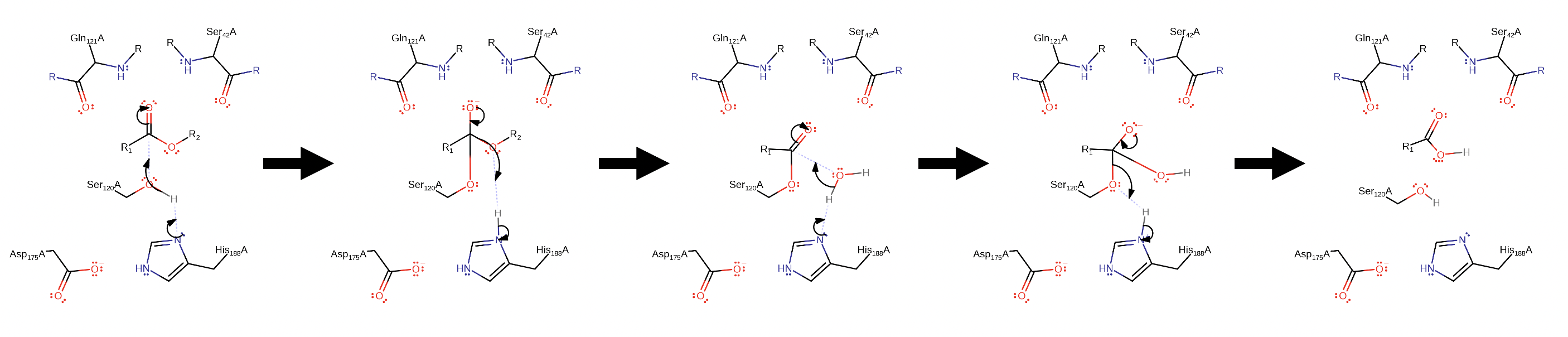
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Martinez et al., 1992).
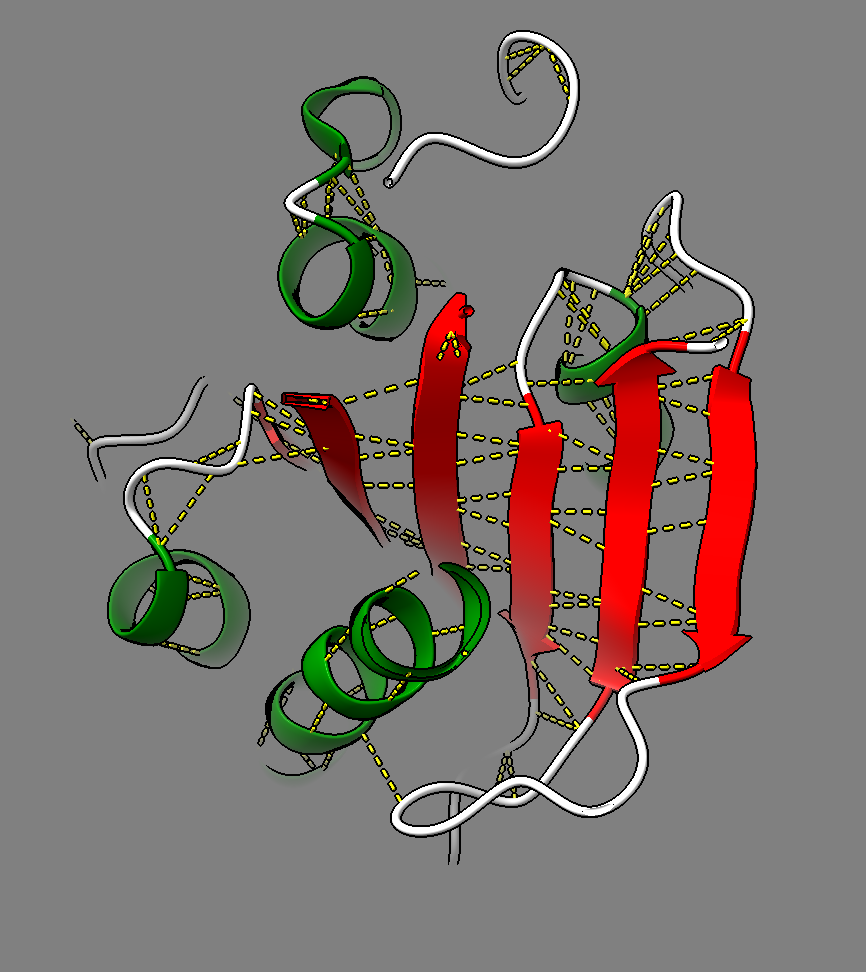
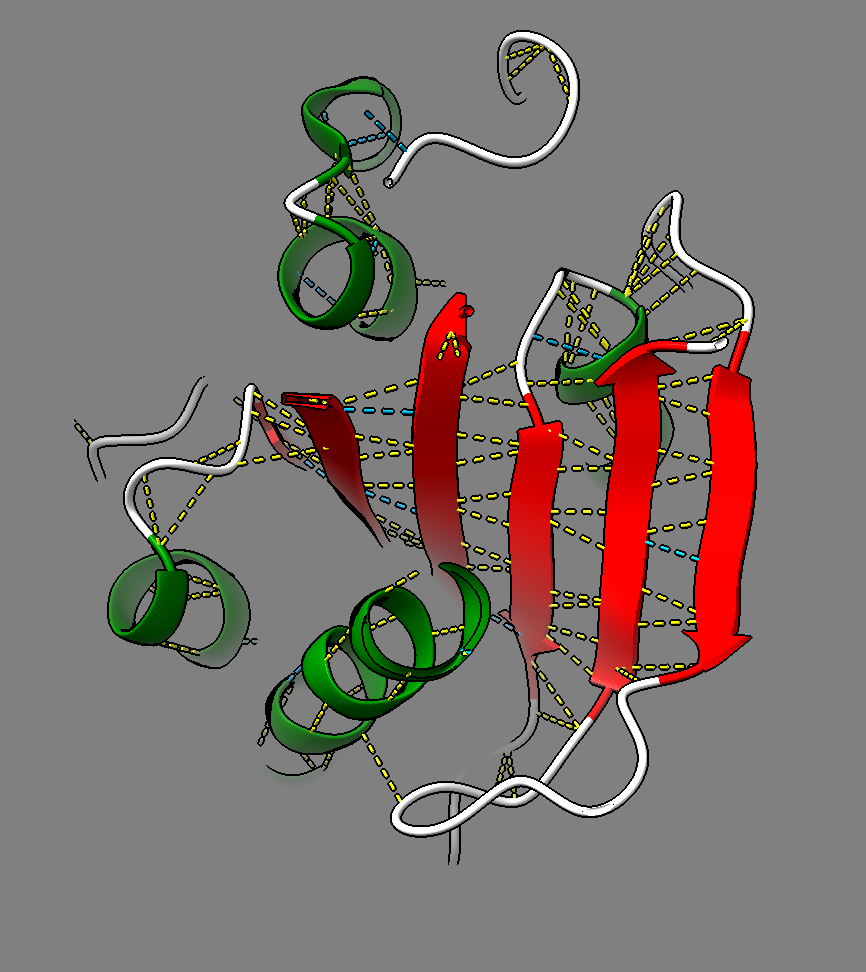
Modificacions i variants
La funció depèn sobretot de la triada catalítica i de la superfície d’accés al substrat; les modificacions posttraduccionals només s’han de discutir si provenen de la proteïna exacta o d’un homòleg alineat. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.
Referències
- Martinez, C. et al. (1992). Fusarium solani cutinase is a lipolytic enzyme with a catalytic serine accessible to solvent. Nature. doi: 10.1038/356615a0.