QIEP
Fenilalanina amoni-liasa
Grup D · Química i Enginyeria de Proteïnes 2024-2025
Seqüència problema
Aquesta és la cadena aminoacídica analitzada. La identificació de la proteïna o del constructe es fa a partir d’aquesta seqüència, i totes les correspondències amb UniProt, PDB, CATH/ECOD o AlphaFold s’han d’interpretar en relació amb aquesta numeració.
>Practica_1_Leire_Celia.md | 2024-2025 | seqüència problema
MAPSLDSISHSFANGVASAKQAVNGASTNLAVAGSHLPTTQVTQVDIVEKMLAAPTDSTLELDGYSLNLGDVVSAARKGR
PVRVKDSDEIRSKIDKSVEFLRSQLSMSVYGVTTGFGGSADTRTEDAISLQKALLEHQLCGVLPSSFDSFRLGRGLENSL
PLEVVRGAMTIRVNSLTRGHSAVRLVVLEALTNFLNHGITPIVPLRGTISASGDLSPLSYIAAAISGHPDSKVHVVHEGK
EKILYAREAMALFNLEPVVLGPKEGLGLVNGTAVSASMATLALHDAHMLSLLSQSLTAMTVEAMVGHAGSFHPFLHDVTR
PHPTQIEVAGNIRKLLEGSRFAVHHEEEVKVKDDEGILRQDRYPLRTSPQWLGPLVSDLIHAHAVLTIEAGQSTTDNPLI
DVENKTSHHGGNFQAAAVANTMEKTRLGLAQIGKLNFTQLTEMLNAGMNRGLPSCLAAEDPSLSYHCKGLDIAAAAYTSE
LGHLANPVTTHVQPAEMANQAVNSLALISARRTTESNDVLSLLLATHLYCVLQAIDLRAIEFEFKKQFGPAIVSLIDQHF
GSAMTGSNLRDELVEKVNKTLAKRLEQTNSYDLVPRWHDAFSFAAGTVVEVLSSTSLSLAAVNAWKVAAAESAISLTRQV
RETFWSAASTSSPALSYLSPRTQILYAFVREELGVKARRGDVFLGKQEVTIGSNVSKIYEAIKSGRINNVLLKMLA
Seqüència recuperada del lliurament original (Practica_1_Leire_Celia.md). Longitud: 716 aminoàcids. Cisteïnes: 140, 455, 467, 530.
Identificació i estructura de referència
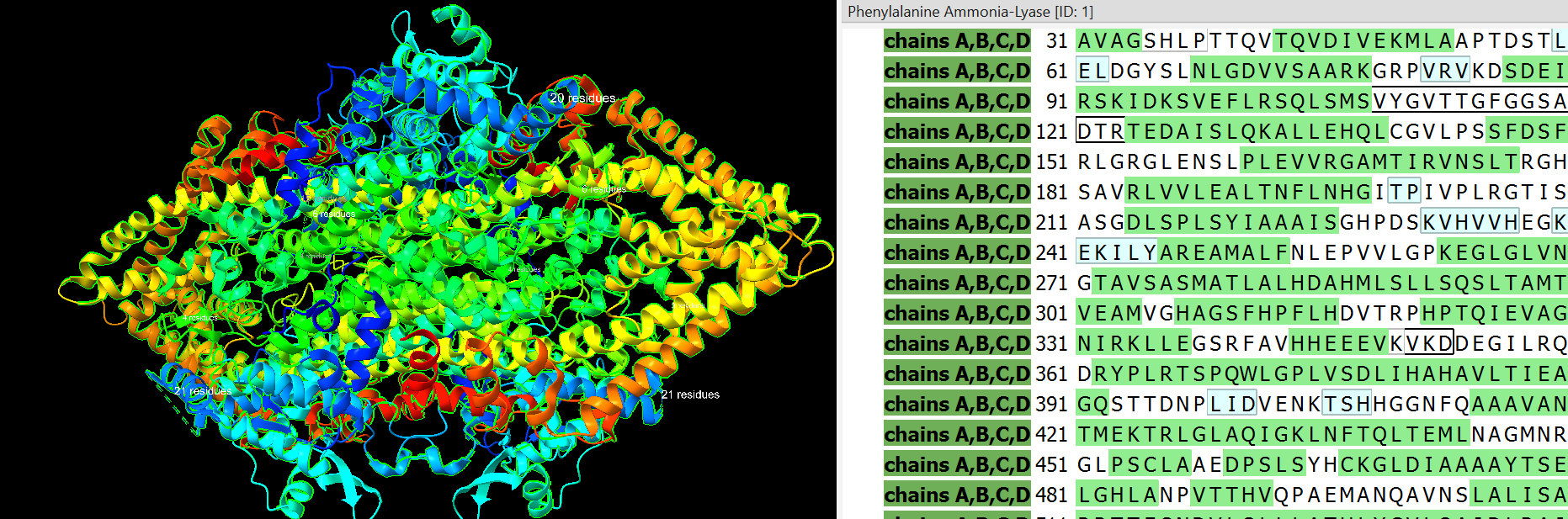
A partir de la seqüència anterior i de les bases de dades principals de seqüència i estructura, la proteïna s’identifica com a fenilalanina amoni-liasa. L’estructura de treball s’ha d’interpretar sempre comprovant que el PDB triat cobreix prou bé la seqüència analitzada; si hi ha diversos PDB possibles, la resolució només és decisiva després de comprovar cobertura, identitat, estat del lligand i rellevància biològica.
| Camp | Valor |
|---|---|
| UniProt / gen | segons organisme de la seqüència; gen: PAL |
| EC / BRENDA | 4.3.1.24 |
| Estructura principal | estructura PAL del lliurament o AlphaFold si no hi ha coincidència experimental completa |
| Plegament o família | enzim tetramèric de la família ammonia-lyase amb cofactor MIO generat autocatalíticament |
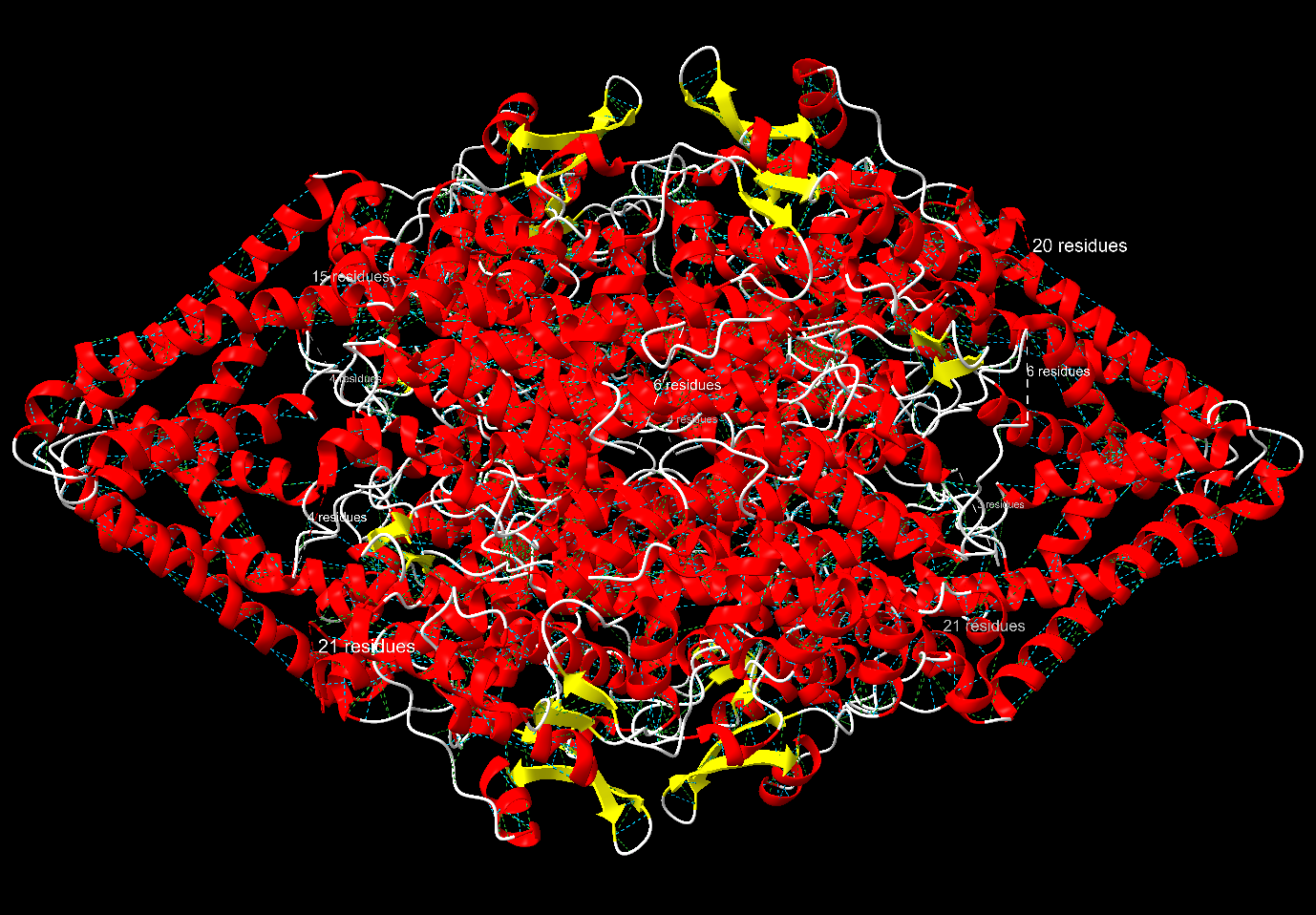
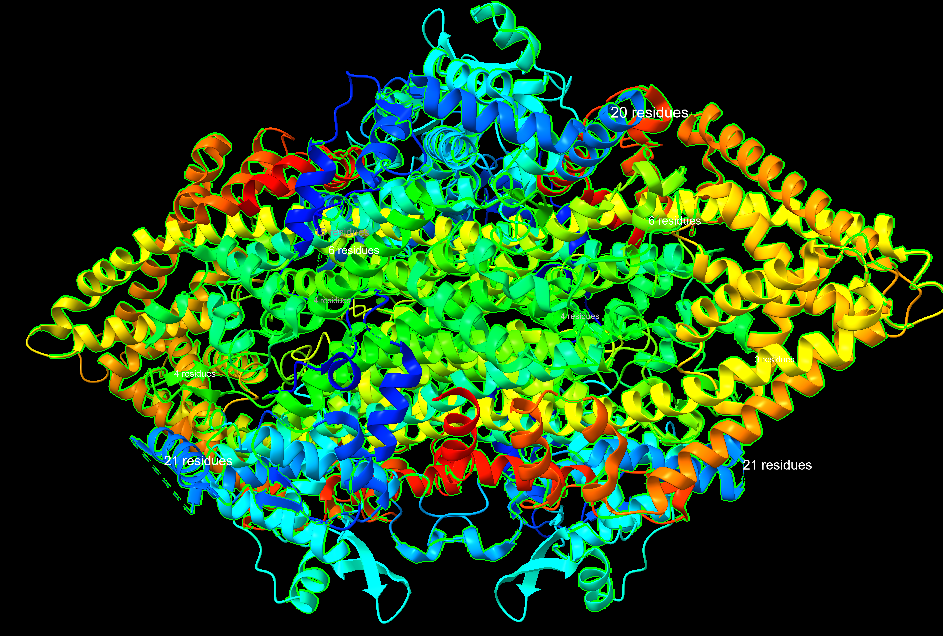
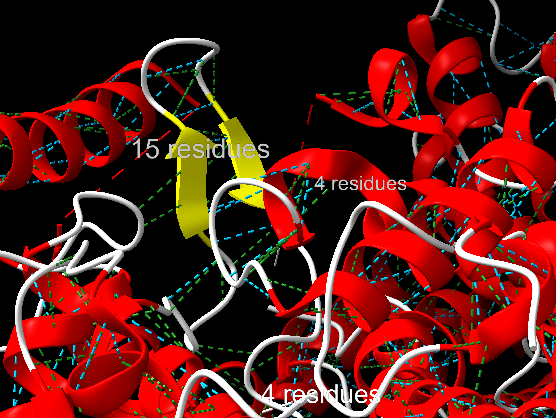
| Estructura secundària i lectura ChimeraX | arquitectura oligomèrica de PAL amb centre MIO; cal separar hèlixs de suport, interfícies de subunitat i túnel d’accés al substrat |
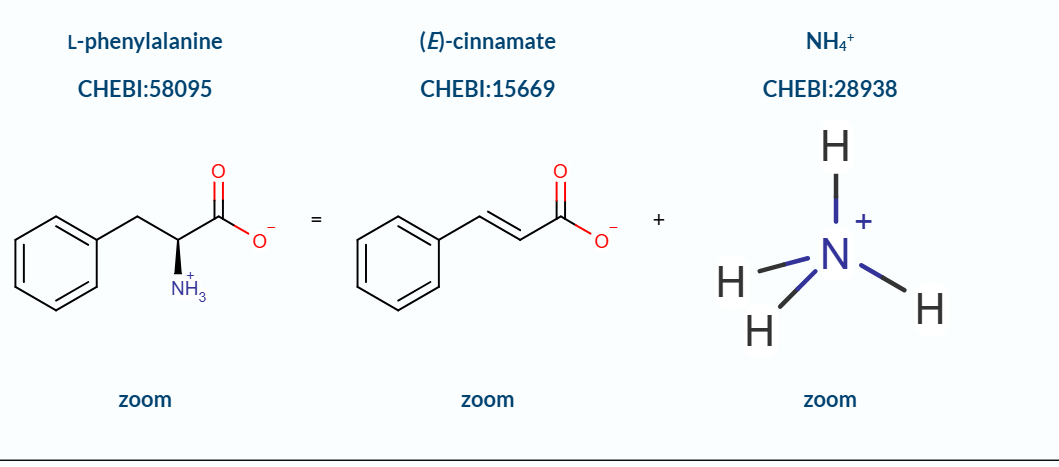
| Lligands, cofactors o lloc funcional | centre actiu amb MIO; la reacció elimina amoni de L-fenilalanina per formar trans-cinamat |
La transferència de residus funcionals requereix conservar la correspondència entre la numeració de la seqüència i la del model estructural, especialment quan l’estructura prové d’un homòleg, d’un domini aïllat o d’un model predictiu. La fenilalanina amoni-liasa elimina amoníac de la fenilalanina i connecta el metabolisme aromàtic amb la química del cofactor MIO.
Arquitectura molecular
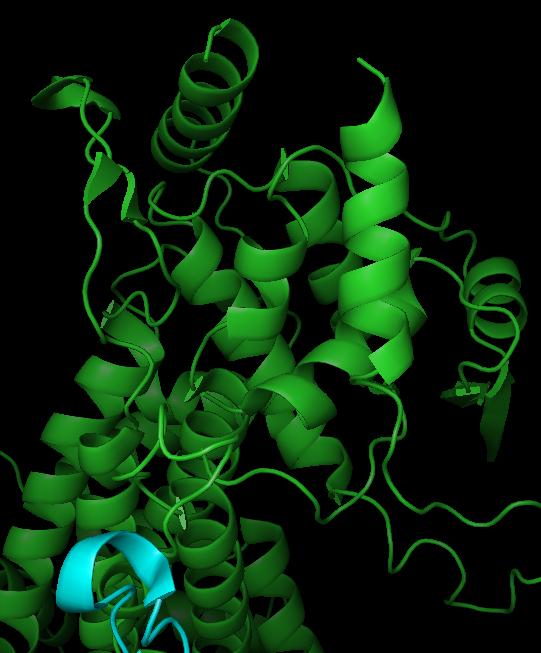
La PAL és un enzim sovint oligomèric amb un centre actiu que conté el cofactor MIO, generat autocatalíticament. La cavitat posiciona la fenilalanina i el seu anell aromàtic.
Lloc funcional i mecanisme
La reacció elimina amoníac de la fenilalanina i forma àcid trans-cinàmic. El cofactor MIO actua com a centre electrofílic i facilita la química d’eliminació.
La interpretació estructural i funcional d’aquest sistema es pot situar en el context de la literatura experimental corresponent (Ritter et al., 2004).
Modificacions i variants
La modificació important no és una modificació posttraduccional reguladora externa sinó la formació autocatalítica del grup MIO a partir del motiu intern conservat. Les modificacions, mutacions o variants només tenen valor estructural si s’indiquen amb residu, numeració i equivalència amb el PDB o model usat a les figures.
Relació seqüència-estructura-funció
La relació seqüència-estructura-funció s’ha d’interpretar situant sobre el model els residus que estabilitzen el plegament i els que defineixen el lloc funcional. Les variants, els lligands o els cofactors només són informatius si es manté la correspondència entre la numeració de la seqüència i la del PDB o model utilitzat.


Referències
- Ritter, H.; Schulz, G. E. (2004). Structural Basis for the Entrance into the Phenylpropanoid Metabolism Catalyzed by Phenylalanine Ammonia-Lyase. The Plant Cell. doi: 10.1105/tpc.104.025288.